
- Автоматизация
- Антропология
- Археология
- Архитектура
- Биология
- Ботаника
- Бухгалтерия
- Военная наука
- Генетика
- География
- Геология
- Демография
- Деревообработка
- Журналистика
- Зоология
- Изобретательство
- Информатика
- Искусство
- История
- Кинематография
- Компьютеризация
- Косметика
- Кулинария
- Культура
- Лексикология
- Лингвистика
- Литература
- Логика
- Маркетинг
- Математика
- Материаловедение
- Медицина
- Менеджмент
- Металлургия
- Метрология
- Механика
- Музыка
- Науковедение
- Образование
- Охрана Труда
- Педагогика
- Полиграфия
- Политология
- Право
- Предпринимательство
- Приборостроение
- Программирование
- Производство
- Промышленность
- Психология
- Радиосвязь
- Религия
- Риторика
- Социология
- Спорт
- Стандартизация
- Статистика
- Строительство
- Технологии
- Торговля
- Транспорт
- Фармакология
- Физика
- Физиология
- Философия
- Финансы
- Химия
- Хозяйство
- Черчение
- Экология
- Экономика
- Электроника
- Электротехника
- Энергетика
B. Бессимптомный
ЖДАНОВА В. А. 11 гр. Гломерулонефриты острый и хронический. (Glomerulonephritisacutaetchronica)
Вопросов -9 д. з.
1)расписать уровень 2 оценки силы рекомендаций со стороны пациентов, со стороны врача, дальнейших направлений исследований в соответствии с клиническими рекомендациями KDIGO;
Уровень 2(эксперты «полагают»)
ü Со стороны пациентов: Большая часть пациентов, оказавшихся в подобной ситуации, высказались бы за то, чтобы следовать рекомендуемым путем, однако значительная часть отвергла бы этот путь.
ü Со стороны врачей: Для разных пациентов следует подбирать различные варианты рекомендаций, подходящие именно им. Каждому пациенту необходима помощь в выборе и принятии решения, которое будет соответствовать ценностям и предпочтениям данного пациента.
ü Со стороны дальнейших направлений исследований: Рекомендации, вероятно, потребуют обсуждения с участием всех заинтересованных сторон до принятия их в качестве клинического стандарта.
2)Дать определение БПГН;
Быстропрогрессирующий гломерулонефрит (БПГН) – ургентная нефрологическая ситуация, требующая срочных диагностических и лечебных мероприятий. БПГН клинически характеризуется остронефритическим синдромом с быстро прогрессирующей почечной недостаточностью (удвоение креатинина в срок 3 мес. ), морфологически - наличием в более чем в 50% клубочков экстракапиллярных клеточных или фиброзно-клеточных полулуний
3)Полулуния при БПГН являются результатом повреждения клубочков воздействием анти-БМК-антител, АНЦА, иммунных комплексов и проникновением плазменных белков в пространство капсулы Шумлянского-Боумена.
4)Классификационная характеристика типов БПГН в виде таблицы из 4 колонок с заглавиями: тип БПГН, характеристика,, клинические варианты, частота;
| Тип БПГН | Характеристика | Клинические варианты | Частота |
| I | Опосредованный АТ к БМК: линейные отложения IgG при иммунологическом исследовании ткани почек | Синдром Гудспачера Изолированное поражение почек, ассоциированное с АТ к БМК | 5-7% |
| II | Иммунокомплексный: Гранулярные отложения иммуноглобулина в клубочках почки | Постинфекционный Постстрептококковый При висцеральных абсцессах Люпус-нефрит Геморрагический васкулитIgA-нефропатия Смешанная криоглобулинемияМембранопролиферативный ГН | 30-40% |
| III | АНЦА-ассоциированный: Малоиммунный с отсутствием иммунных отложений при иммунологическом иследовании | ГПА МПА ЭГПА | 50% |
| IV | Сочетание I и III типов | - | - |
| V | АНЦА-негативный васкулит почек: С отсутствием иммунных отложений | Идиопатический | 5-10% |
5)принципы лечения БПГН: сроки. содержание лечения;
Необходимо — по возможности — экстренное исследование сыворотки на наличие анти-БМК-антител и АНЦА; биопсия почки необходима для своевременной постановки диагноза (выявления ЭКГН и типа свечения антител — линейного, гранулярного, «малоиммунного»), оценки прогноза и выбора тактики терапии.
Для предотвращения необратимой катастрофической потери почечной функции необходимо срочно начинать и сразу же после установления клинического диагноза БПГН (остронефритического синдрома в сочетании с быстропрогрессирующей почечной недостаточностью при нормальных размерах почек и исключении других причин ОПН). (1В)
Лечение БПГН следует начинать еще до получения результатов диагностических исследований (серологических, морфологического) с пульс-терапии метилпреднизолоном в дозе до 1000 мг в течение 1-3 дней. (1A)
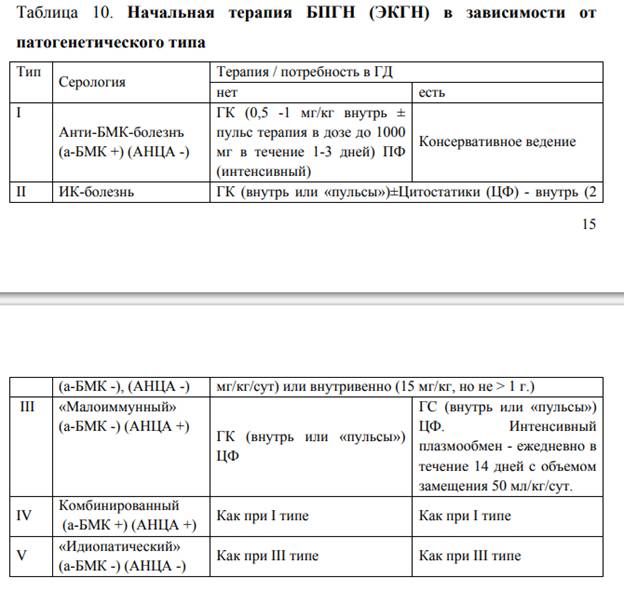
Всем пациентам с анти-БМК ГН (за исключением диализзависимых на момент установки диагноза, имеющих 100% полулуний по данным адекватной нефробиопсии и не имеющих при этом легочных кровотечений) следует начинать иммуносупрессиюциклофосфамидом, кортикостероидами и плазмаферезом. (1B)
При уровне креатинина крови менее 600 мкмоль/л назначают преднизолон внутрь в дозе 1мг/кг/сут и циклофосфамид в дозе 2 – 3 мг/кг/сут. По достижении стабильного клинического эффекта дозу преднизолона постепенно снижают в течение последующих 12 нед, а циклофосфамид полностью отменяют через 10 нед лечения. Терапию иммуносупрессивными препаратами сочетают с интенсивным плазмаферезом, который проводят ежедневно. В случае риска развития лёгочного кровотечения часть объема удалённой плазмы замещают свежезамороженной плазмой. Стабильный эффект
достигают после проведения 10 – 14 сеансов плазмафереза. Такой режим терапии позволяет добиться улучшения функции почек почти у 80% больных, причем снижение азотемии начинается уже через несколько суток после начала плазмафереза.
При содержании креатинина в крови более 600 мкмоль/л агрессивная терапия малоэффективна и улучшение функции почек возможно лишь у небольшого числа больных с недавней историей заболевания, бурным прогрессированием (в течение 1 – 2 нед) и наличием в биоптате почки потенциально обратимых изменений. В этих ситуациях основную терапию проводят в сочетании с сеансами гемодиализа.
В случае развития обострений синдрома Гудпасчера применяют тот же терапевтический режим, что и в дебюте болезни.
Проведение поддерживающей иммуносупрессивной терапии при анти-БМК ГН не целесообразно. (1D)
6)Какая тактика с позиций доказательной медицины (указать уровень и силу рекомендаций) в отношении поддерживающей терапии установлена для пациентов достигших полной ремисии;
Рекомендация 1: Пациентам, достигшим ремиссии, следует проводить поддерживающую терапию в менее агрессивных режимах. (1B)
Рекомендация 2.: Пациентам, у которых сохраняется полная ремиссия, поддерживающую терапию следует проводить не менее 18 месяцев. (2D)
Рекомендация 3: Пациентам, остающимся диализ-зависимыми и не имеющим внепочечных проявлений заболевания, поддерживающую терапию проводить не следует. (1C)
Рекомендация 4.: Режим поддерживающей терапии определяет основное заболевание, в рамках которого развился БПГН (1B).
Рекомендация 5.: Для лечения АГ необходимо применять антигипертензивные препараты различных групп в разных комбинациях с обязательным использованием ингибиторов АПФ или блокаторов рецепторов ангиотензина II с антипротеинурической и нефропротективной целями.
Рекомендация 6.: Пациентам с протеинурией более 500мг/с (белок/креатинин мочи > 50 мг/моль) назначение ингибиторов АПФ или блокаторов рецепторов ангиотензина II строго обязательно.
У пациентов с полной ремиссией в течение 3 мес. индукционного лечения можно отменить преднизон (преднизолон) через 5 мес. В других случаях применяется преднизон (преднизолон) в течение > 12 мес. У пациентов с вовлечением в процесс болезни верхних дыхательных путей в качестве поддерживающей терапии дополнительно используют котримоксазол (960 мг/сут. ). У больных, нуждающихся в заместительной почечной терапии, без экстраренальных симптомов заболевания и без ремиссии после 3-х мес. полного курса индукционного лечения, поддерживающую терапию не применяют.
В период ремиссии за исключением медицинского обследования, периодически оценивают функцию почек (анализ мочи, СКФ) и иммунных показателей, связанных с болезнью (АНЦА).
7)Какой патогенез развития иммунноА глобулиновой нефропатии?
Причина неизвестна, но данные свидетельствуют о том, что может существовать несколько механизмов, в том числе:
ü Увеличение продукции IgA1
ü Гликозилирование дефектного IgA1 создает повышенное связывание с мезангиальными клетками
ü Уменьшение клиренса IgA
ü Нарушения иммунной системы слизистой оболочки
ü Избыточная выработка цитокинов, стимулирующих пролиферацию мезангиальных клеток
Пусковым моментом патогенеза заболевания являются вовлечение различных антигенов, нарушение иммунного ответа, как системного, так и со слизистых оболочек, возможно, модулированное множественными генетическими влияниями, формирование иммунных комплексов.
Появляется все больше данных о том, что ведущую роль в патогенезе IgA нефропатии могут играть структурные аномалии молекулы IgA.
Механизм развития IgA-нефропатии – иммунокомплексный. Ведущую роль играют изменения структуры молекулы IgA, обусловленные нарушением процессов ее гликозилирования и полимеризации и, как следствие, нарушение взаимодействия с белками матрикса, рецепторами к IgA на мезангиальных и других клетках, с компонентами системы комплемента. Это приводит к депонированию полимерного IgAl в мезангии, активации синтеза клетками почек различных цитокинов и факторов роста с развитием характерных морфологических изменений.
Предрасположенность к IgA-нефропатии может быть обусловлена носительством определенных локусов системы HLA, в частности, для семейных форм идентифицированы локусы 6q22–23 (IGAN1), 4q26–31 (IGAN2) и 17q12–22 (IGAN3). Уточняется роль других возможных генов-кандидатов.
Провоцирующими факторами являются инфекции верхних и нижних дыхательных путей, острые инфекционные или вирусные гастроэнтериты, другие инфекции, вакцинация, УФоблучение.
8)Различают несколько (каких)? клинических вариантов течения иммунноА глобулиновой нефропатии;
A. Классический с повторными эпизодами макрогематурии (синфарингитная гематурия):
- чаще развивается у молодых лиц;
- характерно острое начало с эпизода макрогематурии, возникает на фоне инфекционного заболевания (обычно респираторной, реже мочевой, кишечной инфекции и т. д. ) одновременно или в первые 2-3 дня болезни и сохраняется от нескольких часов до нескольких дней;
- выявляется моча бурого цвета;
- могут отмечаться боли в поясничной области;
- наличие сгустков крови в моче не характерно;
- при микроскопическом исследовании осадка мочи обнаруживают дисморфные эритроциты, эритроцитарные цилиндры;
- выявляется протеинурия (ПУ);
- возможно нарушение функции почек, как правило, обратимое;
B. Бессимптомный
- чаще развивается у лиц после 40 лет;
- при обследовании выявляют персистирующую микрогематурию в сочетании с ПУ и/или АГ.
C. Атипичные формы протекают с клинической картиной, в большей степени сходной с другими вариантами гломерулярного повреждения – болезнь минимальных изменений с IgA-депозитами в мезангии; острое повреждение почек (ОПП), ассоциированное с эпизодами макрогематурии; быстропрогрессирующий ГН с полулуниями и депозитами IgA в мезангии.
9)При протеинурии нефротического уровня или персистированиипротеринурии более 1 грсут при адексатном контроле АЛ и СКФ> 50 мл /мин/1. 73м2 какая тактика показана?
Тактика: Для лечения используют ингибиторы ангиотензинпревращающего фермента (иАПФ) или блокаторы рецепторов ангиотензина II (БРА) при протеинурии от 0, 5 до 1 г/сут.
Рекомендуется длительное лечение иАПФ или БРА при ПУ более 1 г/сут, с повышением дозы препаратов в зависимости от АД.
Пациентам с персистирующей ПУ> 1 г/сут (несмотря на 3-6 месячное оптимальное поддерживающее лечение иАПФ/БРА, адекватный контроль артериального давления) и СКФ более 50 мл/мин/1, 73 м 2, предлагается проведение 6-месячного курса монотерапии кортикостероидами.
При отсутствии ответа на монотерапию кортикостероидами (ГКС) тактика дальнейшей иммуносупрессивной терапии не определена, соответствующие рандомизированные клинические исследования не проводились.
|
|
|
© helpiks.su При использовании или копировании материалов прямая ссылка на сайт обязательна.
|