
- Автоматизация
- Антропология
- Археология
- Архитектура
- Биология
- Ботаника
- Бухгалтерия
- Военная наука
- Генетика
- География
- Геология
- Демография
- Деревообработка
- Журналистика
- Зоология
- Изобретательство
- Информатика
- Искусство
- История
- Кинематография
- Компьютеризация
- Косметика
- Кулинария
- Культура
- Лексикология
- Лингвистика
- Литература
- Логика
- Маркетинг
- Математика
- Материаловедение
- Медицина
- Менеджмент
- Металлургия
- Метрология
- Механика
- Музыка
- Науковедение
- Образование
- Охрана Труда
- Педагогика
- Полиграфия
- Политология
- Право
- Предпринимательство
- Приборостроение
- Программирование
- Производство
- Промышленность
- Психология
- Радиосвязь
- Религия
- Риторика
- Социология
- Спорт
- Стандартизация
- Статистика
- Строительство
- Технологии
- Торговля
- Транспорт
- Фармакология
- Физика
- Физиология
- Философия
- Финансы
- Химия
- Хозяйство
- Черчение
- Экология
- Экономика
- Электроника
- Электротехника
- Энергетика
Равновесия в растворах электролитов
Равновесия в растворах электролитов
Задание 1. Расчет равновесных концентраций
Запишите уравнения диссоциации и выражения для константы диссоциации электролитов: А, Б, В. Рассчитайте равновесные концентрации ионов Н+, ОН- и катионов металла в растворе труднорастворимого соединения. Значения Кравн. см. в справочной таблице.
| вариант | Электролит А | Электролит Б | Электролит В |
| 0, 1м NaOH | 0, 1м CH3COOH | CaC2O4 (насыщ) | |
| 0, 1м HCl | 0, 1м NH4OH | BaSO4 (насыщ) | |
| 0, 05м H2SO4 | 0, 2м NH4OH | Ag3PO4 (насыщ) | |
| 0, 1м KOH | 0, 2м CH3COOH | CuS (насыщ) | |
| 0, 1м HNO3 | 0, 01м NH4OH | MgCO3 (насыщ) | |
| 0, 05м NaOH | 0, 02м H2C2O4 | Ni(OH)2 (насыщ) | |
| 0, 05м HCl | 0, 02м NH4OH | CdCO3 (насыщ) | |
| 0, 05м HNO3 | 0, 05м NH4OH | SrSO4 (насыщ) | |
| 0, 01м KOH | 0, 01м H2C2O4 | ZnCO3 (насыщ) | |
| 0, 1м NH4OH | 0, 01м HNO3 | PbF2 (насыщ) | |
| 0, 01м H2SO4 | 0, 02м NH4OH | Cu(OH)2 (насыщ) | |
| 0, 01м H3BO3 | 0, 5м KOH | Ni(OH)2 (насыщ) | |
| 0, 01м CH3COOH | 0, 05м KON | CO(OH)2 (насыщ) | |
| 0, 05м H2C2O4 | 0, 1м NaOH | AgCl (насыщ) | |
| 0, 01м HCN | 0, 5м Ba(OH)2 | BaSO4(насыщ) | |
| 0, 5м LiOH | 0, 01м HNO2 | AgJ (насыщ) | |
| 0, 1м RbOH | 0, 02м H3PO4 | PbSO4 (насыщ) | |
| 0, 01м H2CO3 | 0, 1м C6OH | Ag2CO3 (насыщ) | |
| 0, 5м Ba(OH)2 | 0, 01м H2SO3 | BaCO3 (насыщ) | |
| 0, 02м LiOH | 0, 5м H2CO3 | Ca(OH)2 (насыщ) | |
| 0, 1м H2Cr O4 | 0, 05м Ba(OH)2 | PbCrO4 (насыщ) | |
| 0, 5м KOH | 0, 1м H2S | CuS (насыщ) | |
| 0, 05м H3PO3 | 0, 1м C3OH | CdS (насыщ) | |
| 0, 1м H2Cr2O7 | 0, 05м LiOH | CaF2 (насыщ) | |
| 0, 05м NaOH | 0, 01м HBrO | MgF2 (насыщ) | |
| 0, 02м H3VO3 | 0, 005м LiOH | MgCO3 (насыщ) | |
| 0, 001м RbOH | 0, 001м HJO3 | CaSO4(насыщ) | |
| 0, 005м H3A5O3 | 0, 01м C5OH | CuS(насыщ) | |
| 0, 01м NH4OH | 0, 05м H2C2O4 | CaC2O4 (насыщ) | |
| 0, 01м HNO2 | 0, 05м Ba(OH)2 | Cr(OH)3 (насыщ) |
Задание 2. Предсказание направления процессов.
| Запишите выражение Крав для системы А. В каком направлении сместится равновесие в системе А при введении вещества Б. Укажите ион ответственный за смещение равновесия в системе А. |
Равновесные системы.
| вариант | Система А | Вещество В |
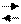   CH3COOH CH3COO-+H+ CH3COOH CH3COO-+H+
| CH3COONa (крист) | |
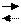   NH4OH NH4-+OH- NH4OH NH4-+OH-
| NH4Cl (крист) | |
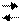   BaCO3(нас) Ba2++CO32- BaCO3(нас) Ba2++CO32-
| HCl (2м) | |
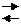   Cu(OH)2(н) Cu2++2OH- Cu(OH)2(н) Cu2++2OH-
| HCl (2м) | |
 [Fe(SCN)6] [Fe(SCN)6]   3- Fe3++6SCN- 3- Fe3++6SCN-
| NaF(крист) | |
   H2C2O4 2H++C2O42- H2C2O4 2H++C2O42-
| Na2C2O4 (крист) | |
   Al(OH)3(нас) Al3++3OH- Al(OH)3(нас) Al3++3OH-
| KOH (2м) | |
    SbCl3+H2O SbOCl +2HCl SbCl3+H2O SbOCl +2HCl
| HCl (2м) | |
   Cu(OH)2(нас) Cu2++2OH- Cu(OH)2(нас) Cu2++2OH-
| NH3H2O (конц) | |
   CaSO4(нас) Ca2++SO42- CaSO4(нас) Ca2++SO42-
| CaCl2 (2м) | |
   PbCl2(нас) Pb2++2Cl- PbCl2(нас) Pb2++2Cl-
| HCl (2м) | |
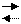   AgCl(нас) Ag++Cl- AgCl(нас) Ag++Cl-
| HCl (2м) | |
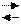   Ni(OH)2(нас) Ni2++2OH- Ni(OH)2(нас) Ni2++2OH-
| HCl (2м) | |
   Cu(OH)2(нас) Cu2++2OH- Cu(OH)2(нас) Cu2++2OH-
| NH3H2O (конц) | |
   HgJ2(нас) Hg2++2J- HgJ2(нас) Hg2++2J-
| KJ (конц) | |
   H2CO3 H++HCO3- H2CO3 H++HCO3-
| NaHCO3 (крист) | |
   CH3COOH CH3COO-+H+ CH3COOH CH3COO-+H+
| HCl (2м) | |
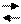   H3PO4 H++H2PO4- H3PO4 H++H2PO4-
| KH2PO4 (крист) | |
   H2S H++HS- H2S H++HS-
| HCl (2м) | |
   H2SO3 H++HSO3- H2SO3 H++HSO3-
| NaHSO3 (крист) | |
   HNO2 H++NO2- HNO2 H++NO2-
| KNO2 (крист) | |
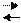   H2C2O4 2H++C2O42- H2C2O4 2H++C2O42-
| K2C2O4 (крист) | |
   H3PO3 H++H2PO3- H3PO3 H++H2PO3-
| HNO3 (2м) | |
   H2CrO4 2H++CrO42- H2CrO4 2H++CrO42-
| BaCl2 (2м) | |
   NH4OH NH4++OH- NH4OH NH4++OH-
| HCl (2м) | |
   CaCrO4(нас) Ca2++CrO42- CaCrO4(нас) Ca2++CrO42-
| HCl (2м) | |
   Fe(OH)3(нас) Fe3++3OH- Fe(OH)3(нас) Fe3++3OH-
| HNO3 (2м) | |
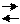   H3BO3(нас) H++H2BO3- H3BO3(нас) H++H2BO3-
| Na3BO3 (крист) | |
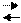   NH4OH NH4++OH- NH4OH NH4++OH-
| CH3COOHNH4 (крист) | |
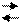   CH3COOH CH3COO-+H+ CH3COOH CH3COO-+H+
| CH3COONH4 (крист) |
|
|
|
© helpiks.su При использовании или копировании материалов прямая ссылка на сайт обязательна.
|