
- Автоматизация
- Антропология
- Археология
- Архитектура
- Биология
- Ботаника
- Бухгалтерия
- Военная наука
- Генетика
- География
- Геология
- Демография
- Деревообработка
- Журналистика
- Зоология
- Изобретательство
- Информатика
- Искусство
- История
- Кинематография
- Компьютеризация
- Косметика
- Кулинария
- Культура
- Лексикология
- Лингвистика
- Литература
- Логика
- Маркетинг
- Математика
- Материаловедение
- Медицина
- Менеджмент
- Металлургия
- Метрология
- Механика
- Музыка
- Науковедение
- Образование
- Охрана Труда
- Педагогика
- Полиграфия
- Политология
- Право
- Предпринимательство
- Приборостроение
- Программирование
- Производство
- Промышленность
- Психология
- Радиосвязь
- Религия
- Риторика
- Социология
- Спорт
- Стандартизация
- Статистика
- Строительство
- Технологии
- Торговля
- Транспорт
- Фармакология
- Физика
- Физиология
- Философия
- Финансы
- Химия
- Хозяйство
- Черчение
- Экология
- Экономика
- Электроника
- Электротехника
- Энергетика
Насыщенный пар. Давление насыщенного пара зависит от температуры
Насыщенный пар
На предыдущих уроках мы ввели понятие идеального газа в качестве модели, в рамках которой справедливы все газовые законы, которые мы изучали. Однако это не означает, что молекулярная физика ограничивается изучением только идеальных газов. Для реальных газов наши выкладки тоже справедливы. Однако связь параметров реальных газов между собой выглядит немного иначе.
Рассмотрим такой реальный газ, как насыщенный пар. Насыщенный пар – пар, находящийся в динамическом равновесии со своей жидкостью. То есть количество молекул жидкости, покидающих жидкость за некий отрезок времени, в среднем равно количеству молекул пара, возвращающихся обратно в жидкость (см. рис. 1). Область насыщенного пара всегда есть над любой поверхностью жидкости. Чтобы создать более широкую область, следует предотвратить утечку молекул пара в окружающую среду (герметично закрыть сосуд).
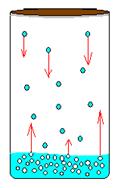
Рис. 1
Для понимания отличий насыщенного пара от идеального газа нужно представить себе два опыта.
Во-первых, возьмём герметично закрытый сосуд с водой и начнём его нагревать. С увеличением температуры молекулы жидкости будут иметь всё большую кинетическую энергию, и всё большее количество молекул сможет вырваться из жидкости (см. рис. 2), следовательно, будет расти концентрация пара и, следовательно, его давление. То есть:
Давление насыщенного пара зависит от температуры
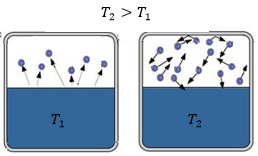
Рис. 2.
Если поместить жидкость с её насыщенным паром под подвижный поршень и начать этот поршень опускать, то концентрация насыщенного пара увеличится из-за уменьшения объёма. Но через некоторое время пар перейдёт с жидкостью к новому динамическому равновесию путём конденсации лишнего количества пара, и давление в итоге не поменяется. То есть:
|
|
|
© helpiks.su При использовании или копировании материалов прямая ссылка на сайт обязательна.
|