
- Автоматизация
- Антропология
- Археология
- Архитектура
- Биология
- Ботаника
- Бухгалтерия
- Военная наука
- Генетика
- География
- Геология
- Демография
- Деревообработка
- Журналистика
- Зоология
- Изобретательство
- Информатика
- Искусство
- История
- Кинематография
- Компьютеризация
- Косметика
- Кулинария
- Культура
- Лексикология
- Лингвистика
- Литература
- Логика
- Маркетинг
- Математика
- Материаловедение
- Медицина
- Менеджмент
- Металлургия
- Метрология
- Механика
- Музыка
- Науковедение
- Образование
- Охрана Труда
- Педагогика
- Полиграфия
- Политология
- Право
- Предпринимательство
- Приборостроение
- Программирование
- Производство
- Промышленность
- Психология
- Радиосвязь
- Религия
- Риторика
- Социология
- Спорт
- Стандартизация
- Статистика
- Строительство
- Технологии
- Торговля
- Транспорт
- Фармакология
- Физика
- Физиология
- Философия
- Финансы
- Химия
- Хозяйство
- Черчение
- Экология
- Экономика
- Электроника
- Электротехника
- Энергетика
Опорный конспект №2 «ЦИКЛОАЛКАНЫ»
Стр 1 из 2Следующая ⇒
Опорный конспект №2 «ЦИКЛОАЛКАНЫ»
Циклоалканы – предельные углеводороды, циклические молекулы которых состоят из 3 и более атомов углерода.
Общая формула - СnH2n
Тип гибридизации всех атомов С - sp3,
Валентный угол 109028' (гибридные облака направлены к вершинам тетраэдра),
Длина связи С-С равна 0, 154нм, связи С-С и С-Н являются σ -связями
Виды изомерии – изомерия углеродного скелета
- межклассовая (с алкенами)
- пространственная (цис-транс).
Химические свойства
| Взаимодействие | Уравнение реакции |
| 1. р. замещения (Свойство общее с алканами) (разрыв связи С-Н) (характерны для больших циклов, где С ≥ 5 ) | 1. Галогенирование(+Cl2, +Br2)
(с йодом реакция не идёт ни при каких условиях)
  +Br2 +Br2  Br +НBr
циклопентан бромциклопентан
2. Нитрование (+HNO3) Br +НBr
циклопентан бромциклопентан
2. Нитрование (+HNO3)
  + HO-NO2 + HO-NO2 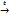 NO2 + Н2O
циклопентан нитроциклопентан NO2 + Н2O
циклопентан нитроциклопентан
|
| 2. р. присоединения (протекают с разрывом цикла) (характерны для небольших циклов, где С =3, 4 ) | 1.   Галогенирование(+Cl2, +Br2) Галогенирование(+Cl2, +Br2)
 +Br2 +Br2 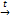 Br -СН2-СН2-СН2- Br
циклопропан 1, 3-дибромпропан
2. Гидрирование (+H2)
+ H2 Br -СН2-СН2-СН2- Br
циклопропан 1, 3-дибромпропан
2. Гидрирование (+H2)
+ H2  H3С-СН2-СН3
циклопропан пропан
3. Гидрогалогенирование (+HCl, +HBr)
+ HCl H3С-СН2-СН3
циклопропан пропан
3. Гидрогалогенирование (+HCl, +HBr)
+ HCl  H3С-СН2-СН2-Cl
циклопропан хлорпропан H3С-СН2-СН2-Cl
циклопропан хлорпропан
|
| 4. р. окисление | 1. Горение (полное окисление):
Общее уравнение СnН2n +  О2= nС02 +nН2О +Q О2= nС02 +nН2О +Q
|
| 5. р. отщепление | 1. Дегидрирование (-H2)
1.   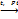  + 3Н2
циклогексан бензол + 3Н2
циклогексан бензол
|
|
|
|
© helpiks.su При использовании или копировании материалов прямая ссылка на сайт обязательна.
|