
- Автоматизация
- Антропология
- Археология
- Архитектура
- Биология
- Ботаника
- Бухгалтерия
- Военная наука
- Генетика
- География
- Геология
- Демография
- Деревообработка
- Журналистика
- Зоология
- Изобретательство
- Информатика
- Искусство
- История
- Кинематография
- Компьютеризация
- Косметика
- Кулинария
- Культура
- Лексикология
- Лингвистика
- Литература
- Логика
- Маркетинг
- Математика
- Материаловедение
- Медицина
- Менеджмент
- Металлургия
- Метрология
- Механика
- Музыка
- Науковедение
- Образование
- Охрана Труда
- Педагогика
- Полиграфия
- Политология
- Право
- Предпринимательство
- Приборостроение
- Программирование
- Производство
- Промышленность
- Психология
- Радиосвязь
- Религия
- Риторика
- Социология
- Спорт
- Стандартизация
- Статистика
- Строительство
- Технологии
- Торговля
- Транспорт
- Фармакология
- Физика
- Физиология
- Философия
- Финансы
- Химия
- Хозяйство
- Черчение
- Экология
- Экономика
- Электроника
- Электротехника
- Энергетика
Отчёт по лабораторной работе на тему: «Изучение кинетики реакции гидролиза сахарозы»
Выполнили студентки 3 курса 4 группы:
Пузык Александра, Степанова Кира
Преподаватель:
Трофимова Майя Александровна
Теоретические основы.
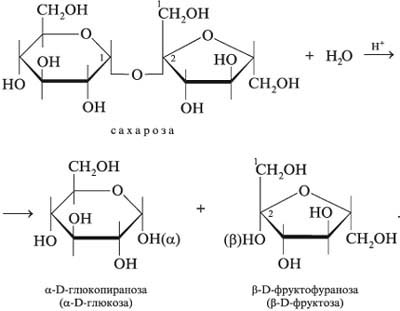 Сахароза гидролизуется с образованием D-фруктозы иD-глюкозы (инвертный сахар):
Сахароза гидролизуется с образованием D-фруктозы иD-глюкозы (инвертный сахар):

|
Без катализаторов реакция практически не идет. Гидролиз ускорятся при добавлении кислот (специфический катализ). Предложен следующий механизм:
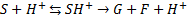
РаспадкомплексаSH+на продукты является лимитирующим.
Реакция имеет первый порядок как по сахарозе, так и по гидроксониевым ионам. Константа скорости псевдопервого порядка равна 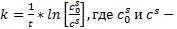 начальная и текущая концентрации сахарозы.
начальная и текущая концентрации сахарозы.
Сахароза и продукты ее гидролиза обладают асимметрическими атомами углерода и являются оптически активными, или деятельными. При прохождении линейно-поляризованного света через растворы этих веществ наблюдается вращение плоскости поляризации. Сахароза вращает вправо, а раствор продуктов гидролиза – влево.
Для растворов существует закон, согласно которому угол поворота плоскости поляризации α прямо пропорционален толщине слоя раствора dи концентрации активного веществас:
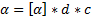 , где
, где 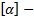 удельное вращение. Оно является характеристикой вращательной способности вещества и зависит от температуры, длины волны и растворителя. Для смеси оптически активных веществ угол поворота равен алгебраической сумме углов поворота для каждого оптически активного вещества.
удельное вращение. Оно является характеристикой вращательной способности вещества и зависит от температуры, длины волны и растворителя. Для смеси оптически активных веществ угол поворота равен алгебраической сумме углов поворота для каждого оптически активного вещества.
Тогда формула для константы скорости примет вид: 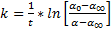 , где
, где 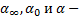 конечное, начальное и текущее значение угла вращения соответственно.
конечное, начальное и текущее значение угла вращения соответственно.
Проведение опыта.
1. Экспериментальные значения температуры, концентрации, значения углов вращений.
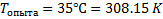
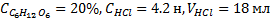
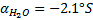 (в дальнейших расчетах этот показатель уже учтен);
(в дальнейших расчетах этот показатель уже учтен);
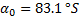 ;
; 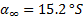
2. Ход работы.
В мерную колбу на 50 мл было налито 18 мл соляной кислоты, в другие две колбы налиты дистиллированная вода и 20% раствор сахарозы и поставлены в термостат с T=35⁰ C.
На сахариметре работа проводилась с желтым светофильтром. Сначала в кювету залили дистиллированную воду (записали 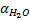 ). После этого измерили начальную величину угла вращения сахарозы (
). После этого измерили начальную величину угла вращения сахарозы ( 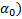 .
.
Приготовление реакционной смеси: в мерную колбу, в которой находилась соляная кислота, было добавлено 25 мл сахарозы и 7 мл воды. Последняя была тщательно перемешана, залита в кювету, а остатки были поставлены в термостат при T=70⁰ C(для последующего определения конечного вращения ( 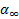 ). С интервалом в одну-две минуты проводилось определение угла вращения. Данные помещены в таблицу, последняя строчка которой отвечает значению угла вращения по завершении реакции (
). С интервалом в одну-две минуты проводилось определение угла вращения. Данные помещены в таблицу, последняя строчка которой отвечает значению угла вращения по завершении реакции ( 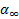 ).
).
3. 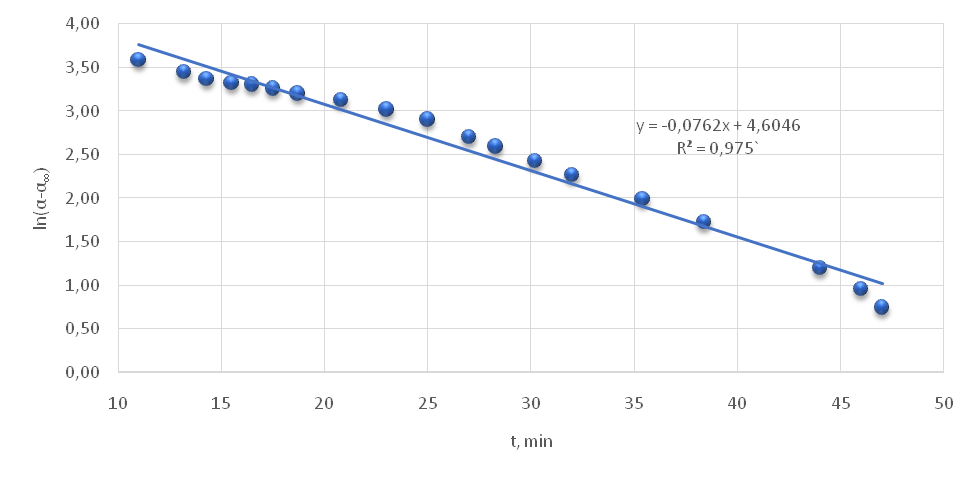 Расчёты и графики.
Расчёты и графики.
| № | 
| 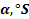
| 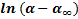
| 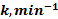
| № | 
| 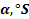
| 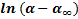
| 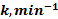
|
| 20, 2 | 3, 58 | 9, 13*10-2 | -0, 1 | 2, 90 | 6, 99*10-2 | ||||
| 13, 2 | 15, 6 | 3, 44 | 8, 67*10-2 | 28, 3 | -1, 6 | 2, 70 | 7, 07*10-2 | ||
| 14, 3 | 13, 3 | 3, 36 | 8, 56*10-2 | 30, 2 | -3, 8 | 2, 59 | 7, 16*10-2 | ||
| 15, 5 | 12, 2 | 3, 32 | 8, 19*10-2 | -5, 55 | 2, 42 | 7, 27*10-2 | |||
| 16, 5 | 11, 7 | 3, 30 | 7, 81*10-2 | 35, 4 | -7, 9 | 2, 26 | 7, 35*10-2 | ||
| 17, 5 | 10, 75 | 3, 26 | 7, 61*10-2 | 38, 4 | -9, 6 | 1, 99 | 7, 46*10-2 | ||
| 18, 7 | 9, 45 | 3, 20 | 7, 44*10-2 | -11, 8 | 1, 72 | 7, 71*10-2 | |||
| 20, 8 | 7, 5 | 3, 12 | 7, 06*10-2 | -12, 6 | 1, 19 | 7, 90*10-2 | |||
| 5, 75 | 3, 01 | 6, 85*10-2 | -13, 1 | 0, 96 | 8, 18E-02 | ||||
| 3, 58 | 6, 75*10-2 | -15, 2 |
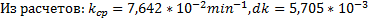
Из графика: 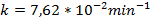
Ответ: 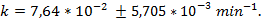
|
|
|
© helpiks.su При использовании или копировании материалов прямая ссылка на сайт обязательна.
|