| №
| Название формулы
| Формула
| Расшифровка обозначений
|
|
| Относительная молекулярная (атомная) масса
| 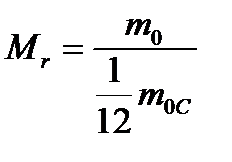
| Mr- относительная молекулярная (атомная) масса
m0 - масса молекулы (атома)
m0C – масса атома углерода
|
|
| Физический смысл числа Авогадро
| NA = 6·1023 моль-1
| Число молекул (атомов) в 1 моль любого вещества
|
|
| Количество вещества ν
| 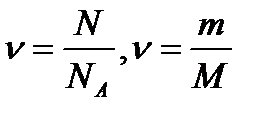
| ν – количество вещества, N – число молекул (атомов),
m – масса любого количества вещества (кг),
M – молярная масса вещества (кг/ моль)
|
|
| Молярная масса вещества M
| 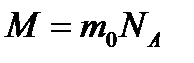
| m0 - масса молекулы (атома)
NA – число Авогадро
|
|
| Масса любого количества вещества m
| 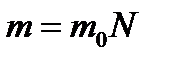
| m0 - масса молекулы, N – число молекул в теле
|
|
| Основное уравнение молекулярно-кинетической теории газа
| 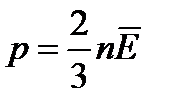
| 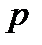 - давление идеального газа (Па) - давление идеального газа (Па)
 - концентрация молекул ( 1/м3 =м-3) - концентрация молекул ( 1/м3 =м-3)
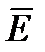 - Средняя кинетическая энергия молекулы (Дж) - Средняя кинетическая энергия молекулы (Дж)
|
|
| Плотность газа ρ
|  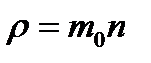
| ρ – плотность газа (кг/м3), m0 - масса молекулы
 - концентрация молекул (м-3) - концентрация молекул (м-3)
|
|
| Физический смысл постоянной Больцмана k
| k=1, 38·10-23 Дж/ К
| Постоянная Больцмана k связывает температуры в энергетических единицах (Дж) и в кельвинах (К)
|
|
| Зависимость давления идеального газа от концентрации молекул и температуры
| 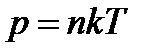
| 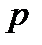 – давление газа (Па), – давление газа (Па),  - концентрация молекул (м-3)
k - постоянная Больцмана, T – температура газа (К) - концентрация молекул (м-3)
k - постоянная Больцмана, T – температура газа (К)
|
|
| Средняя квадратичная скорость молекулы 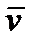
| 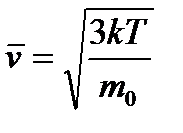
| k - постоянная Больцмана, k=1, 38·10-23 Дж/ К
T – температура газа (К)
m0 - масса молекулы (кг)
|
|
| Уравнение состояния идеального газа для любой массы газа (уравнение Клапейрона- Менделеева)
| 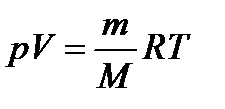
| R=8, 31 Дж/(моль·К) – универсальная газовая постоянная
R=kNA
|
|
| Уравнение состояния идеального газа для любой массы газа для постоянной массы газ (уравнение Клапейрона)
| 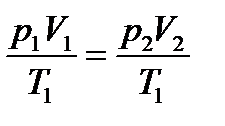 =... =...
|
|
|
| Изотермический процесс T=const
Закон Бойля-Мариотта
| 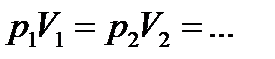
| Показать график в осях pV, pT, VT
|
|
| Изобарный процесс p=const
Закон Гей-Люссака
| 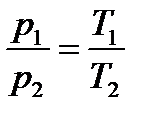
| Показать график в осях pV, pT, VT
|
|
| Изохорный процесс V=const
Закон Шарля
| 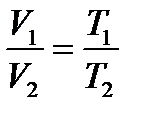
| Показать график в осях pV, pT, VT
|
|
| Зависимость давления насыщенного пара от температуры
|  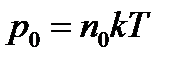
| 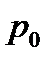 -давление насыщенного пара (Па) -давление насыщенного пара (Па)
|
|
| Относительная влажность воздуха
| 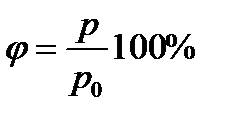
| 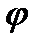 - относительная влажность, % - относительная влажность, %
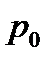 - давление насыщенного пара (Па) - давление насыщенного пара (Па)
|
|
| Внутренняя энергия идеального одноатомного газа
| 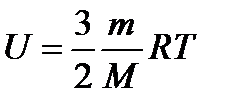
| U –внутренняя энергия газа (Дж)
|
|
| Работа в термодинамике, совершаемая внешними телами
| 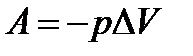
| При сжатии газа, когда 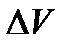 отрицательна, работа внешних сил положительна, внутр. энергия увеличивается отрицательна, работа внешних сил положительна, внутр. энергия увеличивается
|
|
| Работа в термодинамике, совершаемая самим газом
| 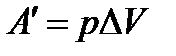 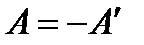
| Если сам газ совершает работу, внутренняя
энергия U газа уменьшается.
|
|
| Первый закон термодинамики
|  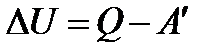
| 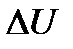 - изменение внутренней энергии (Дж), A – работа внешних сил (Дж), Q –кол-во теплоты, переданная телу (Дж) - изменение внутренней энергии (Дж), A – работа внешних сил (Дж), Q –кол-во теплоты, переданная телу (Дж)
|
|
| КПД теплового двигателя 
| 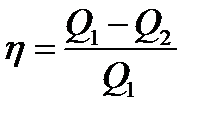
| 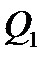 - количество теплоты, полученное от нагревателя, - количество теплоты, полученное от нагревателя, 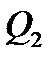 - количество теплоты, переданная холодильнику, - количество теплоты, переданная холодильнику, 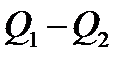 - полезная работа - полезная работа
|
|
| Максимальный КПД идеальной тепловой машины (машины Карно)
| 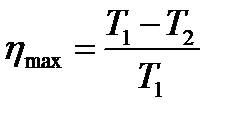
| 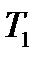 - температура нагревателя, - температура нагревателя,  - температура холодильника, - температура холодильника,  - полезная работа - полезная работа
|

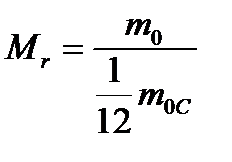
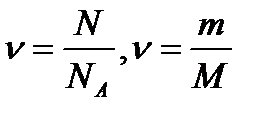
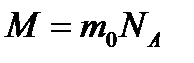
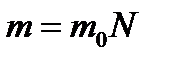
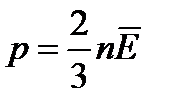
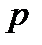 - давление идеального газа (Па)
- давление идеального газа (Па)
 - концентрация молекул ( 1/м3 =м-3)
- концентрация молекул ( 1/м3 =м-3)
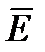 - Средняя кинетическая энергия молекулы (Дж)
- Средняя кинетическая энергия молекулы (Дж)

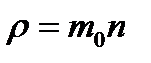
 - концентрация молекул (м-3)
- концентрация молекул (м-3)
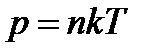
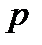 – давление газа (Па),
– давление газа (Па),  - концентрация молекул (м-3)
k - постоянная Больцмана, T – температура газа (К)
- концентрация молекул (м-3)
k - постоянная Больцмана, T – температура газа (К)
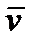
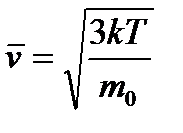
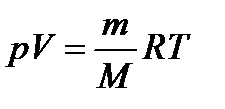
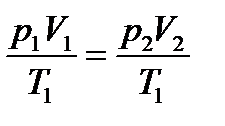 =...
=...
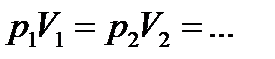
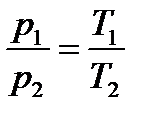
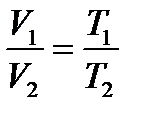

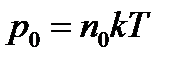
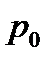 -давление насыщенного пара (Па)
-давление насыщенного пара (Па)
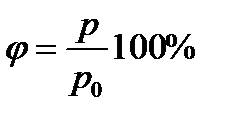
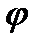 - относительная влажность, %
- относительная влажность, %
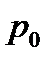 - давление насыщенного пара (Па)
- давление насыщенного пара (Па)
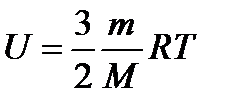
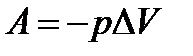
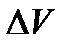 отрицательна, работа внешних сил положительна, внутр. энергия увеличивается
отрицательна, работа внешних сил положительна, внутр. энергия увеличивается
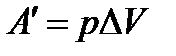
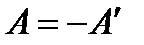

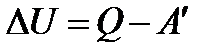
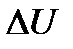 - изменение внутренней энергии (Дж), A – работа внешних сил (Дж), Q –кол-во теплоты, переданная телу (Дж)
- изменение внутренней энергии (Дж), A – работа внешних сил (Дж), Q –кол-во теплоты, переданная телу (Дж)

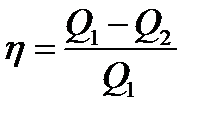
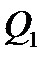 - количество теплоты, полученное от нагревателя,
- количество теплоты, полученное от нагревателя, 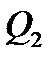 - количество теплоты, переданная холодильнику,
- количество теплоты, переданная холодильнику, 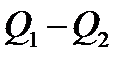 - полезная работа
- полезная работа
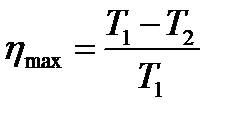
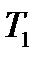 - температура нагревателя,
- температура нагревателя,  - температура холодильника,
- температура холодильника,  - полезная работа
- полезная работа