
- Автоматизация
- Антропология
- Археология
- Архитектура
- Биология
- Ботаника
- Бухгалтерия
- Военная наука
- Генетика
- География
- Геология
- Демография
- Деревообработка
- Журналистика
- Зоология
- Изобретательство
- Информатика
- Искусство
- История
- Кинематография
- Компьютеризация
- Косметика
- Кулинария
- Культура
- Лексикология
- Лингвистика
- Литература
- Логика
- Маркетинг
- Математика
- Материаловедение
- Медицина
- Менеджмент
- Металлургия
- Метрология
- Механика
- Музыка
- Науковедение
- Образование
- Охрана Труда
- Педагогика
- Полиграфия
- Политология
- Право
- Предпринимательство
- Приборостроение
- Программирование
- Производство
- Промышленность
- Психология
- Радиосвязь
- Религия
- Риторика
- Социология
- Спорт
- Стандартизация
- Статистика
- Строительство
- Технологии
- Торговля
- Транспорт
- Фармакология
- Физика
- Физиология
- Философия
- Финансы
- Химия
- Хозяйство
- Черчение
- Экология
- Экономика
- Электроника
- Электротехника
- Энергетика
Тема урока: Скорость химических реакций
Тема урока: " Скорость химических реакций"
Одни реакции протекают практически мгновенно (между растворами):
ВаСl2 + H2SO4 = BaSO4↓ + 2HCl
Некоторые реакции протекают в течение определенного периода времени (2 - 3ч. ):
4Fe + 3O2 + 6H2O = 4Fe(OH)3 (ржавчина)
Некоторые реакции протекают в течение многих лет. Например, образование антрацита (уголь) в земной коре протекает в течение сотен и тысяч лет.
Что же такое скорость химических реакций и как она определяется и изменяется?
Скорость реакции определяется изменением концентрации прореагировавшего или образующегося вещества в единицу времени.
Концентрация вещества часто определяется числом молей в литре.
Допустим, что начальная концентрация SO2 в реакции окисления его до SO3 была 2 моль/л, а через 50 с стала 0, 5 моль/л. В этом случае скорость данной реакции ( υ )равна:
υ = 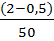 =
= 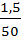 = 0, 03 моль/л∙ с
= 0, 03 моль/л∙ с
Это означает, что в каждую секунду в 1 л газовой смеси 0, 03 моль SO2 превращается в SO3.
Если первоначальную концентрацию вещества обозначить С1, а через некоторое время t - C2, то скорость реакции в общем виде можно выразить так:
υ = 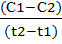 =
= 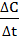 ,
,
где ∆ С = С1 - С2
∆ t = t2 - t1
Следовательно, скорость химической реакции определяется изменением концентрации одного из реагирующих веществ единицу времени.
Факторы, влияющие на скорость реакции:
1. Природа реагирующих веществ.
Под природой реагирующих веществ понимают их состав, строение, взаимное влияние атомов в неорганических и органических веществах.
Zn + CH3COOH (слабая кислота) υ 1
|
|
|
© helpiks.su При использовании или копировании материалов прямая ссылка на сайт обязательна.
|