
- Автоматизация
- Антропология
- Археология
- Архитектура
- Биология
- Ботаника
- Бухгалтерия
- Военная наука
- Генетика
- География
- Геология
- Демография
- Деревообработка
- Журналистика
- Зоология
- Изобретательство
- Информатика
- Искусство
- История
- Кинематография
- Компьютеризация
- Косметика
- Кулинария
- Культура
- Лексикология
- Лингвистика
- Литература
- Логика
- Маркетинг
- Математика
- Материаловедение
- Медицина
- Менеджмент
- Металлургия
- Метрология
- Механика
- Музыка
- Науковедение
- Образование
- Охрана Труда
- Педагогика
- Полиграфия
- Политология
- Право
- Предпринимательство
- Приборостроение
- Программирование
- Производство
- Промышленность
- Психология
- Радиосвязь
- Религия
- Риторика
- Социология
- Спорт
- Стандартизация
- Статистика
- Строительство
- Технологии
- Торговля
- Транспорт
- Фармакология
- Физика
- Физиология
- Философия
- Финансы
- Химия
- Хозяйство
- Черчение
- Экология
- Экономика
- Электроника
- Электротехника
- Энергетика
№1. Экзамен (Алиева Алсу)
Химическая антисептика. Основные группы антисептических средств. Способы использования различных химических веществ. Различные виды местного и общего применения антисептиков.
Химическая антисептика - уничтожение микроорганизмов в патологическом очаге или организме больного с помощью различных химических веществ.
Классификации антисептиков.
Дезинфицирующие средства используются для обработки инструментов, мытья стен, полов, обработки предметов ухода и пр.
Антисептические вещества применяются наружно для обработки кожи, рук хирурга, промывания ран и слизистых оболочек.
Химиотерапевтические средства вводятся внутрь и оказывают резорбтивное действие в организме больного, подавляя рост бактерий в различных патологических очагах.
Основные группы химических антисептиков.
Группа галоидов.
Йод - 1-5 % спиртовая настойка. Антисептическое средство наружного применения. Используется для обработки кожи вокруг раны при перевязке, для обработки ссадин; царапин, поверхностных ран. Обладает выраженным дубящим действием.
Йодинол— 1 % раствор, «синий йод». Антисептическое средство наружного применения. Используется для промывания ран, полоскания зева.
Йодонат и йодопирон — органические соединения йода. Используют 1 % раствор. Антисептические средства наружного применения. Используются для обработки операционного поля.
Повидон-йодин — органическое соединение йода О, 1—1 % свободного йода). Антисептическое средство наружного применения. Используется для обработки кожи при перевязках и операции, а также обработки ран (аэрозоль).
Раствор Люголя — содержит йод и йодид калия, может использоваться водный и спиртовой раствор. Препарат комбинированного действия. Как дезинфицирующее средство используется для стерилизации кетгута. Как химиотерапевтическое средство — для лечения заболеваний щитовидной железы.
Хлорамин Б — 1-3 % водный раствор. Дезинфицирующее средство. Используется для дезинфекции предметов ухода, резиновых инструментов, помещений.
Соли тяжелых металлов.
Сулема — в концентрации 1: 1000 для дезинфекции перчаток, предметов ухода, как этап в стерилизации шелка. В настоящее время в связи с токсичностью практически не применяется.
Оксицианид ртути — дезинфицирующее средство. В концентрации 1: 10000, 1: 50000 применяют для стерилизации оптических инструментов.
Нитрат серебра — антисептическое средство наружного применения. В виде 0, 1-2 % растворов используется для промывания конъюнктивы, слизистых оболочек. 5-20 % растворы обладают выраженным прижигающим действием и используются для обработки избыточных грануляций, ускорения рубцевания пупка у новорожденных и пр.
Протаргол, колларгол — антисептические средства наружного применения, обладают вяжущим действием. Используются для смазывания слизистых оболочек, промывания мочевого пузыря при наличии воспалительного процесса.
Оксид цинка — антисептическое средство наружного применения. Входит в состав-многих присыпок и паст, обладающих противовоспалительным эффектом, предотвращает развитие мацерации кожи.
Спирты.
Этиловый спирт — используется в качестве дезинфицирующего средства (стерилизация шовного материала, обработка инструментов) и как антисептическое средство наружного применения (обработка рук хирурга и операционного поля, краев раны при перевязках, для компрессов и пр. ). 70 ° спирт обладает антисептическим действием, а 96 ° — еще и дубящим. В настоящее время широкое применение для обработки рук хирурга и хирургических инструментов нашли препараты АХД-2000Х активные вещества этанол и эфир полиольной жирной кислоты) и АХД-2000-специаль (в состав дополнительно входит хлоргексидин).
Альдегиды.
Формалин — 37 % раствор формальдегида. Сильное дезинфицирующее средство. 0, 5-5 % растворы используются для дезинфекции перчаток, дренажей, инструментов. Эффективен против эхинококка. Применяется также при фиксации препаратов для гистологического исследования. В сухом виде применяется для стерилизации в газовых стерилизаторах, в частности, оптических инструментов.
Лизол — сильное дезинфицирующее средство. 2 % раствор используется для дезинфекции предметов ухода, помещений, замачивания загрязненных инструментов. В настоящее время практически не применяется из-за высокой токсичности.
Фенолы.
Карболовая кислота — сильное дезинфицирующее средство. 2-3 % раствор в прошлом использовали для дезинфекции перчаток, предметов ухода. Сейчас применяется только в комплексе с другими препаратами (входит в состав присыпок, мазей).
Тройной раствор — содержит 20 г формалина, 10 г карболовой кислоты, 30 г соды и дистиллированную воду (до 1 литра). Сильное дезинфицирующее средство. Используют для обработки инструментов, предметов ухода, холодной стерилизации режущих инструментов.
Красители.
Бриллиантовый зеленый — антисептическое средство наружного применения. 1-2 % спиртовой (или водный) раствор используется для обработки поверхностных ран и ссадин слизистой полости рта и кожи.
Метиленовый синий — антисептическое средство наружного применения. 1-2 % спиртовой (или водный) раствор используется для обработки поверхностных ран и ссадин слизистой полости рта и кожи. 0, 02 % водный раствор — для промывания ран.
Кислоты.
Борная кислота — антисептическое средство наружного применения. 2-4 % раствор ее — один из основных препаратов для промывания и лечения гнойных ран. Можно использовать в виде порошка, входит в состав присыпок и мазей.
Салициловая кислота — антисептическое средство наружного применения. Обладает кератолитическим действием. Применяют в виде кристаллов (для лизиса тканей), входит в состав присыпок, мазей.
Щелочи.
Нашатырный спирт — антисептическое средство наружного применения. Раньше 0, 5 % раствор широко использовался для обработки рук хирурга (метод Спасокукоцкого —Кочергина).
Окислители.
Перекись водорода — антисептическое средство наружного применения. 3 % раствор —. основной препарат для промывания гнойных ран при перевязках. Основные свойства: антисептик (активный агент — атомарный кислород); гемостатик (способствует остановке кровотечения); дезодорант; вызывает пенообразование, улучшающее очищение раны. Входит в состав первомура (средство для обработки рук хирурга и операционного поля). 6% раствор перекиси водорода является важным дезинфицирующим веществом.
Перманганат калия — антисептическое средство наружного применения. 2-5 % раствор используется для лечения ожогов и пролежней (обладает коагулирующим и дубящим действием). 0, 02 %-0, 1 % раствором промывают раны и слизистые оболочки. Имеет выраженный дезодорирующий эффект.
Детергенты (поверхностно-активные вещества).
Хлоргексидина биглюконат — антисептическое средство наружного применения. 0, 5 % спиртовой раствор используется для обработки рук хирурга и операционного поля. 0, 1-0, 2 % водный раствор — один из основных препаратов для промывания ран и слизистых оболочек, лечения гнойных ран. Входит в состав растворов для обработки рук и операционного поля (Пливасепт, АХД-специаль).
Церигель — антисептическое средство наружного применения. Используется для обработки рук (пленкообразующий антисептик).
Дегмин, дегмицид — антисептические средства наружного применения. Используются для обработки рук и операционного поля.
«Астра», «Новость» — компоненты моющих растворов для дезинфекции инструментов.
Производные нитрофурана.
Фурацилин — антисептическое средство наружного применения. Раствор 1: 5000 — один из основных препаратов для лечения гнойных ран, промывания ран и слизистых оболочек.
Лифузоль — содержит фурацилин, линетол, смолы, ацетон (аэрозоль). Антисептическое средство наружного применения. Наносится в виде пленки. Применяется для защиты послеоперационных ран и дренажных отверстий от экзогенной инфекции, а также для лечения поверхностных ран.
Фурадонин, фурагин, фуразолидон — химиотерапевтические средства, так называемые «уроантисептики». Кроме инфекции мочевыводящих путей используются при лечении кишечных инфекций.
Производные 8-оксихинолина.
Нитроксолин (5-НОК) — химиотерапевтическое средство, «уроантисеп-тик». Применяется при инфекции мочевыводящих путей.
Энтеросептол, интестопан — химиотерапевтические средства, применяемые при кишечных инфекциях.
Производные хиноксалина.
Диоксидин — антисептическое средство наружного применения. 0, 1-1 % водный раствор используется при промывании гнойных ран и слизистых оболочек, особенно при неэффективности антибиотиков и других антисептиков. При сепсисе и тяжелых инфекциях может вводиться и внутривенно капельно.
Производные нитроимидазола.
Метронидозол (метрагил, флагил, трихопол) — химиотерапевтическое средство широкого спектра действия. Эффективен в отношении простейших, бактероидов и ряда анаэробов.
Дегти, смолы.
Деготь березовый — антисептическое средство наружного применения. Входит как компонент в состав мази Вишневского, используемой при лечении гнойных ран (кроме антисептического действия стимулирует рост грануляций).
Ихтиол, нафталан — используются в виде мазей, обладают противовоспалительным действием.
Антисептики растительного происхождения.
Хлорофиллипт, эктерицид, бализ, календула — в основном применяются как антисептические средства наружного применения для промывания поверхностных ран, слизистых оболочек, обработки кожи. Обладают противовоспалительным эффектом.
Сульфаниламидные препараты — химиотерапевтические средства, оказывающие бактериостатическое действие. Используются для подавления различных очагов инфекции в организме, обычно — таблетированные препараты. Входят также в состав мазей и присыпок для наружного применения. Таблетированные препараты имеют различный срок действия: от 6 часов до 1 суток.
Стрептоцид, этазол, сульфадимезин — короткого действия.
Сульфазин — среднего срока действия.
Сульфадиметоксин — длительного действия.
Сулъфален — сверхдлительного действия.
Бисептол (бактрим) — комбинированный препарат, в состав которого входят сульфаниламид, сульфаметоксазол и производное диаминопири-мидина — триметоприм. Является весьма распространенным лекарственным средством при лечении различных воспалительных процессов в организме.
Биологическая антисептика. Виды биологической антисептики. Основные фармакологические препараты и методы их применения. Пассивная и активная иммунизация в хирургии. Иммунокоррекция и иммуностимуляция.
Виды биологической антисептики:
• биологическая антисептика прямого действия — использование фармакологических препаратов биологического происхождения, непосредственно воздействующих на микроорганизмы;
• биологическая антисептика опосредованного действия — использование фармакологических препаратов и методов различного происхождения, стимулирующих способности макроорганизма в борьбе с микроорганизмами.
Основные фармакологические препараты и методы.
Фармакологические препараты прямого действия на микроорганизмы:
Антибиотики.
Протеолитические ферменты: трипсин, химотрипсин, химопсин, террилитин, ируксол.
Препараты для пассивной иммунизации: лечебные сыворотки, антитоксины, Y-глобулины, бактериофаги, гипериммунная плазма.
Фармакологические препараты и методы для опосредованного действия на микроорганизмы:
Методы, стимулирующие неспецифическую резистентность: кварцевание, витаминотерапия, УФО крови, лазерное облучение крови, использование перфузата и клеток ксеноселезенки, переливание крови и ее компонентов.
Препараты, стимулирующие неспецифический иммунитет: препараты вилочковой железы (тималин, Т-активин), продигиозан, левамизол, лизоцим, интерфероны, интерлейкины.
Препараты, стимулирующие специфический иммунитет: вакцины, анатоксины.
Антибиотики — вещества, являющиеся продуктом, жизнедеятельности микроорганизмов, подавляющие рост и развитие определенных групп других микроорганизмов.
Основные группы антибиотиков.
Пенициллины (ингибируют синтез клеточной стенки микроорганизма (МО); в основном — широкий спектр действия):
пенициллин (натриевая и калиевая соль бензилпенициллина);
полусинтетические: оксациллин, метициллин, ампициллин, амоксициллин;
пролонгированные: бициллин, бициллин-3, бициллин-5;
комбинированные: ампиокс (ампициллин + оксациллин), аугментин (амоксициллин + калиевая соль клавулоновой кислоты), уназин (ампициллин + сульбактам).
Клавулонат калия и сульбактам — ингибиторы пенициллиназы, вырабатываемой микроорганизмами.
Стрептомицины (подавляют функцию рибосом МО; широкий спектр; ото-, нефро-, гепатотоксичны, угнетают гемопоэз): стрептомицин.
Тетрациклины (подавляют функцию рибосом МО; широкий спектр) тетрациклин;
Макролиды (нарушают синтез белка в МО; гепатотоксичны, возможно нарушение функции желудочно-кишечного тракта): эритромицин, олеандомицин, рокситромицин, азитромицин, кларитромицин.
Аминогликозиды (нарушают синтез клеточной синтез МО; широкий спектр; ото- и нефротоксичны): канамицин, гентамицин, тобрамицин, сизомицин; полусинтетические: амикацин, нетромицин.
Левомицетины (нарушают синтез белка в МО; широкий спектр; угнетают гемопоэз): левомицетин.
Рифампицины (нарушают синтез белка в МО; широкий спектр; вызывают гиперкоагуляцию, гепатотоксичны): рифампицин
Противогрибковые антибиотики: леворин, нистатин.
Полипептиды: нарушают функции клеточных мембран, нефротоксичны
Полимиксин В (воздействует на грамотрицательные МО, в том числе на палочку сине-зеленого гноя).
Линкозамины (нарушают синтез белка в МО): линкомицин, клиндамицин.
Цефалоспорины (нарушают синтез клеточной стенки МО; широкий спектр; нефротоксичны в высоких дозах).
Карбапенемы (нарушают синтез клеточной стенки МО; широкий спектр): имипенем, меропенем.
Комбинированный препарат тиенам (имипенем + циластатин); циластатин — ингибитор фермента, влияющего на метаболизм антибиотика в почках.
Гликопептиды (изменяют проницаемость и нарушают синтез клеточной стенки МО, широкий спектр, ото- и нефротоксичны): ванкомицин, эримомицин.
Кроме представленной классификации по группам антибиотики разделяются на препараты широкого и узкого спектра действия.
№2.
Гнойная хирургическая инфекция.
Термин infectio («заражаю») впервые был введён в 1841 году Гуфеландом. Инфекция в хирургии определяет сущность многих заболеваний и послеоперационных осложнений.
Инфекция – внедрение и размножения микроорганизмов в макроорганизме с последующим развитием сложного комплекса их взаимодействия от носительства возбудителя до выраженной болезни.
Термин «хирургическая инфекция» подразумевает два вида процессов:
Инфекционный процесс, при лечении которого хирургическое вмешательство имеет решающее значение.
Инфекционные осложнения, развивающиеся в послеоперационном периоде.
Патологические гнойно-воспалительные процессы включают следующие группы:
Гнойные заболевания.
Гнойно-деструктивные процессы при острых хирургических заболеваниях.
Гнойные послеоперационные осложнения.
Гнойные осложнения открытой и закрытой травмы.
+Факторами, определяющими начало развития, особенности течения и исход заболеваний, связанных с инфекцией в хирургии, являются: состояние иммунологических сил организма; количество, вирулентность, лекарственная устойчивость и другие биологические свойства микробов, проникших во внутреннюю среду организма человека; анатомо-физиологические особенности очага внедрения микрофлоры; состояние общего кровообращения; степень аллергизации больного.
Классификация хирургической инфекции:
По клиническому течению выделяют:
Острая хирургическая инфекция
а) гнойная
б) гнилостная
в) анаэробная
г) специфическая (столбняк, сибирская язва и др. )
Хроническая хирургическая инфекция
а) неспецифическая
б) специфическая (туберкулёз, сифилис и др. )
По этиологии:
1. стафилококковая инфекция
2. стрептококковая инфекция
3. пневмококковая инфекция
4. колибациллярная инфекция
5. гонококковая инфекция
6. анаэробная неспорообразующая инфекция
7. клостридиальная анаэробная инфекция
8. смешанная инфекция
По клиническому течению:
1. местная
2. генерализованная
Патогенез.
Острая гнойная инфекция – это острый воспалительный процесс различной локализации и характера, вызванный гноеродной микрофлорой. Для ее развития необходимо наличие трех элементов:
1)Возбудитель инфекции (гноеродный микроорганизм);
2)Входные ворота инфекции (место и способ внедрения 3)микроорганизма в ткани больного);
4)Макроорганизм с его реакциями – местными и общими, защитными и патологическими.
5)Возбудители гнойной хирургической инфекции.
Современная характеристика возбудителей гнойной хирургической инфекции значительно отличается от классических схем, сформулированных несколько десятилетий тому назад. В настоящее время основными возбудителями являются: золотистый стафилококк, синегнойная палочка, кишечная палочка, энтерококки, стрептококки, протей, пневмококки. Вследствие широкого применения антибиотиков и их мутагенного действия эти микроорганизмы, как правило, характеризуются устойчивостью к большинству антимикробных средств. Лекарственная устойчивость стафилококков, выделенных у больных гнойной инфекцией, превышает 70%. Такая же устойчивость наблюдается у палочки сине-зеленого гноя, чем объясняется ее возрастающая роль при осложнении ожогов и ран.
+Важную роль в лечении гнойной хирургической инфекции играют биологические особенности микроорганизмов: инвазивность, токсичность и вирулентность. Кроме того, существенное значение имеет степень инфицированности. Проникновение менее чем 105 бактерий на 1 г ткани, как правило, оказывается недостаточными для развития инфекции (надежно срабатывают факторы защиты).
Входными воротами наиболее часто являются повреждения кожи и слизистых оболочек – различные виды случайных ран. Проникновение инфекции возможно и через ссадины, царапины, потёртости, укусы. Кроме того, организмы могут проникать через протоки сальных и потовых желез. Быстрому распространению микроорганизмов способствуют большое количество некротических тканей в области входных ворот, нарушение кровообращения, охлаждение.
К неспецифическим механизмам защиты можно отнести анатомические барьеры (кожа и слизистые), наличие нормальной микрофлоры, проявляющей антагонизм по отношению к экзогенным микроорганизмам, гуморальные факторы защиты (лейкины, плакины, лизины, лизоцим, система комплимента), клеточные механизмы, представленные воспалительной реакцией и фагоцитозом.
Воспаление складывается из следующих последовательно развивающихся фаз: 1) альтерация; 2) экссудация; 3) пролиферация.
Альтерация – повреждение ткани, является инициальной фазой воспаления, определяющей кинетику воспалительной реакции. В эту фазу происходит выброс биологически активных веществ – медиаторов воспаления, которые могут быть плазменного (кинины, плазмин, система комплимента и др. ) и клеточного (гистамин, серотонин, простагландины, лизосомные ферменты и др. ) происхождения. Медиаторы плазменного и клеточного происхождения взаимосвязаны и работают по принципу аутокаталитической реакции с обратной связью и взаимной поддержкой.
Экссудация – фаза, быстро следующая за альтерацией и выбросом медиаторов. Она складывается из ряда стадий: реакция микроциркуляторного русла с нарушением реологических свойств крови; повышение сосудистой проницаемости на уровне микроциркуляторного русла; экссудация составных частей плазмы крови; эмиграция клеток крови; фагоцитоз; образование экссудата и воспалительного клеточного инфильтрата. Воспалительная гиперемия обуславливает повышение температуры (calor) и покраснение(rubor) воспаленного участка. Накопление в ткани экссудата ведет к увеличению ее объема (tumor), сдавлению нервных окончаний и появлению боли (dolor), возникновение которой при воспалении связывают также с воздействием медиаторов и нарушением функции ткани или органа (funcio laesa).
Пролиферация клеток– является завершающей фазой воспаления, направленной на восстановление поврежденных тканей. Возрастает число мезенхимальных камбиальных клеток, В и Т лимфоцитов, моноцитов.
Для гнойного воспаления характерно преобладание в экссудате нейтрофилов. Распадающиеся нейтрофилы, которых называют гнойными тельцами, вместе с жидкой частью экссудата образуют гной. В нем встречаются также лимфоциты, макрофаги, погибшие клетки ткани, микробы. Гнойное воспаление в зависимости от распространенности его может быть представлено абсцессом или флегмоной.
Абсцесс – очаговое гнойное воспаление с образованием полости, заполненной гноем. Гнойники со временем отграничиваются валом грануляционной ткани, богатой капиллярами, через стенки которых происходит усиленная эмиграция лейкоцитов. Образуется как бы оболочка абсцесса. Снаружи она состоит из соединительно тканых волокон, которые предлежат к неизменённой ткани, а внутри из грануляционной ткани и гноя, непрерывно обновляющегося благодаря выделению грануляциями гнойных телец. Оболочку абсцесса, продуцирующего гной, называют пиогенной мембраной.
+Флегмона – разлитое гнойное воспаление, при котором гнойный экссудат распространяется диффузно между тканевыми элементами, пронизывая, расслаивая и лизируя ткани. Чаще всего флегмона наблюдается там, где гнойный экссудат может легко пробить себе дорогу, т. е. по межмышечным прослойкам, по ходу сухожилий, фасций, в подкожной клетчатке, вдоль сосудисто-нервных стволов.
Специфически механизмы защиты включают в себя иммунный ответ гуморального и клеточного типа.
В зависимости от реакции макроорганизма выделяют гипоергическую, нормергическую и гиререргическую формы воспалительной реакции.
Факторами снижения защитных сил организма является пожилой возраст, также сопутствующие заболевания, такие как сахарный диабет, иммунодефицитные состояния, авитаминоз и др.
Клиническая картина и диагностика.
Клиническая картина гнойно-воспалительный заболеваний складывается из местных и общих симптомов. Местные проявления определяются стадией развития, характером и локализацией воспалительного процесса. К таким признакам воспаления как краснота, припухлость, боль, повышением местной температуры и нарушение функций органа, могут присоединиться формирование некрозов, воспаление лимфатических сосудов (лимфангит) и узлов (лимфаденит), тромбофлебит.
Клинически в очаге воспаления можно выявить пальпаторно размягчение инфильтрата и симптом флюктуации.
Клиническими признаками общей реакции организма на воспаление являются повышение температуры тела, озноб, вялость, головная боль, общее недомогание, плохой аппетит, тахикардия, признаки нарушения функции печени, почек, снижение артериального давления.
Перечисленные симптомы могут носить ярко выраженный характер.
Характерным является изменение температуры в течении суток более чем на 1, 5 – 2° С – температура утром нормальная или субфибрильная, а вечером достигает высокого уровня (до 39-40° С).
Для всех гнойных хирургических заболеваний характерно наличие лейкоцитоза, сдвига лейкоциторной формулы влево, повышение СОЭ. При этом отмечается относительное снижение количества лимфоцитов и моноцитов. При тяжелых длительных гнойных процессах отмечается анемия.
+В биохимическом анализе может отмечаться повышение азотных показателей (креатинин, мочевина), В сложных случаях определяются белки острой фазы (С – реактивный белок, церупоплазмин, гаптоглобин и др. ), отмечается изменение в составе, белковых фракций (относительное увеличение количества глобулинов).
В анализах мочи в тяжёлых случаях отмечают протеинурию, цилиндрарию, иногда лейкоцитрию.
Для определения уровня интоксикации и динамического наблюдения за больными с острой гнойной хирургической инфекцией используют интегральные показатели: лейкоциторный индекс и гематологический показатель интоксикации.
Общие принципы лечения.
Лечение больных с гнойной хирургической инфекцией, особенно при её выраженных и осложнённых формах, представляет собой трудную задачу и включает комплекс мероприятий, цель которых воздействие как на организм больного, так и на возбудителей заболевания. Среди основных задач в лечении можно определить следующее: 1)своевременное адекватное выполнение хирургической операции; 2) целенаправленная антибактериальная терапия; 3) эффективная дезинтоксикационная терапия; 4) иммунокорригирующая и стимулирующая терапия; 5) восстановление нарушенных функций органов и систем.
В первой фазе (инфильтрация) задачей лечения является скорейшее отграничение воспалительного очага, уменьшение интоксикации и ослабление болевой реакции, по возможности разрешение воспалительного процесса в стадии серозного и инфильтративного пропитывания без перехода в деструктивную фазу.
Во второй фазе (абсцедирования) важнейшей задачей является скорейшее опорожнение гнойника, обеспечение беспрепятственного оттока экссудата, уменьшение всасывания продуктов распада и токсинов из гнойного очага, отграничение и скорейшее отторжение некротизированной ткани, очищение зоны воспаления от продуктов экссудации и нежизнеспособных тканей.
Консервативное лечение.
Хирургическая операция при гнойных заболеваниях является основным методом лечения. Однако успех в лечении больных возможен лишь при комплексной терапии, предусматривающей использование антибактериальных, иммунных препаратов, детоксикационных средств и методов симптоматического лечения.
Антибактериальная терапия. Для местной антибактериальной терапии – санация полостей, гнойных ран, используют химические антибактериальные препараты – производные нитрофуранов, хиноксолина и др.
+ лечение начинают с антибиотиков широкого спектра действия, а после установления возбудителя назначают антибиотики, к которым чувствителен выделенный возбудитель. При микробных ассоциациях показана комбинированная антибактериальная терапия, при этом наилучший вариант достигается в случае применения препаратов, обладающих синергичным действием, а микрофлора должна быть чувствительная ко всем антибиотикам, входящим в данную комбинацию. Применение антибиотика должно учитывать противопоказания к их назначению. Перед назначением антибиотика следует учитывать анамнестические данные о переносимости антибиотиков в прошлом, наличие аллергических заболеваний. Длительность лечения антибиотиком определяется стиханием воспалительных явлений, нормализацией температуры тела. В острых случаях продолжительность лечения составляет 6-8 дней, при необходимости продолжать лечение производят смену препарата. Существует поверхностная антибиотикотерапия (промывание ран), внутриполостная (введение в грудную, брюшную полость, в полость сустава) и глубокая антибиотикотерапия: внутримышечное, внутривенное, внутриартериальное и эндолимфатическое введение, а также пероральный способ.
В настоящее время существует два вида эндолимфатической терапии:
Прямая – введение препаратов непосредственно в лимфатические сосуды и узлы:
а) антеградная;
б) ретроградная.
Непрямая лимфатропная терапия – введение препаратов в различные клетчаточные пространства с последующей преимущественной резорбцией в лимфатическую систему.
Преимуществами эндолимфатической терапии являются:
Метод позволяет создать высокую длительную концентрацию антибиотика в лимфатические сосуды и центральной лимфы
Обеспечивает более длительную концентрацию в регионарных лимфатических узлах.
При разовом эндолимфатическом введении антибиотика его бактерицидная концентрация сохраняет в плазме в лечении 24-х часов.
Достижение максимальной локализации антибиотика в очаге воспаления.
Меньшая кратность и доза введения антибиотика.
Иммуномоделирующее действие.
Детоксикационная терапия. Дезинтоксикационная терапия может проводиться различными способами, что определяется характером и тяжестью интоксикации. . Как иммуностимулирующие средства при иммунодефицитных состояниях с поражением Т–системы иммунитета применяют препараты вилочковой железы (тималин, тактивин). Иммуностимулирующим действием обладают интерферрон, продигкиозан, левамизол. Для создания специфического антитоксического иммунитета применяют анатоксины – стафилококковый, столбнячный.
Симптоматическое лечение. Оно направлено на восстановление нарушенных функций органов и систем. Необходимым бывает применение жаропонижающих и противовоспалительных препаратов.
Хирургическое лечение.
Хирургическая операция – вскрытие гнойника – обычно выполняется под проводниковой или общей анестезией, (инфильтрационная анестезия используется редко так как может способствовать распространению инфекции, эффективность действия анестетиков в воспалительном очаге снижается).
Разрез производят на всю длину воспалительного инфильтрата. После вскрытия очага определяют наличие гнойных затеков и дополнительно вскрывают их, разделяют перемычки, определяют состояние соседних органов, явившихся причиной или вовлеченных вторично в гнойный процесс. Осмотр гнойной полости не всегда возможен. В таких случаях обязательным является обследование полости пальцем.
Операция при гнойном воспалении может заключаться в полном удалении гнойного очага (иссечении абсцесса небольших размеров в пределах здоровых тканей при гнойном мастите, абсцессе подкожной клетчатки и др. ).
Важным элементом интраоперационной санации является использование химических антисептиков для обильного промывания гнойной полоски, образовавшейся при воспалении. Полость промывают раствором одного из антисептиков (перекись водорода, фурацилин, хлоргексидин),
Всегда целесообразно проводить взятие на посев содержимое гнойного экссудата, для его бактериологического исследования и определения чувствительности к антибиотикам, что позволяет выбрать оптимальный вариант антибактериальной терапии.
+Любая операция по вскрытию гнойника завершается его дренированием. Для адекватного дренирования применяются всевозможные способы, относящиеся к физической антисептике: пассивное дренирование (используются тампоны, перчаточная резина, дренажные трубки), активная аспирация и проточное дренирование. Дренажи должны проходить в нижней точке гнойной полости с учетом положения больного в постели на спине. Дренажные материалы должны удовлетворять определенным требованиям: они не должны оказывать значительного механического раздражающего действия на ткани, быть биологически интактными, как можно дольше сохранять функциональные (дренажные) свойства. Трубки, рассеченные по длине желоба, резиновые полоски и т. п., не в состоянии обеспечить полноценное дренирование, поэтому их можно применять только для предотвращения слипания краев раны, например, после вскрытия сухожильного влагалища при панариции и т. д.
Местные проявления
Местные проявления воспаления определяются стадией развития, характером и локализацией воспалительного процесса. Так, поверхностно расположенные очаги воспаления (гнойно-воспалительные заболевания кожи, подкожной клетчатки молочной железы, мышц и др. ) или расположенные в глубине тканей очаги, но с вовлечением в воспалительный процесс кожных покровов, характеризуются классическими признаками воспаления - покраснением(rubor), обусловленным воспалительной гиперемией, отёком, припухлостью(tumor), болью(dolor), повышением местной температуры(calor) и нарушением функций органа(functio laesa). Распространённость и выраженность воспалительного процесса определяют и степень выраженности местных клинических проявлений. При воспалительном процессе во внутренних органах отмечаются характерные для каждого заболевания местные признаки (например, при гнойном плеврите, перитоните).
При клиническом обследовании больных с гнойно-воспалительными заболеваниями можно определить фазу воспалительного процесса: пальпируемое плотное болезненное образование при наличии других признаков воспаления свидетельствует об инфильтративной фазе процесса в мягких тканях и железистых органах, коже и подкожной клетчатке, молочной железе, брюшной полости. Определяемое при пальпации размягчение инфильтрата, положительный симптом флюктуации указывают на переход инфильтративной фазы воспаления в гнойную.
Местными клиническими признаками прогрессирующего гнойного воспаления служат краснота в виде полос на коже (лимфангиит), плотные шнурообразные болезненные уплотнения по ходу поверхностных вен (тромбофлебит), появление плотных болезненных уплотнений в месте расположения регионарных лимфатических узлов (лимфаденит). Между выраженностью местных симптомов воспаления и общими клиническими признаками интоксикации имеется соответствие: прогрессирование воспалительного процесса проявляется нарастанием как местных, так и общих проявлений воспаления и интоксикации.
Общие проявления
Клиническими признаками общей реакции организма на воспаление являются повышение температуры тела, озноб, возбуждение или, наоборот, вялость больного, в крайне тяжёлых случаях затемнение (а иногда и потеря) сознания, головная боль, общее недомогание, разбитость, учащение пульса, выраженные изменения состава крови, признаки нарушения функций печени, почек, снижение АД, застой в малом круге кровообращения. Перечисленные симптомы могут носить ярко выраженный характер или быть малозаметными (в зависимости от характера, распространённости, локализации воспаления и особенностей реакции организма).
Температура тела при хирургической инфекции может достигать 40 °C и выше, возникают повторные озноб и головная боль, резко уменьшаются уровень гемоглобина и число эритроцитов, увеличивается содержание лейкоцитов, в тяжёлых случаях до 25, 0-30, 0х109/л. В плазме крови увеличивается уровень глобулинов и уменьшается количество альбуминов, у больных пропадает аппетит, нарушаются функции кишечника, появляется задержка стула, в моче определяются белок и цилиндры. Развивающаяся интоксикация приводит к нарушению функций органов кроветворения, в результате чего наступают анемизация больного и значительные изменения в составе белой крови: появляются незрелые форменные элементы, отмечается сдвиг лейкоцитарной формулы влево (уменьшение числа сегментоядерных и увеличение - палочкоядерных форм нейтрофилов). Для воспалительных процессов характерно резкое увеличение скорости оседания эритроцитов (появляясь в начале процесса, оно обычно наблюдается ещё долго после ликвидации воспаления). Иногда увеличиваются селезёнка, печень, появляется желтушная окраска склер.
При сильно выраженной (гиперергической) общей реакции организма на хирургическую инфекцию все перечисленные изменения проявляются в резкой степени; если реакция средняя или слабая, они бывают умеренными и даже малозаметными. Тем не менее любой местный воспалительный процесс сопровождается общими проявлениями, которые при гнойной инфекции имеют клиническую картину, весьма сходную с таковой при сепсисе и некоторых инфекционных заболеваниях (тифе, бруцеллёзе, паратифе, ту- беркулёзе и др. ). Поэтому такие больные нуждаются в тщательном клиническом обследовании, одна из важных целей которого - выявление первичного гнойного очага, входных ворот для гноеродных микроорганизмов. При выраженной общей реакции у больных с местным воспалительным процессом необходимо не только помнить о возможности инфекционного заболевания, но и повторными посевами крови установить наличие или отсутствие бактериемии. Обнаружение бактерий в крови, особенно при отсутствии клинического улучшения после хирургического воздействия на первичный очаг инфекции, свидетельствует о наличии сепсиса, а не просто об общей реакции на местный гнойный процесс.
Основным отличием общей реакции организма на гнойный процесс от сепсиса является то, что в первом случае все симптомы её резко ослабевают или исчезают при вскрытии гнойного очага и создании условий для хорошего дренирования; при сепсисе симптомы после этого почти не изменяются. Определение степени выраженности общей реакции на местную гнойную инфекцию имеет большое значение для правильной оценки состояния больного, характера развития воспаления и прогноза возможных осложнений.
+Клинические признаки эндогенной интоксикации зависят от степени её тяжести: чем выраженнее интоксикация, тем значительнее её проявления. При лёгкой степени интоксикации отмечается бледность кожного покрова, при тяжёлой - кожа землистого оттенка, определяются акроцианоз, гиперемия лица. Соответственно пульс частый - до 100- 110 в минуту, в тяжёлых случаях - более 130 в минуту, снижается АД. Развивается одышка - число дыханий до 25-30 в минуту, при тяжёлой интоксикации - более 30 в минуту. Важный показатель интоксикации - нарушение функций ЦНС: от лёгкой эйфории вначале до заторможённости или психического возбуждения при развитии токсемии, при тяжёлой интоксикации развивается интоксикационный делирий. Большое значение в оценке тяжести интоксикации имеет определение диуреза: при тяжёлой интоксикации количество мочи снижается, в крайне тяжёлых случаях развивается острая почечная недостаточность с выраженной олигурией и даже анурией.
Различают несколько путей проникновения возбудителей инфекционных заболеваний в организм человека:
с воздухом через пищеварительный тракт
через слизистые оболочки рта, носа, глаз
через поврежденные кожные покровы
через поврежденную кожу в результате укусов зараженных кровососущих насекомых

Различают экзогенный путь проникновения возбудителей в рану (контактный, капельный, воздушно-пылевой, имплантационный) и эндогенный — через кровеносные или лимфатические сосуды из определенного источника инфекции (абсцесс, флегмона, кариозные зубы, ангина и др. )
№3.
Экзогенные и эндогенные пути проникновения инфекции
Экзогенная (воздушно-капельная, контактная, имплантационная) инфекция.
Основным источником экзогенной инфекции являются больные с гнойно-воспалительными заболеваниями, бациллоносители, реже — животные (схема 1). От больных с гнойно-воспалительными заболеваниями микроорганизмы попадают во внешнюю среду (воздух, окружающие предметы, руки медицинского персонала) с гноем, слизью, мокротой и другими выделениями. При несоблюдении определенных правил поведения, режима работы, специальных методов обработки предметов, инструментов, рук, перевязочного материала микроорганизмы могут попасть в рану и вызвать гнойно-воспалительный процесс. Микроорганизмы проникают в рану из внешней среды различными путями: контактным — при соприкосновении с раной инфицированных предметов, инструментов, перевязочного материала, операционного белья; воздушным — из окружающего воздуха, в котором микроорганизмы находятся.
Эндогееная инфекция.
+Инфекция, которая попадает в рану из организма самого больного, называется эндогенной. Основные её источники: кожа пациента, внутренние органы, патологические очаги. Эндогенной называется инфекция, источник которой находится в организме самого больного. Ее источниками могут быть: кожа больного, желудочно-кишечный тракт, ротовая полость, а также очаги инфекции, наличие которых обусловлено существованием сопутствующих заболеваний. Наиболее частыми из них являются кариозные зубы, воспалительные заболевания мочевыводящих путей, хронический тонзиллит, аднексит, хронический бронхит и пр. Из очага инфекции в рану микроорганизмы могут попадать по кровеносным сосудам (гематогенно), но лимфатическим сосудам (лимфогенно) и непосредственно (контактно). Профилактика эндогенной инфекции - обязательный компонент современной хирургии. Различают профилактику эндогенной инфекции при плановой и экстренной операциях.
В основе профилактики хирургической инфекции неизменно на протяжении многих веков лежат методы асептики и антисептики. Наибольшее распространение получили методы биологической антисептики, включающие использование антибиотиков, ферментов и бактериофагов, а также методы физической антисептики, такие как орошение и дренирование ран, использование усовершенствованных перевязочных материалов и раневых покрытий.
Основные мероприятия по профилактике хирургической инфекции
Мероприятия по профилактике хирургической инфекции в основном следующие: 1. Дезинфекция
(уничтожение вегетативных форм микроорганизмов) и стерилизация (уничтожение микробов и
спор) изделий медицинского назначения (перевязочный материал, операционное белье, резиновые
изделия, металлический инструментарий и др. ). 2. Обработка рук хирурга и операционного поля.
3. Соблюдение строго режима и соблюдение мер по дезинфекции помещений и оборудования
операционного поля. 4. Выполнение особых приемов, имеющих целью не допустить загрязнение
операционной раны инфицированным содержимым внутренних полостей, абсцессов при вскрытии
их.
При экзогенном пути инфекция проникает в рану из внешней среды. Это может происходить контактным, воздушно-капельным (аэрозольным) и имплантационным путями. Эндогенный путь связан с проникновением в хирургическую рану инфекции, уже имеющейся в организме больного, при этом могут быть выявлены явные патологические процессы — воспаленные орга-ны.
№4.
Асептика – это комплекс мер, направленных на предупреждение попадания возбудителя инфекции в рану, органы больного при операциях, лечебных и диагностических процедурах. Асептика включает: стерилизацию и сохранение стерильности инструментов, перевязочного материала, операционного белья, перчаток и всего, что приходит в соприкосновение с раной: дезинфекция рук хирурга, операционного поля, аппаратуры, операционной и других помещений, применение специальной одежды, масок. К мерам асептики относится также планировка операционных (этаж, боксирование, вентиляция, кондиционирование воздуха).
Стерилизация – полное освобождение какого-либо вещества или предмета от микроорганизмов путем воздействия на них физическими или химическими факторами.
Используются следующие методы стерилизации:
• термические: паровой, воздушный, гласперленовый;
• химические: газовый, химические препараты;
• радиационный (установки с радиоактивным источником излучения для промышленной стерилизации изделий однократного применения);
1. Термический метод
В практике работы лечебных учреждений наиболее широкое распространение получил термический метод стерилизации с использованием насыщенного пара и сухого горячего воздуха (паровой и воздушный стерилизаторы).
Преимуществами термического метода стерилизации являются надежность, удобство и оперативность работы персонала, возможность использования разных видов упаковок с целью удлинения сроков сохранения стерильности изделий, отсутствие необходимости удаления остатков химических средств с изделий и т. д.
При паровом методе стерилизации стерилизующим средством является водяной насыщенный пар под избыточным давлением в паровых стерилизаторах (автоклавах).
Изделия (ватные шарики, шприцы, иглы, пеленки, пинцеты, катетеры, зонды, перчатки и т. д. ) размещают в стерилизационных коробках (биксах): в крафт-пакетах, в 2-х слойной мягкой бязевой упаковке.
Режим стерилизации
1. обычный режим — t = 132 0С, давление – 2 атм., время – 20 минут.
2. щадящий режим — t = 120 0С, давление – 1, 1 атм., время – 45 минут.
Эти режимы стерилизации используются для обработки изделий медицинского назначения
При воздушном методе стерилизации стерилизующим средством является сухой горячий воздух, стерилизацию осуществляют в воздушных стерилизаторах.
+Изделия (хирургические, стоматологические, гинекологические инструменты, детали приборов и аппаратов, в том числе изготовленные из коррозионно-нестойких материалов, шприцы с пометкой 200, инъекционные иглы, изделия из силиконовой резины) размещают в лотках (открытая емкость), крафт-бумаге.
Эффект стерилизации достигается лишь при равномерном распределении горячего воздуха. Поэтому беспорядочная загрузка стерилизатора не допускается.
Режим стерилизации
1. обычный режим — t = 180 0С, время -60 минут.
2. щадящий режим — t = 160 0С, время – 150 минут.
Эти режимы стерилизации используются для обработки изделий медицинского назначения
2. Химический метод — обеззараживание инструментов и изделий различными химическими средствами. Этот метод особенно ценен для обработки изделий, изготовленных из термолабильных материалов (к примеру, из стекла, пластмасс или резины). В частности, его применяют для стерилизации эндоскопов. Еще одним преимуществом метода можно назвать его дешевизну. Однако химический метод стерилизации достаточно трудоемкий, что можно расценивать как недостаток.
Особенности химического метода стерилизации инструментов
Для проведения стерилизации используют контейнер, который наполняют раствором химического средства. В наполненную емкость полностью погружают использованные инструменты, при этом они не должны лежать плотно друг к другу. Время экспозиции зависит от используемого химического средства и может составлять от 60 до 600 минут. По завершению обработки инструменты вынимают стерильными пинцетами и промывают в стерильной воде. Обработанные изделия хранят в стерильных контейнерах не более трех дней.
3. Радиационная стерилизация в ЛПУ
К сожалению, радиационные установки для стерилизации не устанавливаются в лечебно-профилактических учреждениях. Причин тому две: большая стоимость самой установки и техника безопасности. Однако в последние годы ведутся исследования в области разработки бюджетного и безопасного оборудования с использованием ускоренных электронов для стерилизации медицинских изделий в ЛПУ.

№5.
Кровотечение – истечение крови из кровеносных сосудов при разрушении или нарушении проницаемости их стенок.
Этиология.
- кровотечении возникающие вследствие повреждения сосудов при их ранении
- вследствие патологических изменения в стенке сосуда
- нарушения свертываемости системы крови
Различают 3 степени кровопотери: - умеренную – не более 25 % исходного ОЦК (1-1, 25 л крови); - большую, равную в среднем 30–40 % ОЦК (1, 5-2, 0 л крови); - массивную – более 40 % исходного ОЦК (2 л крови).
Классификация.
Физиологические и патологические
По анатомической классификации
- капиллярные
- паренхиматозные
- венозное
- артериальное
- сочетанное
По причине возникновения
- травматическое
- аррозивное, возникает вследствие нарушения целостности сосудистой стенки прорастание опухоли или ее распадом, язвенный и некротический процесс, инфекция, инородное тело
- диапедезные, вследствие нарушения проницаемости сосудистой стенки, авитаминозы, уремия, сепсис, холемия, действие токсинов.
4. По клинике
- наружные
- внутренние
- скрытые
5. В зависимости от скорости и объема кровопотери
- острое
-хроническое
6. По времени проявления
- первичное, сразу
- вторичное, через какое то время
- поздние вторичные, через несколько дней и даже недель после травмы
- повторные вторичные,
Наружное кровотечение – во внешнюю среду. Есть видимый источник в виде раны, открытого перелома либо размозженных мягких тканей.
Внутреннее кровотечение – в одну из естественных полостей тела, сообщающуюся с внешней средой: мочевой пузырь, легкое, желудок, кишечник.
Скрытое кровотечение – в ткани или полости тела, не сообщающиеся с внешней средой: в межфасциальное пространство, желудочки мозга, полость сустава, брюшную, перикардиальную или плевральную полости.
В зависимости от типа поврежденного сосуда, различают следующие виды кровотечений:
Артериальное кровотечение. Возникает при повреждении стенки артерии. Отличается высокой скоростью кровопотери, представляет опасность для жизни. Кровь ярко-алая, изливается напряженной пульсирующей струей.
Венозное кровотечение. Развивается при повреждении стенки вены. Скорость кровопотери ниже, чем при повреждении артерии аналогичного диаметра. Кровь темная, с вишневым оттенком, течет ровной струей, пульсация обычно отсутствует. При повреждении крупных венозных стволов может наблюдаться пульсирование в ритме дыхания.
Капиллярное кровотечение. Возникает при повреждении капилляров. Кровь выделяется отдельными каплями, напоминающими росу или конденсат (симптом «кровавой росы»).
Паренхиматозное кровотечение. Развивается при повреждении паренхиматозных органов (селезенки, печени, почек, легких, поджелудочной железы), пещеристой ткани и губчатого вещества кости. Из-за особенностей строения этих органов и тканей поврежденные сосуды не сдавливаются окружающей тканью и не сокращаются, что обуславливает значительные трудности при остановке кровотечения.
Смешанное кровотечение. Возникает при одновременном повреждении вен и артерий. Причиной, как правило, становится ранение паренхиматозных органов, имеющих развитую артериально-венозную сеть.
В зависимости от тяжести кровотечение может быть:
Легким (потеря не более 500 мл крови или 10-15% ОЦК).
Средним (потеря 500-1000 мл или 16-20% ОЦК).
Тяжелым (потеря 1-1, 5 л или 21-30% ОЦК).
Массивным (потеря более 1, 5 л или более 30% ОЦК).
Смертельным (потеря 2, 5-3 л или 50-60% ОЦК).
Абсолютно смертельным (потеря 3-3, 5 л или более 60% ОЦК).
К числу общих признаков кровотечения относятся головокружение, слабость, одышка, сильная жажда, бледность кожи и слизистых оболочек, снижение давления, учащение пульса (тахикардия), предобморочные состояния и обмороки. Выраженность и скорость развития перечисленных симптомов определяется скоростью истечения крови. Острая кровопотеря переносится тяжелее хронической, поскольку в последнем случае организм успевает частично «приспосабливаться» к происходящим изменениям.
Местные изменения зависят от особенностей травмы или патологического процесса и вида кровотечения. При наружных кровотечениях имеется нарушение целостности кожных покровов. При кровотечении из желудка возникает мелена (дегтеобразный черный жидкий стул) и рвота измененной темной кровью. При пищеводном кровотечении также возможна кровавая рвота, но кровь более яркая, красная, а не темная. Кровотечение из кишечника сопровождается меленой, но характерная темная рвота при этом отсутствует. При повреждении легкого отхаркивается ярко-алая, светлая пенящаяся кровь. Для кровотечения из почечной лоханки или мочевого пузыря характерна гематурия.
Скрытые кровотечения – самые опасные и самые сложные в плане диагностики, их можно выявить только по косвенным признакам. При этом скапливающаяся в полостях кровь сдавливает внутренние органы, нарушая их работу, что в некоторых случаях может стать причиной развития опасных осложнений и смерти больного. Гемоторакс сопровождается затруднением дыхания, одышкой и ослаблением перкуторного звука в нижних отделах грудной клетки (при спайках в плевральной полости возможно притупление в верхних или средних отделах). При гемоперикарде из-за сдавления миокарда нарушается сердечная деятельность, возможна остановка сердца. Кровотечение в брюшную полость проявляется вздутием живота и притуплением перкуторного звука в его отлогих отделах. При кровотечении в полость черепа возникают неврологические расстройства.
Истечение крови за пределы сосудистого русла оказывает выраженное негативное влияние на весь организм. Из-за кровотечения снижается ОЦК. В результате ухудшается сердечная деятельность, органы и ткани получают меньше кислорода. При продолжительной или обширной кровопотере развивается анемия. Потеря значительного объема ОЦК в течение короткого периода времени становится причиной травматического и гиповолемического шока. Развивается шоковое легкое, уменьшается объем почечной фильтрации, возникает олигурия или анурия. В печени формируются очаги некроза, возможна паренхиматозная желтуха.
Осложнения
Геморрагический шок, ишемия конечностей и гангрена, анемия общая, гипоксия, пульсирующая гематома, сдавление жизненно важных органов, гематомы.
Диагностика.
+ОАК, показатели количества эритроцитов, гемоглобина, гематокрита
ФГС, при подозрении на кровотечение из ЖКТ
УЗИ брюшной полости
РКС колоноскопия
Правила наложение жгута:
Перед наложение жгута следует приподнять конечность. Жгут накладывается проксимальные арт кровоток. Под жгут накладывают повязку. Время наложение жгута летом 2 часа, зимой 1 – 1, 5 часа
капиллярное
Кровотечение поверхностное, кровь по цвету близка к артериальной, выглядит как насыщенно-красная жидкость. Кровь вытекает в небольшом объёме, медленно. Так называемый симптом «кровавой росы», кровь появляется на поражённой поверхности медленно в виде небольших, медленно растущих капель, напоминающих капли росы или конденсата. Остановка кровотечения проводится с помощью тугого бинтования. При адекватной свертывающей способности крови свертывание проходит самостоятельно без медицинской помощи.
Артериальное
Артериальное кровотечение легко распознается по пульсирующей струе ярко-алой (темно-красной при повреждении легочной артерии) крови, которая вытекает очень быстро, возможно даже фонтанирует. Оказание первой помощи необходимо начать с пережатия сосуда выше места повреждения (ближе к телу). Далее накладывается жгут, который необходимо ослаблять каждый 1 час (зимой — 30 минут) у взрослых и на 20-40 минут — у детей, оставляя записку о времени наложения жгута. При полной остановке кровяного тока на продолжительное время (более 2 часов), может развиться некроз тканей.
Венозное
Венозное кровотечение характеризуется тем, что из раны постоянным потоком струится тёмная по цвету венозная кровь (либо ярко-алая если повреждена легочная вена). Сгустки крови, возникающие при повреждении, могут смываться потоком крови, поэтому возможна кровопотеря. При оказании помощи на рану необходимо наложить давящую марлевую повязку. Жгут применяется только в крайнем случае, если не получается остановить кровь давящей повязкой.
Паренхиматозное
Наблюдается при ранениях паренхиматозных органов (печень, поджелудочная железа, лёгкие, почки, селезёнка), губчатого вещества костей и пещеристой ткани. При этом кровоточит вся раневая поверхность. В паренхиматозных органах и пещеристой ткани перерезанные сосуды не сокращаются, не уходят в глубину ткани и не сдавливаются самой тканью. Кровотечение бывает очень обильным и нередко опасным для жизни. Остановить такое кровотечение очень трудно.
Смешанное кровотечение
Возникает при одновременном ранении артерий и вен, чаще всего при повреждении паренхиматозных органов (печень, селезёнка, почки, лёгкие), имеющих развитую сеть артериальных и венозных сосудов, а также при глубоких проникающих ранениях грудной и/или брюшной полости.
№6.
Шоковое состояние возникает при резком нарушении привычного кровообращения. Это тяжелая стрессовая реакция организма, не справившегося с управлением жизненно важными системами. Геморрагический шок вызывает внезапная кровопотеря. Поскольку кровь является основной жидкостью, поддерживающей метаболизм в клетках, то подобная разновидность патологии относится к гиповолемическим состояниям (обезвоживанию).




№7.
Методы временной остановки кровотечения
Временные способы остановки кровотечения по своей природе являются механическими.
Временная остановка наружного кровотечения осуществлется при оказании внебольничной (первая медицинская, фельдшерская, первая врачебная) помощи.
Основной задачей этих видов помощи является временная остановка наружного кровотечения. Правильное и своевременное выполнение этой задачи может оказаться решающим для спасения жизни пострадавшего.
Методы временной остановки кровотечения дают возможность спасти пострадавшего от острой кровопотери и предполагают немедленную остановку кровотечения на месте происшествия и доставку раненого в лечебное учреждение, где будет произведена окончательная остановка.
Прежде всего, необходимо определить наличие наружного кровотечения и его источник. Каждая минута промедления, особенно при массивном кровотечении, может оказаться роковой. Транспортировать пострадавшего с наружным кровотечением можно только после временной остановки кровотечения на месте происшествия.
Способы временной остановки кровотечений:
• прижатие артерии пальцами проксимальнее раны;
• максимальное сгибание конечности в суставе;
• приподнятое положение конечности;
• наложение давящей повязки;
• тугая тампонада раны;
• прижатие кровоточащего сосуда в ране;
• наложение зажим на кровоточащий сосуд в ране;
• наложение артериального жгута.
№8.
Первая помощь и лечение наружных кровотечений
При капиллярном или небольшом венозном кровотечении достаточно наложить давящую повязку.
При артериальных кровотечениях применяется форсированное сгибание конечности, пальцевое прижатие или наложение жгута. Вначале для того, чтобы немедленно остановить кровь, артерию прижимают пальцами или кулаком выше места повреждения, а затем накладывают жгут.
Наилучший вариант – фабричный жгут в виде резиновой ленты. Если такого жгута нет, можно использовать любые подручные средства: бинт, платок, пояс, ремень или галстук. Нельзя применять предметы, которые могут повредить ткани в месте наложения (например, проволоку). Под любой жгут по возможности следует подкладывать широкую полосу ткани, свернутую в несколько слоев – это предохранит подлежащие ткани от повреждения.
Жгут при артериальных кровотечениях накладывается выше места повреждения – на среднюю треть бедра или плеча – нервы в этих местах проходят достаточно глубоко, поэтому нет риска, что жгут их повредит. В то же время, достаточное количество мягких тканей обеспечивает мягкое, нетравматичное, но эффективное «пережимание» просвета артерии и быструю остановку кровотечения.
Наложение жгута на голень и предплечье нерационально – из-за недостаточного количества мягких тканей и особенностей месторасположения сосудов такой способ обычно недостаточно эффективен. Зимой у взрослых жгут накладывается на срок не более часа, у детей – на 10-15 минут. Летом у взрослых – на 1, 5-2 часа, у детей – на 25-30 минут.
Окончательная остановка кровотечения производится в специализированном медицинском учреждении. Лечением пациентов с капиллярными и венозными кровотечениями обычно занимаются травматологи. Помощь больному с артериальным кровотечением могут оказывать травматологи или сосудистые хирурги.
Для остановки наружного кровотечения применяется ушивание сосудов, реже – тампонада раны. При повреждении крупных артериальных стволов возможно наложение сосудистого шва. Операция по остановке кровотечения проводится в экстренном порядке и сопровождается общими мероприятиями, направленными на компенсацию кровопотери и предупреждение развития осложнений.
Неотложная помощь при внутреннем кровотечении:
При внутреннем кровотечении категорически нельзя принимать обезболивающие, кормить и поить пострадавшего.
Алгоритм оказания первой помощи:
1. Приложить холод в область травмы;
2. Придать положение полусидя;
3. Вызвать скорую медицинскую помощь либо отвезти пострадавшего в больницу.

№9.
Общее обезболивание (анестезия) — состояние обратимого тороможения центральной нервной системы, достигаемое фармакологическими средствами, воздействием физических или психических факторов. Оно предполагает подавление восприятия болевых раздражений, достижение нейровегетативной блокады и мышечной релаксации, выключение сознания, поддержание адекватного газообмена и кровообращения, регуляцию обменных процессов. К общему обезболиванию относят наркоз, нейролептаналгезию, атаралгезию, центральную аналгезию, аудиоанестезию и гипноз.
МЕСТНОЕ ОБЕЗБОЛИВАНИЕ
Местная анестезия предполагает обезболивание тканей операционного поля без выключения сознания больного, когда воздействие осуществляется на периферические механизмы восприятия и проведения болевого раздражения, т. е. на периферические отделы нервной системы. Различают инъекционный (иифильтрационная, проводниковая) и неинъекционный методы (химический, физический, физико-химический) местной анестезии.
Неинъекционная местная анестезия позволяет получить только поверхностное обезболивание тканей. Для этого используют лекар-ственные средства (химический или аппликационный метод), воздействие низкой температурой (замораживание), лучами лазера, электромагнитными волнами (физический метод), введение в ткани анестетика с помощью электрофореза (физико-химический метод).
Инъекцией раствора анестетика проводят инфильтрационную и проводниковую анестезию.
При инфильтрационной, аппликационной анестезии и обезболивании охлаждением выключают периферические рецепторы, воспринимающие болевые раздражения. При проводниковой анестезии блокируют нервный ствол (главный или чаще его периферические ветви), проводящий болевые импульсы из зоны оперативного вмешательства.
Показания и противопоказания к проведению местного обезболивания. Любое вмешательство в полости рта и на лице, сопровождающееся болью, является показанием к проведению местного обезболивания. Это операции на мягких тканях челюстно-лицевой области, на челюстях и зубах, органах полости рта. Местное обезболивание показано у ослабленных больных, у стариков, у лиц с дыхательной и сердечно-сосудистой недостаточностью, т. е. в тех случаях, когда и «малые наркозы связаны с большим риском».
Местная анестезия противопоказана при выполнении длительных и травматических операций, при непереносимости местных анестетиков или повышенной чувствительности к ним, при выраженной лабильности или неполноценности психики больного. Нежелательно применение местной анестезии при некоторых пластических операциях, когда введенный обезболивающий раствор значительно изменяет соотношение и объем тканей.
Передозировка препарата Новокаин, симптомы и лечение:
Передозировка новокаина вызывает двигательное возбуждение, коллапс, тошноту, рвоту, судороги, угнетение дыхания. В послеоперационный период возможны вторичная гиперемия и кровотечение как следствие применения адреномиметических средств в комбинации с местными анестетиками. У больных, а также у медицинского персонала возможна аллергия на Новокаин.
Лечение. При передозировке применяют искусственное дыхание, вдыхание карбогена, при судорогах вводят в/в барбитураты кратковременного действия, при коллапсе — в/в капельно кровозамещающие жидкости, при расстройстве сердечной деятельности — соответствующие реанимационные мероприятия.
№10.
Гру́ ппа кро́ ви — описание индивидуальных антигенных характеристик эритроцитов, определяемое с помощью методов идентификации специфических групп углеводов и белков, включённых в мембраны эритроцитов.
Резус-фактором (Rh)-называют антиген D, который может располагаться на поверхности эритроцитов. Наличие или отсутствие этого антигена на поверхности эритроцитов индивидуума определяет такую характеристику группы крови, как резус положительная или резус отрицательная (Rh+ или Rh–). Примерно 85% популяции людей имеют резус-положительную группу крови (Rh+). В отличие от антител к антигенам АВ, антитела к антигену D не присутствуют в крови.
Пробы на совместимость при переливании компонентов крови
1. Оценка пригодности гемотрансфузионной среды для переливания
убедиться в пригодности для переливания трансфузионной среды: удостовериться в правильности обозначения группы крови и резус-принадлежности, идентичности группы крови донора и реципиента. Провести визуальный контроль контейнера с компонентом крови. Проверить герметичность, правильность паспортизации, наличия номера, даты заготовки, обозначения группы крови, резус- принадлежности, наименование консерванта, Ф. И. О. донора, наименование учреждения-заготовителя, наличие подписи врача. Компоненты крови не должны содержать сгустки, признаки гемолиза и бактериального загрязнения. Критерий годности: прозрачность плазмы, отсутствие в ней мути, хлопьев, нитей фибрина, гемолиза, наличие чёткой границы между глобулярной массой и плазмой.
2. показания к переливанию: острая анемия (при кровопотере, геморрагическом шоке), хроническая анемия (при гипо/аплазии кроветворения), тромбоцитопения, лейкопения, плазмопотеря.
3. противопоказания: абсолютные (отек легких), относительные (остротекущий туберкулез, амилоидоз, печеночно/почечная недостаточность, нарушение коронарного кровообращения (инфаркт миокарда), гломерулонефрит, тяжелые аллергические состояния.
После переливания наблюдают за пациентом в течение 48 часов. Первые 2 часа – постельный режим. Проверяют мочу (количество введенной/выделенной жидкости, цвет, прозрачность), температуру, АД. Через сутки делают общ анализ крови, общ анализ мочи.
Перед переливанием проводят 3 пробы на совместимость:
1. совместимость по системе ABO. На планшетку нанести 2-3 капли плазмы донора, 1 каплю эритроцитов реципиента. Перемешать. Ждать 5 мин. Если агглютинации нет, то переливаем. Если есть – помещаем планшетку в суховоздушный шкаф на 5 мин (температура 37 градусов). Агглютинация есть – не переливаем, нет – переливаем.
2. Совместимость по резусу. В центрифужную пробирку капают 2 капли плазмы донора, 1 калю эритроцитов реципиента, 1 каплю 33% полиглюкина. Встряхнуть, прокручивать 5 мин. Добавить 2-3 мл NaCl, 2-3 раза перемешать. Оценить результаты.
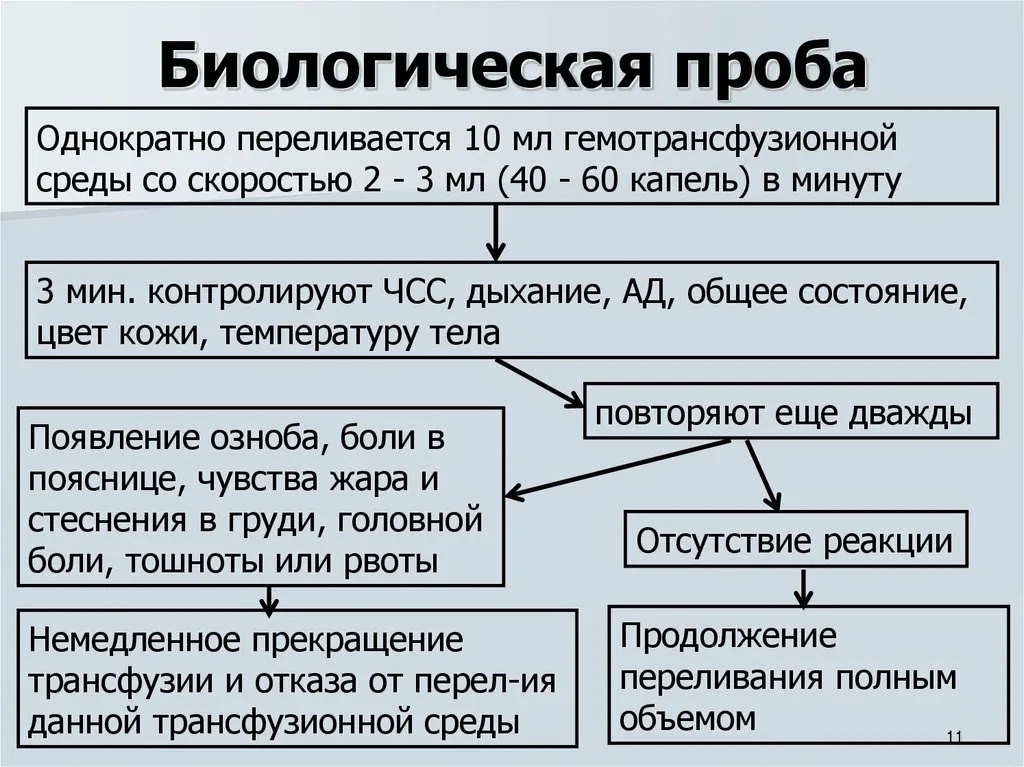
3. Биологическая проба. Влить струйно пациенту 10-15 мл крови, наблюдать за реакцией. Если появились осложнения (учащение дыхания, сердцебиение, одышка, гиперемия лица, боль в пояснице) переливать кровь нельзя. Если этого ничего нет, проводим пробу еще 2 раза, наблюдаем за состоянием. Если без осложнений – переливает кровь.
Проба Бакстера: проводится больным в коме, псих. Больным, глухонемым, находящимся под наркозом. Ввести 30-45 мл эритромассы, взять из вены 5-10 мл крови. Поместить в центрифугу, если сыворотка розовая, это гемолиз, переливать нельзя. Если сыворотка соломенная, переливаем.
13. Способы определения групповой принадлежности. Перекрестный метод определения групп крови по системе «аво», его предназначение.
Способы определения групповой принадлежности крови индивидуума основываются на трех принципах антигенной совместимости (Ландштейнер):
1. У одного человека не может быть одноименных АГ и АТ.
2. Если в эритроцитах имеется антиген одной изопары, то в плазме присутствует антитело другой изопары.
3. При встрече одноименных антигенов и антител происходит реакция агглютинации эритроцитов.
Основное значение для обеспечения совместимости при переливании компонентов крови имеет выбор крови по системе «АВО». Выделяют два способа определения группы крови системы «АВО»:
1. Прямой метод (прямая реакция): устанавливают наличие или отсутствие групповых АГ системы «АВО» при помощи известных АТ. Происходит определение группы крови при помощи стандартных изогемагглютинирующих сывороток или моноклональных антител.
2. Перекрестный метод (перекрестная реакция): устанавливают наличие и АГ, и АТ при помощи стандартных изогемагглютинирующих сывороток или моноклональных антител, а также при помощи стандартных эритроцитов.
Перекрестный метод - заключается в одновременном определении АГ при помощи стандартных сывороток, и АТ при помощи стандартных эритроцитов. У исследуемого берут кровь из вены. Ее либо центрифугируют, либо оставляют постоять 20-30 минут для отделения сыворотки. Пипеткой извлекают сыворотку, капают ее по 0, 1 мл на стандартные эритроциты. После пипеткой набирают со дна пробирки эритроциты и помещают по маленькой капле рядом со стандартными сыворотками. Тщательно перемешивают, оставляют на 1-2 минуты в покое, затем поколачивают. На 3 минуте добавляют теплый NaCl (для исключения ложной холодовой агглютинации, когда эритроциты могут принимать вид «монетных столбиков»). Если после этого агглютинация исчезла, то она была ложной, если осталась – то образовался комплекс антиген-антитело.
Положит. Результат: появляются агглютинаты (комочки из эритроцитов).
Отрицательный результат: в течение 5 минут жидкость остается равномерно красной.

№11.
Кровезаменители. Классификация. Показания к применению.
Кровезаменитель – физически однородная трансфузионная среда с целенаправленным действием на организм, способная заменить определенную функцию крови.
Кровезаменители принято делить на:
- коллоидные растворы (декстраны, препараты желатина)
- солевые растворы (изотонический раствор NaCl, раствор Рингера-Локка: содержит NaCl)
- буферные растворы (раствор гидрокарбоната натрия, раствор трометамола)
- растворы сахаров и многоатомных спиртов (декстроза, сорбитол, фруктоза)
- белковые препараты (гидролизаты белков, растворы аминокислот) - препараты жиров – жировые эмульсии (триглицериды)
- препараты оксиэтилкрахмала (гидроксиэтилкрахмал)
Классификация кровезамещающих жидкостей (в зависимости от направленности действия):
1. Гемодинамические (противошоковые): декстран, препараты желатина, препараты на основе оксиэтилкрахмала
2. Дезинтоксикационные: низкомолекулярный поливиниловый спирт
3. Препараты для парентерального питания: растворы аминокислот, жировые эмульсии, сахара и многоатомные спирты
4. Регуляторы водно-солевого и кислотно-основного состояния: солевые растворы, буферные растворы
5. Переносчики кислорода: перфторан, перфукал
Показания к применению:
1. Гемодинамических (противошоковых) кровезаменителей: различные виды шока, острая кровопотеря, при нарушениях микроцеркуляции (декстран).
2. Дезинтоксикационных кровезаменителей: при гнойной интоксикации, травматическом токсикозе
3. Препаратов для парентерального питания: если энтеральное питание невозможно или ограничено (гипопртеинемия, гнойные заболевания, ожоги)
4. Регуляторов водно-солевого и кислотно-основного состояния: обезвоживание, нарушение электролитного баланса, нарушение кислотно-основного состояния.
№12.
Виды уборки операционной
Выделяют пять видов уборки помещения операционной.
Предварительная уборка – Ежедневно утром перед началом работы. Главной её целью является удаление осевшей за ночь пыли на горизонтальных поверхностях предметов и самой операционной. При этом сначала протирают чистой сухой ветошью полированные и никелированные поверхности мебели и оборудования. Затем влажной ветошью протирают операционные столы и завершают уборку подтиранием пола.
Текущая уборка – выполняют во время операции. Несмотря на то, что около операционного стола ставят тазик для использованного материала, на пол могут упасть салфетки, инструменты и использованное операционное бельё, их тотчас убирают в специальные ёмкости. При выполнении операции на органах живота на пол попадает содержимое брюшной полости, которое убирают чистой ветошью. После этого пол протирают дезинфицирующим раствором.
Послеоперационная уборка – По завершении оперативного вмешательства. Она состоит в удалении из операционной всего, что использовали во время операции и не потребуется в дальнейшей работе. Меняют бельё на операционном столе, приводят в порядок состояние не стерильных столов, пополняют запасы растворов. В заключение протирают пол влажной ветошью, подготавливая таким образом помещение к следующей операции.
Заключительная уборка – Ежедневно в конце рабочего дня., во время которой помимо удаления использованного материала, белья, инструментов проверяют готовность аппаратуры и различных устройств, протирают их влажной или сухой чистой ветошью. Рамы, стёкла и подоконники, светильники, мебель и калориферы центрального отопления протирают влажной ветошью. Подставки под ноги, пол и прилежащие части стен моют шваброй или щётками. По окончании уборки операционный стол, наркозный аппарат и другую аппаратуру покрывают чистой простынёй.
Последовательность действий во время уборки сводится к тому, что вначале обрабатывают потолок и стены, затем окна, подоконники, калориферы и завершают уборку мытьём пола методом двух вёдер. При этом сначала сдвигают всю аппаратуру в одну сторону помещения, моют пол на освободившейся части и вытирают его насухо, затем то же самое делают со второй половиной пола. Уходя из помещения, включают бактерицидную лампу и так же убирают другие помещения зоны стерильного режима.
(для влажной уборки пользуются 0, 75% раствором хлорамина Б или 3% раствором перекиси водорода, которые изготавливают на 0, 5% растворе синтетических моющих средств, а также раствором первомура или другими средствами, оставшимися после обработки рук участников операции).
Плановая дезинфекция (генеральная уборка) – в конце рабочей недели в операционной и в конце месяца во всём операционном блоке. На время уборки из помещения всё, что можно выносят, стены и потолок опрыскивают дезинфицирующим раствором с помощью гидропульта и сразу же их протирают насухо, чтобы не образовались подтёки. Затем моют пол, используя те же дезинфицирующие средства (0, 75% раствор хлорамина Б или 6% раствор перекиси водорода, которые изготовлены на 0, 5% растворе синтетических моющих средств, а также 2, 4-4, 8% раствор первомура или 3% раствор лизола).
При загрязнении операционной кишечным содержимым, гноем и после операций у больных с анаэробной инфекцией тотчас по завершении оперативного вмешательства по той же методике выполняют внеплановую дезинфекцию.
Профилактика воздушно-капельной инфекции. Стерилизация воздуха
Ношение масок
Для предупреждения воздушно-капельной инфекции применяется комплекс мер, главными из которых являются организационные мероприятия, направленные на уменьшение загрязнения воздуха микробами, а также на уничтожение уже имеющихся.
Принцип соблюдения правил асептики и антисептики лежит основе организации хирургического стационара. Большинство больниц строится в зеленых, наиболее чистых районах. Хирургические отделения не должны располагаться на первом этаже стационара, по возможности палаты должны быть рассчитаны на 1-2 человек.
В хирургическом отделении должны быть оборудованы палаты для больных, пост палатной медсестры, процедурный кабинет, чистая и гнойная перевязочные, санитарная комната, лечебные и диагностические кабинеты, кабинеты заведующего отделением и старшей медсестры, ординаторская, сестринская.
Хирургическое отделение должно быть приспособлено для тщательной многократной влажной уборки с применением антисептических средств. Для этого полы должны быть каменными или заливными, либо покрыты линолеумом. Стены выложены плиткой или окрашены краской. В операционной и перевязочной эти же требования предъявляются и к потолкам.
В хирургическом отделении обязательно использование спецодежды. Все работники должны иметь сменную обувь, халаты или специальные костюмы из легкой ткани, регулярно проходящие стирку. Оптимальным является использование санпропускника: сотрудники, приходящие на работу, принимают душ, снимают с себя повседневную одежду и надевают костюмы (халаты). Выход в спецодежде за пределы отделения не разрешается.
В перевязочной, процедурном кабинете, в операционной, в послеоперационных отделениях и отделении реанимации необходимо ношение колпаков и масок. Ношение колпаков обязательно для постовых медсестер, выполняющих различные процедуры у постели больно (инъекции, забор крови на анализ и т. д. ). Для профилактики воздушно-капельной инфекции большое значение имеет контроль за соблюдением правил личной гигиены медперсоналом, отстранение от работы сотрудников с простудными и гнойничковыми заболеваниями.
Маски используются медицинским персоналом для уменьшения выделения при дыхании капель секрета из носоглотки и ротовой полости во внешнюю среду. Существует два типа масок: фильтрующие и отражающие.
К фильтрующим прежде всего относятся марлевые маски. 3-слойные марлевые маски, закрывающие нос и рот, задерживают 70% выдыхаемых микроорганизмов, 4-слойные — 88%, 6-слойные — 96%. Однако, чем больше слоев, тем хирургу труднее дышать. При увлажнении марли ее фильтрующая способность падает. Через 3 часа 100% 3-слойных марлевых масок обильно обсеменены микрофлорой. Для придания маскам большего эффекта они пропитываются антисептиком (например, хлоргексидином), высушиваются и автоклавируются. Свойства таких масок сохраняются 5-6 часов. Современные разовые маски из целлюлозы обычно эффективны в течение 1 часа.
В отражающих масках конденсат из выдыхаемого воздуха стекает по стенкам маски в специальные емкости. Оперировать в таких масках трудно.
Ношение масок обязательно в операционной (причем каждый раз — новой, стерильной маски), в перевязочной.
Бактерицидные лампы
Одна бактерицидная лампа в течение 2 часов стерилизует 30 м воздуха, кроме того, уничтожаются микроорганизмы на открытых поверхностях. Бактерицидные лампы должны обязательно быть в операционных, перевязочных, процедурных кабинетах, послеоперационных и реанимационных палатах, палатах для гнойных больных.
№13.
Предоперационный период и подготовка больного к операции.
Предоперационная подготовка начинается с момента постановки диагноза, требующего операции, и принятия решения о выполнении оперативного вмешательства. Заканчивается же она подачей больного в операционную.
Весь предоперационный период условно делят на два этапа:
диагностический и подготовительный, во время которых решают основные задачи предоперационной подготовки.
1)Диагностический этап
Задачи диагностического этапа - установление точного диагноза основного заболевания и оценка состояния основных органов и систем организма больного.
• предварительная оценка;
• стандартный минимум обследования (клинический анализ крови; биохимический анализ крови; время свёртывания крови; группа крови и резус-фактор; общий анализ мочи; флюорография органов грудной клетки; заключение стоматолога о санации ротовой полости; ЭКГ; осмотр терапевта; для женщин - осмотр гинеколога. );
• дополнительное обследование (проводят при выявлении у пациента сопутствующих заболеваний или при отклонении от нормы результатов лабораторных исследований. );
• определение противопоказаний к операции.
2)Подготовительный этап
Существует три основных вида предоперационной подготовки:
• психологическая;
• общая соматическая (её задача - добиться компенсации нарушенных в результате основного и сопутствующих заболеваний функций органов и систем, а также создания резерва в их функционировании);
• специальная (её необходимость связана с особыми свойствами органов, на которых выполняют операцию, например назначение диеты, клизмы).
Непосредственная подготовка больного к операции:
«Пустой желудок»
Для профилактики аспирации перед плановой операцией больной с утра в день операции не ест и не пьет ни капли жидкости, а накануне не очень плотно ужинает в 5-6 ч вечера.
Опорожнение кишечника
Перед плановой операцией больным нужно сделать очистительную клизму
Опорожнение мочевого пузыря
Премедикация
Премедикация - введение медикаментозных средств перед операцией с целью снижения вероятности интра- и послеоперационных осложнений. Премедикация необходима для решения нескольких задач:
• снижение эмоционального возбуждения;
• нейровегетативная стабилизация;
• снижение реакций на внешние раздражители;
• создание оптимальных условий для действия анестетиков;
• профилактика аллергических реакций на средства, используемые при анестезии;
• уменьшение секреции желёз.
Для премедикации используют следующие основные группы фармакологических веществ.
1. Снотворные средства (барбитураты: фенобарбитал; бензодиазепины: нитразепам, флунитразепам).
2. Транквилизаторы (диазепам, бромдигидрохлорфенилбензодиазе- пин, оксазепам). Эти препараты оказывают снотворное, противосудорожное, гипнотическое и амнезическое действие, устраняют тревогу и потенцируют действие общих анестетиков, повышают порог болевой чувствительности. Всё это делает их ведущими средствами премедикации.
3. Нейролептики (галоперидол, дроперидол).
4. Антигистаминные средства (дифенгидрамин, хлоропирамин, клемастин).
5. Наркотические анальгетики (тримеперидин, морфин, морфин + наркотин + папаверин + кодеин + тебаин) устраняют боль, оказывают седативный и снотворный эффекты, потенцируют действие анестетиков.
6. Холинолитические средства (атропин, метоциния йодид) блокируют вагусные рефлексы, тормозят секрецию желёз.
№14.
Послеоперационный период. Ранние и поздние осложнения, уход за больными.
Послеоперационный период.
Послеоперационный период начинается сразу же после окончания операции и заканчивается выздоровлением больного. Он делится на 3 части:
1. ранний - 3-5 суток
2. поздний - 2-3 недели
3. отдаленный (реабилитации) - обычно от 3 недель до 2-3 месяцев
Основными задачами послеоперационного периода являются:
Профилактика и лечение послеоперационных осложнений.
Ускорение процессов регенерации.
Реабилитация больных.
Ранний послеоперационный период - это время, когда на организм больного прежде всего оказывают влияние операционная травма, последствия наркоза и вынужденное положение.
Ранний послеоперационный период может быть неосложненным и осложненным.
При неосложненном течении послеоперационного периода реактивные изменения, возникающие в организме, обычно выражены умеренно и длятся в течение 2-3 дней. При этом отмечается лихорадка до 37, 0-37, 5 °С, наблюдается торможение ЦНС, может быть умеренный лейкоцитоз и анемия. Поэтому основной задачей является коррекция изменений в организме, контроль функционального состояния основных органов и систем.
Терапия при неосложненном послеоперационном периоде заключается в следующем:
1. борьба с болью;
2. правильное положение в постели (положение Фовлера – приподнят головной конец);
3. ношение бандажа;
4. предупреждение и лечение дыхательной недостаточности;
5. коррекция водно-электролитного обмена;
6. сбалансированное питание;
7. контроль функции выделительной системы.
Основные осложнения раннего послеоперационного периода.
I. Осложнения со стороны раны:
кровотечение,
развитие раневой инфекции,
расхождение швов (эвентерация).
Кровотечение- наиболее грозное осложнение, порой угрожающее жизни больного и требующее повторной операции. В послеоперационном периоде для профилактики кровотечения на рану кладут пузырь со льдом или груз с песком. Для своевременной диагностики следят за частотой пульса, АД, показателями красной крови.
Развитие раневой инфекцииможет протекать в виде образования инфильтратов, нагноения раны или развития более грозного осложнения - сепсиса. Поэтому необходимо обязательно перевязывать больных на следующий день после операции. Чтобы снять перевязочный материал, всегда промокающей сукровичным раневым отделяемым, обработать антисептиком края раны и положить защитную асептическую повязку. После этого повязку меняют раз в 3 дня, когда она промокла. По показаниям назначают УВЧ-терапию на область оперативного вмешательства (инфильтраты) или антибиотикотерапию. Необходимо следить за портальным функционированием дренажей.
Расхождение швов (эвентерация)наиболее опасно после операций на брюшной полости. Оно может быть связано с техническими погрешностями при зашивании раны (близко захватывают в шов края брюшины или апоневроза), а также со значительным повышением внутрибрюшного давления (при перитоните, пневмонии с выраженным кашлевым синдромом) или с развитием инфекции в ране. Для профилактики расхождения швов при повторных операциях и при высоком риске развития этого осложнения применяют ушивание раны передней брюшной стенки на пуговицах или трубках.
II. Основными осложнениями со стороны нервной системы: в раннем послеоперационном периоде являются боли, шок, нарушения сна и психики.
Устранению боли в послеоперационном периоде придается исключительно большое значение. Болевые ощущения способны рефлекторно привести к нарушению деятельности сердечно-сосудистой системы, органов дыхания, желудочно-кишечного тракта, органов мочевыделения.
Борьба с болью осуществляется назначением анальгетиков (промедол, омнопон, морфин). Необходимо подчеркнуть, что необоснованное длительное применение препаратов этой группы может привести к возникновению болезненного пристрастия к ним - наркомании. Это особенно актуально в наше время. В клинике кроме анальгетиков применяется длительная перидуральная анестезия. Она особенно эффективна после операций на органах брюшной полости; в течение 5-6 суток дает возможность резко снизить болевые ощущения в области операции и в кратчайшие сроки ликвидировать пару кишечника (1% раствор тримекаина, 2% раствор лидокаина).
Устранение боли, борьба с интоксикацией и чрезмерным возбуждением нервно-психической сферы являются профилактикой таких осложнений со стороны нервной системы как послеоперационное нарушение сна и психики. Послеоперационные психозы чаще развиваются у ослабленных, истощенных больных (бомжей, наркоманов). Необходимо подчеркнуть, что больные с послеоперационными психозами нуждаются в постоянном надзоре. Лечение проводится совместно с психиатром.
Рассмотрим пример: У больного с деструктивным панкреатитом в раннем послеоперационном периоде возник психоз. Он выпрыгнул из окна реанимации.
III. Осложнения со стороны сердечно-сосудистой системымогут наступить первично, в результате слабости сердечной деятельности, и вторично, в результате развития шока, анемии, выраженной интоксикации.
Развитие этих осложнений обычно связано с сопутствующими заболеваниями, поэтому их профилактика во многом определяется лечением сопутствующей патологии. Рациональное применение сердечных гликозидов, глюко-кортикоидов, иногда вазопрессантов (дофамин), возмещение кровопотери, полноценная оксигенация крови, борьба с интоксикацией и другие мероприятия, выполняемые с учетом индивидуальных особенностей каждого больного дают возможность в большинстве случаев справиться с этим тяжелым осложнением послеоперационного периода.
Важным является вопрос о профилактике тромбоэмболических осложнений, наиболее частым из которых является тромбоэмболия легочной артерии- тяжелое осложнение, являющееся одной из частых причин летальных исходов в раннем послеоперационном периоде. Развитие тромбозов после операции обусловлено замедленным кровотоком (особенно в венах нижних конечностей и малого таза), повышением вязкости крови, нарушением водно-электролитного баланса, нестабильной гемодинамикой и активацией свертывающей системы вследствие интраоперационного повреждения тканей. Особенно велик риск тромбоэмболии легочной артерии у пожилых тучных больных с сопутствующей патологией сердечно-сосудистой системы, наличием варикозной болезни нижних конечностей и тромбофлебитов в анамнезе.
Принципы профилактики тромбоэмболических осложнений:
1. ранняя активизация больных, активное ведение их в послеоперационном периоде;
2. воздействие на возможный источник (например, лечение тромбофлебита);
3. обеспечение стабильной динамики (контроль АД, пульса);
4. коррекция водно-электролитного баланса с тенденцией к гемодилюции;
5. использование дезагрегантов и других средств, улучшающих реологические свойства крови (реополиглюкин, трентал, неотон);
6. применение антикоагулянтов прямого (гепарин, фраксипарин, стрептокиназа) и непрямого действия (синкумар, пелентан, эскузин, фенилин, дикумарин, неодикумарин);
7. бинтование нижних конечностей у больных с варикозным расширением вен.
IV. Среди послеоперационных осложнений со стороны органов дыханиянаиболее частыми являются трахеобронхиты, пневмонии, ателектазы, плевриты. Но наиболее грозное осложнение -развитие острой дыхательной недостаточности, связанной прежде всего с последствиями наркоза.
Поэтому главными мероприятиями по профилактике и лечению осложнений со стороны органов дыханияявляются:
ранняя активизация больных,
адекватное положение в постели с приподнятым головным концом
(положение Фовлера),
дыхательная гимнастика,
борьба с гиповентиляцией легких и улучшение дренажной функции трахеобронхиального дерева (ингаляции увлажненным кислородом,
банки, горчичники, массаж, физиотерапия),
разжижение мокроты и применение отхаркивающих средств,
назначение антибиотиков и сульфаниламидных препаратов с учетом чувствительности,
санация трахеобронхиального дерева у тяжелобольных (через интубационную трубку при продленной ИВЛ или через микротрахеостому при спонтанном дыхании)
Разбор ингаляторов и кислородной системы.
V. Осложнения со стороны брюшной полости и в послеоперационном периоде достаточно тяжелы и разнообразны. Среди них особое место занимают перитонит, спаечная кишечная непроходимость, парез желудочно-кишечного тракта. Внимание обращается на сбор информации при исследовании брюшной полости: исследование языка, осмотр, пальпация, перкуссия, аускультация живота; пальцевое исследование прямой кишки. Подчеркивается особое значение в диагностике перитонита таких симптомов как икота, рвота, сухость языка, напряжение мышц передней брюшной стенки, вздутие живота, ослабление или отсутствие перистальтики, наличие свободной жидкости в брюшной полости, появление симптома Щеткина-Блюмберга.
Наиболее частым осложнением является развитие паралитической непроходимости (парез кишечника). Парез кишечника значительно нарушает процессы пищеварения, и не только их. Повышение внутрибрюшного давления приводит к высокому стоянию диафрагмы, нарушению вентиляции легких и деятельности сердца; кроме того, происходит перераспределение жидкости в организме, всасывание токсичных веществ из просвета кишечника с развитием выраженной интоксикации организма.
Основы профилактики пареза кишечника закладываются на операции:
бережное отношение с тканями;
минимальное инфицирование брюшной полости (использование тампонов);
тщательное гемостаз;
новокаиновая блокада корня брыжейки в крнце операции.
Принципы профилактики и борьбы с парезом после операции:
+
ранняя активизация больных с ношением бандажа;
рациональный режим питания (малыми удобными порциями);
адекватное дренирование желудка;
введение газоотводной трубки;
стимуляция моторики желудочно-кишечного тракта (прозерин 0, 05% - 1, 0 мл подкожно; 40-60 мл гипертонического раствора в/в медленно капельно; церукал 2, 0 мл в/м; очистительная или гипертоническая клизма);
2-х сторонняя новокаиновая паранефральная блокада или перидуральная блокада;
ГБО-терапия.
Послеоперационный период – это промежуток времени от окончания операции до выздоровления больного или перевода его на инвалидность.
Основная цель послеоперационного периода -способствовать процессам регенерации и адаптации, происходящим в организме больного, а также предупреждать, своевременно выявлять и лечить возникающие осложнения.
Принято разделять послеоперационный период на три фазы:
+1. Ранняя фаза ( ранний послеоперационный период) –до 3-5 суток после операции.
2. Поздняя фаза ( поздний послеоперационный период) – 2 – 3 недели после операции.
3. Отдалённая фаза - 3 недели – 3 месяца после операции.
Основными задачами медперсонала в послеоперационном периоде являются:
1. Обеспечить уход за больным силами врача, медсестёр, санитаров ( обезболивание, обеспечение жизненно важных функций, перевязки).
Предупредить возникновение и провести лечение возникших в послеоперационном периоде осложнений.
По окончании операции прекращается введение наркотических веществ.
2. Больного транспортируют из операционной на каталке в послеоперационную палату, или в отделение реанимации и интенсивной терапии. При этом больной может быть вывезен из операционной только с восстановленным самостоятельным дыханием.
3. Врач анестезиолог обязательно должен сопровождать больного в отделение реанимации, или посленаркозную палату вместе с двумя (не менее) медсёстрами.
4. Во время перевозки больного необходимо следить за положением катетеров, дренажей, повязок. Неосторожное обращение с больным может привести к выпадению дренажей, снятию послеоперационной повязки, случайному удалению эндотрахеальной трубки. Анестезиолог должен быть готовым к нарушениям дыхания при транспортировке. С этой целью бригаде, транспортирующей больного, необходимо иметь с собой ручной дыхательный аппарат (или мешок Амбу).
5. Во время транспортировки может проводиться (продолжаться) внутривенная инфузионная терапия, но в большинстве случаев при перевозке система для внутривенного капельного введения растворов перекрывается.
Больной в посленаркозном периоде вплоть до полного пробуждения должен находиться под постоянным наблюдением медперсонала, так как в первые часы после хирургической операции наиболее вероятны
осложнения, связанные с наркозом:
1. Западение языка
2. Рвота.
3. Нарушение терморегуляции.
4. Нарушение сердечного ритма.
-Западение языка
У находящегося ещё в наркотическом сне больного мышцы лица, языка и тела расслаблены. Расслабленный язык может сместиться вниз и закрыть просвет дыхательных путей. Необходимо своевременное восстановление проходимости дыхательных путей с помощью введения воздуховодной трубки, или же при помощи запрокидывания головы и выведения нижней челюсти.
Следует помнить, что пациент после наркоза должен постоянно находиться под наблюдением дежурного медперсонала вплоть до полного пробуждения.
-Рвота в посленаркозном периоде
Опасность рвоты в послеоперационном периоде обусловлена возможностью затекания рвотных масс в ротовую полость, а затем в дыхательные пути (регургитация и аспирация рвотных масс). Если больной находится в наркотическом сне, это может привести к его смерти от асфикисии. При рвоте у больного в бессознательном состоянии необходимо его голову повернуть набок и очистить полость рта от рвотных масс. В послеоперационной палате должен быть готовым к работе электроаспиратор, которым из ротовой полости, или из дыхательных путей при ларингоскопии удаляются рвотные массы.
Рвотные массы можно также удалять из ротовой полости при помощи марлевой салфетки на корнцанге.
Если рвота развилась у больного, находящегося в сознании, необходимо помочь ему, подав тазик, поддержать над тазиком его голову. При повторной рвоте рекомендуется ввести больному церукал (метоклопрамид)
Нарушение ритма сердечной деятельности и дыхания вплоть до их остановки наступает чаще у пожилых людей и детей грудного возраста. Возможна остановка дыхания также вследствие рекураризации – повторного позднего расслабления дыхательных мышц после проведения миорелаксации при эндотрахеальном наркозе. Необходимо в таких случаях быть готовым к проведению реанимационных мероприятий и иметь наготове дыхательную аппаратуру.
-Нарушение терморегуляции
Нарушение терморегуляции после наркоза может выражаться в резком повышении или снижении температуры тела, сильном ознобе. При необходимости требуется накрыть больного, или же наоборот, создать условия создать условия для улучшенного охлаждения его тела.
При высокой гипертермии применяют внутримышечное введение анальгина с папаверином и димедролом. Если и после введения литической смеси температура тела не снижается, используют физическое охлаждение тела растиранием спиртом. При прогрессировании гипертермии внутримышечно вводят ганглиоблокаторы (пентамин, или бензогексоний)
При значительном снижении температуры тела (ниже 36, 0 – 35, 5 град) можно применить согревание тела и конечностей больного тёплыми грелками.
-Борьба с болью в послеоперационном периоде.
Осложнения, связанные с болью в послеоперационном периоде.
Длительное воздействие боли и боли высокой интенсивности приводят не только к морально-психическим переживаниям, но и к вполне реальным биохимическим обменным нарушениям в организме. Выброс в кровь большого количества адреналина (" стрессгормона", вырабатываемого корой надпочечников) приводит к повышению артериального давления, учащению пульса, психическому и двигательному ( моторному ) возбуждению. Затем при продолжении боли нарушается проницаемость стенок кровеносных сосудов, и плазма крови постепенно выходит в межклеточное пространство. Развиваются и биохимические сдвиги в составе крови - гиперкапния ( повышение концентрации СО 2 ), гипоксия ( снижение концентрации кислорода), ацидоз (увеличение кислотности крови), происходят изменения в свёртывающей системе крови. Связанные воедино кровеносной системой, поражаются все органы и системы человека. Развивается болевой шок.
Современные методы анестезии позволяют предупредить опасные последствия боли при травмах, хирургических заболеваниях и при проведении хирургических операций.
Задачами медперсонала при купировании болевого синдрома являются:
Снижение интенсивности боли
1. Уменьшение продолжительности боли
2. Минимизация тяжести побочных нарушений, связанных с болью.
3. Стратегия профилактики болей предусматривает:
4. Ограничение количества пункций, инъекций, взятия анализов.
5. Использование центральных катетеров для исключения многократных пункций вен.
6. Болезненные процедуры должен осуществлять только подготовленный медперсонал.
7. Бережное проведение перевязок, удаления лейкопластыря, дренажей, катетеров.
8. Обеспечение адекватного обезболивания перед болезненными процедурами
Нефармакологические методы борьбы с болью.
1. Создание комфортных условий для пациента
2. Болезненные процедуры должен выполнять только опытный специалист
3. Создаются максимальные перерывы между болезненными процедурами.
4. Поддержание выгодного ( наименее болезненного) положения тела больного.
5. Ограничение внешних раздражителей ( свет, звук, музыка, громкий разговор, быстрые движения персонала).
6. Кроме этого целесообразно применение холода с целью уменьшения боли в области операционной раны. При местном применении холода снижается чувствительность болевых рецепторов. На операционную рану накладывают пузырь со льдом, либо с холодной водой.
Фармакологические методы борьбы с болью:
1. Применение наркотических анестетиков
Промедол – используется как универсальный наркотический анальгетик после большинства хирургических операций
Фентанил - в послеоперационном периоде применяется в дозе
0, 5 – 0, 1 мг при интенсивных болях. Используется также в сочетании с дроперидолом ( нейролептанальгезия)
Трамадол – обладает менее выраженными наркотическими свойствами, т. е. вызывает эйфорию, привыкание и синдром отмены заметно меньше, чем наркотики. Применяется в виде раствора подкожно, внутримышечно и внутривенно капельно по 50мг в 1 мл (ампулы 1 и 2 мл).
2. Применение ненаркотических анестетиков.
Барбитураты – фенобарбитал и тиопентал натрия обладают снотворным и обезболивающим эффектом
Ибупрофен
Метамизол натрия (анальгин) наиболее часто применяется в послеоперационном периоде для снижения интенсивности болей внутримышечно и подкожно, (а иногда и внутривенно) в инъекциях. Используются также таблетированные формы, в состав которых входит метамизол натрия – седалгин, пенталгин, баралгин.
3. Применение местных анестетиков
Кроме используемых для местной инфильтрационной и проводниковой анестезии растворов для обезболивания инъекций, пункций и других болезненных процедур применяются анестетики контактного действия, такие как: тетракаиновый крем, инстиллагель, крем EMLA, лидокаин.
Хорошо зарекомендовал себя метод перидурального введения местного анестетика при выхаживании больных, оперированных по поводу травм живота и гнойного перитонита.
-Профилактика послеоперационной пневмонии
Риск развития послеоперационной пневмонии наиболее высок у оперированных больных, находящихся длительное время в неподвижном состоянии, а также у больных, находящихся на искусственной вентиляции лёгких и у больных с трахеостомой. Наличие у больного назогастрального зонда также может привести к инфицированию дыхательных путей.
Поэтому при длительной искусственной вентиляции лёгких приходится регулярно проводить санацию дыхательных путей, промывая их растворами соды, ферментов, или антисептиков и удаляя скопившуюся мокроту электроаспиратором.
При наличии у больного трахеостомы также периодически проводят санацию дыхательных путей с удалением мокроты электроаспиратором, а также регулярно заменяют загрязнённую канюлю трахеостомической трубки новой стерилизованной.
Для профилактики застойной пневмонии необходима регулярная смена положения больного в постели. По возможности больного необходимо как можно раньше поднимать в кровати, сажать, проводить с ним занятия лечебной физкультурой. По возможности рекомендуется также раннее вставание больного и ходьба.
Дыхательная гимнастика у послеоперационных больных включает в себя периодические глубокие вдохи, надувание пластиковых или резиновых баллонов, или игрушек.
-Тромбоэмболии
Очень грозным осложнением операций у больных пожилого возраста являются тромбоэмболии сосудов сердца, лёгких, мозга. Эти осложнения могут привести к смертельному исходу в кратчайшие сроки. Тромбоэмболиям способствуют нарушения свёртывающей системы крови у пожилых людей, повышение вязкости крови. Необходим постоянный контроль за коагулограммой в послеоперационном периоде у пожилых больных. При возникновении тромбозов и эмболий необходимо быть готовым к введению тромболитиков – фибринолизина, стрептокиназы, гепарина. При тромбоэмболиях периферических сосудов применяют зондирование сосудов с удалением тромба, либо оперативное удаление тромба. При развитии тромбофлебитов применяют местно гепариновую мазь, трокснвазин, троксерутин.
-Послеоперационные кровотечения
Кровотечения в могут возникнуть в раннем послеоперационном периоде из за соскальзывания лигатуры (узла ) с перевязанного сосуда, из за отрыва тромба с сосуда в ране. При небольших кровотечениях бывает достаточным применение холода местно, гемостатической губки, тугой повязки. При обильных кровотечениях требуется их остановка. Так: при кровотечениях из операционной раны требуется наложение повторно лигатуры, либо дополнительное ушивание раны.
Обильные внутренние кровотечения в раннем послеоперационном периоде смертельно опасны. Они часто связаны с недостаточным интраоперацион-ным гемостазом и соскальзыванием лигатуры с кровеносного сосуда.
Кровотечения в позднем послеоперационном периоде чаще развиваются из за гнойного расплавления тканей в ране, распада опухолевой ткани, несостоятельности швов. Остановка поздних послеоперационных кровотечений нередко требует повторной экстренной операции.
В позднем послеоперационном периоде развиваются такие осложнения, как нагноение послеоперационной раны, развитие пролежней, развитие спаечной кишечной непроходимости, рецидивы заболевания ( грыж, опухолей, варикоцеле, свищи.
-Нагноение послеоперационной раны
К развитию гнойного воспаления послеоперационной раны могу привести такие факторы, как:
1. Микробная контаминация операционной раны.
2. Массивное разрушение тканей в районе операционной раны.
3. Нарушение трофики тканей в области операционной раны.
4. Наличие у оперированного больного сопутствующих воспалительных заболеваний (ангины, фурункулы, пневмония ит. п. )
Клинически нагноение послеоперационной раны проявляется развитием покраснения, нарастанием болезненности, припухлостью, местным повышением температуры в области раны. Иногда определяется флюктуация ( зыбление, размягчение) в области раны.
Необходимо снять швы, выпустив гной, провести дренирование раны. Проводятся перевязки, антибактериальная терапия, промывание раны антисептиками.
-Спаечная кишечная непроходимость
После операций на брюшной полости при перитоните, остром аппендиците, травмах брюшной полости могут развиваться множественные спайки между кишками, кишечником и брюшиной. Спайки могут приводить к нарушению перистальтики кишечника и развитию полной кишечной непроходимости. Спаечная кишечная непроходимость проявляется интенсивными болями в животе, многократной рвотой, отсутствием кала и газов, требует экстренного оперативного лечения.
-Рецидивы заболеваний
Повторное развитие хирургического заболевания после оперативного лечения встречается при таких заболеваниях, как грыжи, опухоли, гнойные свищи и связаны либо с недостаточно тщательным выполнением операции, либо с особой тяжестью заболевания. При возможности повторное оперативное лечение рецидивов грыж, опухолей, свищей ит. п.
-Особенности ухода за пациентами после различных хирургических операций.
1. Уход за больным после операции на органах грудной полости
-Строгий постельный режим.
-Полусидячее положении в постели.
-Ингаляции увлажнённого кислорода.
-Контроль за герметичностью дренажей.
-Контроль за работой клапана при пассивной аспирации плевральной полости по Бюлау.
-Определять количество и характер отделяемого по плевральным дренажам.
-Внутривенное введение кровезаменителей и препаратов крови.
-Введение обезболивающих: анальгетиков, или наркотиков.
-Контроль за внутривенным катетером, периодическое промывание катетера с раствором гепарина..
-Перевязки раны.
-Антибиотикотерапия.
-Кормление больного.
-Гигиенический уход за кожей, полостью рта.
-Обеспечение дефекации, уринации.
-Периодический рентгенологический контроль.
-Проведение анализов крови с контролем гемоглобина, эритроцитов, гематокрита.
-Контроль за температурой тела, артериальным давлением, частотой пульса, частотой дыхательных движений.
-Уход за больным после операции по поводу перитонита
-Строгий постельный режим.
-Голод.
-Удаление содержимого желудка посредством постоянного назогастрального зонда.
-Положение Фаулера в функциональной кровати.
-Введение обезболивающих: анальгетиков, наркотиков.
2. Антибиотикотерапия.
-Внутривенное капельное введение кровезаменителей, препаратов крови, парентеральное питание.
-Уход за внутривенным (периферическим, или центральным) катетером.
-Уход за дренажами: периодические перевязки, при необходимости промывание.
-Контроль за количеством и характером отделяемого по дренажам.
3. Перевязки операционной раны.
-Уход за свищами (при наличии колостомы, гастростомы, интубации кишечника)
-При наличии катетера в перидуральном пространстве периодическое введение анестетика.
4. Ингаляции увлажнённого кислорода.
-Катетер в мочевом пузыре для определения функции почек.
-Общие анализы крови, мочи, биохимические анализы крови.
-Контроль за температурой тела, частотой пульса, артериальным давлением, частотой дыхания
-Уход за больным после операции по поводу гнойной хирургической патологии.
5. Изолировать от «чистых» хирургических больных.
-Антибактериальная терапия (антибиотикотерапия, нитрофураны, сульфаниламиды)
Обезболивающие, снотворные.
-Иммобилизация поражённого участка тела, конечности…
-Перевязки, смена промокших повязок, при необходимости замена дренажей.
-Внутривенное введение кровезаменителей, препаратов крови, дезинтоксикационных препаратов.
-Введение обезболивающих, снотворных.
-Контроль за общими анализами крови, мочи.
-Контроль за температурой тела, частотой пульса, дыхания, артериальным давлением.
6. Уход за урологическим больным
-Перевязки, смена промокших повязок.
-Антибиотикотерапия.
-Введение обезболивающих, спазмолитиков или наркотиков.
-Уход за надлобковым дренажом (эпицистостомой), поясничным дренажом (нефростомой, пиелостомой).
-При необходимости промывание дренажей антисептиками.
-Введение мочегонных (при необходимости)
-Контроль за диурезом
-Общие анализы мочи, крови.
-Контроль за температурой тела, пульсом, артериальным давлением
-Уход за больным после онкологической операции.
-Обезболивающие при болях.
-Перевязки операционной раны.
-При наличии свищей уход за свищами.
-Химиотерапия, лучевая терапия по назначению онколога
-Исключение физиотерапевтических процедур, массажа.
-Парентеральное питание при невозможности обычного питания.
-Оптимистический настрой в отношениях с больным.
-Щадящая информация о характере опухоли.
7. Оксигенотерапия
Для борьбы с гипоксией у послеоперационных больных применяются ингаляции кислорода. Из-за токсичности чистого кислорода его дают больным в виде газовой смеси с воздухом концентрации 40 – 60%.
Ингаляции кислорода проводят с помощью лицевой маски, носового катетера, носовой канюли. Может использоваться для кислородотерапии также тенты-палатки и эндотрахеальные трубки.
Общий уход за больными в раннем послеоперационном
периоде включает:
- контроль состояния больного;
- введение лекарственных препаратов согласно листу назначений;
- применение мочеприемников и судна для больных с постельным
режимом;
- контроль отделяемого по дренажам;
- уход за катетером для отведения мочи;
- кормление, транспортировка больных;
- уход за кожными покровами, смена нательного и постельного белья;
- профилактика возникновения пролежней (изменение положения
больного, обработка камфорным спиртом мест наиболее частого
возникновения пролежней);
- контроль состояния операционной раны: обильное промокание
повязки кровью, расхождение краев раны, выхождение органов
брюшной полости в рану (эвентрация), обильное промокание повязки
гноем, кишечным содержимым; контроль отделяемого по дренажам;
- обработка послеоперационных ран, асептические, мазевые повязки;
- в зависимости от характера оперативного вмешательства выполнение
тех или иных манипуляций согласно назначениям врача - уход за
колостомой, активизация больного, зондовое питание и др.
№15.
Доброкачественные и злокачественные опухоли. Критерии злокачественности опухолей
I. Абсолютный критерий – влияние опухоли на жизнедеятельность организма в целом (этот признак нашёл отражение в определении доброкачественных и злокачественных опухолей).
II. Относительные критерии:
1. Характер роста опухоли (доброкачественные опухоли растут, как правило, экспансивно; злокачественные, как правило, – инвазивно). Некоторые доброкачественные опухоли растут инвазивно (например, фиброматозы), а ряд злокачественных опухолей отличается экспансивным ростом (например, некоторые зрелые интракраниальные опухоли). Если медленный инвазивный рост зрелой доброкачественной опухоли вызывает разрушение соседних нормальных тканей, то такая опухоль называется доброкачественной опухолью с местно-деструирующим ростом (например, амелобластома).
2. Метастазирование (доброкачественные опухоли, как правило, не метастазируют; злокачественные, как правило, – метастазируют). Некоторые доброкачественные опухоли могут метастазировать (лейомиома матки иногда метастазирует в лёгкие, пигментные невусы – в регионарные лимфоузлы), в то время как некоторые злокачественные опухоли не метастазируют (такие опухоли называют злокачественными опухолями с местно-деструирующим ростом, например, базальноклеточная карцинома кожи).
3. Степень зрелости опухоли (доброкачественные опухоли, как правило, зрелые; злокачественные, как правило, – незрелые). Однако некоторые доброкачественные опухоли являются незрелыми, например, ювенильный невус (ранее называвшийся ювенильной меланомой) образован незрелыми пигментными клетками с признаками выраженного клеточного атипизма. Ряд злокачественных опухолей, напротив, отличается зрелой структурой (так, все зрелые опухоли в полости черепа, достигая определённой величины, становятся злокачественными).
ЭТИОЛОГИЯ ЗЛОКАЧЕСТВЕННЫХ ОПУХОЛЕЙ
Общей причиной злокачественного роста является недостаточность системы антибластомной резистентности (системы противоопухолевой защиты), основными элементами которой являются ферменты репарации ДНК, антионкогены (например, р53) и ЕК-клетки (естественные киллерные клетки). К недостаточности системы антибластомной резистентности приводят интенсивное канцерогенное воздействие, иммунодефицитные состояния, недостаточность ферментов репарации ДНК и функции антионкогенов, а также рубцовое уплотнение ткани («рак в рубце»).
Интенсивное канцерогенное воздействие. Различают травматический, термический, радиационный, химический и вирусный варианты канцерогенеза.
1. травматический канцерогенез – развитие злокачественной опухоли в месте травмы (например, хроническая травма красной каймы губ может привести к развитию рака).
2. термический канцерогенез – развитие злокачественной опухоли в местах длительного дозированного воздействия высокой температуры (в местах ожогов, например, рак слизистой оболочки полости рта и пищевода у любителей горячей пищи).
3. радиационный канцерогенез – развитие незрелой злокачественной опухоли при воздействии ионизирующих или неионизирующих излучений в канцерогенной дозе. Основным природным канцерогеном для лиц европеоидной и монголоидной рас является солнечный ультрафиолет, поэтому привычка загорать на солнце способствует развитию злокачественных новообразований кожи.
4. химический канцерогенез – развитие незрелых злокачественных опухолей под влиянием химических канцерогенов (канцерогенных веществ). Из экзогенных химических канцерогенов основную роль играют канцерогены табачного дыма, являющиеся основной причиной развития рака лёгкого и рака гортани. Среди эндогенных химических канцерогенов важное значение имеют эстрогенные гормоны (высокий уровень которых приводит к развитию рака молочных желёз, яичников, эндометрия) и канцерогенные метаболиты холестерина, образующиеся в толстой кишке под влиянием микроорганизмов и способствующие развитию рака толстой кишки.
5. вирусный канцерогенез – индукция злокачественных опухолей вирусами (онкогенные вирусы). Онкогенными называют только те вирусы, которые непосредственно вызывают малигнизацию клетки, привнося в её геном онкогены (вирусные онкогены). Некоторые вирусы способствуют развитию злокачественных опухолей косвенно, обусловливая фоновый патологический процесс (например, вирусы гепатитов В, С, D, не являясь онкогенными, способствуют развитию рака печени, вызывая цирроз). Наиболее важными окогенными вирусами человека являются симплекс-вирус (вирус простого герпеса) II типа из семейства Herpesviridae (вызывает рак шейки матки, рак полового члена и, возможно, ряд других опухолей); вирус герпеса VIII типа (приводит к развитию саркомы Капоши); вирус папилломы человека из семейства Papovaviridae (вызывает рак шейки матки и рак кожи); вирус Эпштейна–Барр из семейства Herpesviridae (вызывает злокачественные опухоли в основном в странах с жарким климатом – лимфому/лейкоз Беркитта [Burkitt], наиболее распространённые в Африке, рак носоглотки в Юго-Восточной Азии и, возможно, другие опухоли).
волосовидноклеточный лейкоз (hairy cell leukaemia).
«Рак в рубце». У человека самыми частыми формами «рака в рубце» являются рак, развивающийся в трофических язвах кожи, периферический рак лёгкого, рак из хронической язвы желудка и ДПК, первичный рак печени на фоне цирроза.
ПАТОГЕНЕЗ, МОРФОГЕНЕЗ И ПУТИ
ЭВОЛЮЦИИ ЗЛОКАЧЕСТВЕННЫХ ОПУХОЛЕЙ
Выделяют четыре основные стадии развития незрелых злокачественных опухолей: стадии малигнизации, прединвазивной опухоли, инвазии и метастазирования.
1. Стадия малигнизации – трансформация нормальной клетки в злокачественную (на первом этапе – этапе инициации – происходит соматическая мутация, в результате которой в геноме малигнизирующихся клеток появляются онкогены; на втором – этапе промоции- (повышение)– начинается пролиферация инициированных клеток). Онкогенами (onc) называют любые гены, непосредственно вызывающие трансформацию нормальной клетки в злокачественную или способствующие этому превращению. Онкогены в зависимости от их происхождения делят на две группы: клеточные онкогены (c-onc) и вирусные онкогены (v-onc). Клеточные онкогены формируются из нормальных генов клетки, получивших название протоонкогенов. Типичным примером клеточного онкогена является ген белка р53 – ген нормального («дикого») р53 играет роль одного из активных антионкогенов; его мутация приводит к образованию онкогена (ген «мутантного» р53). Продукты экспрессии онкогенов называются онкопротеинами (онкобелками).
2. Стадия прединвазивной опухоли – состояние незрелой злокачественной опухоли до начала инвазии (в случае рака для этой стадии использовался термин carcinoma in situ).
3. Стадия инвазии – инвазивный рост злокачественной опухоли.
4. Стадия метастазирования.
+Морфогенез злокачественных опухолей.
1. Развитие опухоли de novo («скачкообразная» эволюция), – без предшествующих видимых преопухолевых изменений.
2. Стадийный канцерогенез – развитие опухоли на месте предопухолевых изменений (в случае рака для обозначения предопухолевых изменений используется термин предрак).
Выделяют две формы предрака:
1. облигатный предрак – предрак, рано или позно обязательно трансформирующийся в рак (например, изменения кожи при пигментной ксеродерме),
2. факультативный предрак – предрак, необязательно трансформирующийся в рак (например, лейкоплакия).
Пути эволюции злокачественных опухолей.
1. Прогрессия опухоли – усиление с течением времени её злокачественного потенциала.
2. Регресс опухоли (редкое явление) – спонтанное (без лечения) исчезновение опухоли.
Принципы деонтологии в онкологии.
Два принципиальных положения определяют тактику врача по отношению к онкологическому больному:
1) оптимальное использование диагностических процедур и лечебной помощи должно осуществляться с максимальным щажением психики больного,
2) каждый больной злокачественной опухолью подлежит лечению.
Обследование заболевших должно быть адекватным. Не имеет смысла добиваться гистологического подтверждения диагноза у больных, которым из-за тяжелого состояния не может быть оказана лечебная помощь.
Следует отказаться от использования сложных современных методов исследования, если точный диагноз может быть установлен с помощью более простых приемов.
Начиная с периода обследования, онкологические больные находятся в подавленном состоянии. У них наблюдается эмоциональный стресс, проявляющийся выраженными признаками тревоги и депрессии. В таком состоянии возможны неадекватные реакции, выражающиеся в отказе от лечения и даже в попытках покончить жизнь самоубийством.
Задача врача заключается в том, чтобы успокоить больного и психологически подготовить к предстоящему лечению, внушив ему веру в излечимость заболевания. При этом сообщать больному о наличии у него рака или другой злокачественной опухоли с сомнительным исходом не следует. Чем больше пациент настаивает, чтобы ему открыли правду, тем больше он ее боится. Исключение может быть сделано лишь при недооценке больным серьезности положения и отказе от обследования и лечения. Но даже в таких случаях желательно избегать терминов “рак”, “саркома ”.
С деонтологических позиций нельзя допускать, чтобы в руки больного попадала медицинская документация и данные, подтверждающие диагноз злокачественного новообразования. Следует соблюдать предельную осторожность при разговорах по телефону о больном, анализе рентгенограмм и результатов специальных исследований в присутствии больного и т. д.
Типы высшей нервной деятельности и реакция больных. Реакция онкологических больных в процессе обследования и лечения зависит от типа высшей нервной деятельности.
С а н г в и н и к - оптимист, он понимает необходимость и легко переносит диагностические и лечебные процедуры, верит в успех лечения.
Ф л е г м а т и к стеснителен, мало жалуется, не любит задавать вопросов, не углубляется в результаты обследования. Он дисциплинирован, с уважением относится к рекомендациям врача. Необходимость обследования и лечения принимает без возражений.
С сангвиниками и флегматиками врачу разговаривать нетрудно, тем не менее говорить им о наличии злокачественной опухоли без особой необходимости не следует.
Гораздо сложнее беседа с людьми холерического или меланхолического темперамента.
X о л е р и к бурно реагирует, но легко переходит от энергичных действий к подавленному состоянию. Принимает быстрые решения. Может сразу категорически отказаться от обследования и лечения или наоборот требовать ускоренного производства назначенных процедур. Обычно это не очень дисциплинированный больной, который часто не верит в возможное излечение и может вести себя агрессивно по отношению к врачу и другому медицинскому персоналу.
В разговоре с таким больным врач должен проявить особое внимание, сохранить полное спокойствие и рассудительность. Больной должен почувствовать хорошее, доброжелательное отношение врача, понять, что врач от души старается помочь ему.
М е л а н х о л и к - мнительный человек, часто обладающий поверхностными сведениями негативного характера о злокачественных опухолях. Он стремится выяснить результаты каждого исследования, акцентирует внимание и дает неправильное толкование любым отклонениям от нормы. Предположение о злокачественной опухоли вызывает у него паническое состояние, в возможность излечения он не верит. В процессе разговора он внимательно следит за мимикой врача, ловит каждое слово, отыскивая в нем опасное подтверждение своих предположений.
Такому больному ни в коем случае нельзя говорить о наличии злокачественной опухоли. Его нужно вызвать на доверительный разговор, в процессе которого врач должен спокойным, уверенным тоном разъяснить больному ошибочность его представлений.
Больного следует убедить в том, что направление на консультацию к онкологу продиктовано необходимостью уточнения степени опасности имеющейся у него язвы, уплотнения или затемнения, с целью исключения злокачественного новообразования.
Характер предстоящего лечения обсуждать не следует. Если больной прямо ставит об этом вопрос, нужно сказать, что выбор метода лечения будет сделан в зависимости от результатов обследования в стационаре.
Взаимоотношения врача с онкологическим больным должны строиться на основе сочувствия и внимания. Задачи, стоящие перед врачом, меняются в зависимости от категории больных.
Больные с подозрением на рак. При подозрении на рак возможны две различные ситуации. В большинстве случаев предположение о раке и необходимость обследования в онкологическом учреждении возникает, если у больного в течение некоторого времени сохраняются стойкие симптомы какого-либо заболевания, вызывающие тревогу у самого больного. Таких больных следует ориентировать на необходимость консультации онколога для исключения злокачественной опухоли.
В других случаях подозрение на рак возникает случайно при профилактическом осмотре или обследовании человека, чувствующего себя хорошо и не предъявляющего серьезных жалоб. Для таких людей направление к онкологу является неожиданным и непонятным. Им следует объяснить, что при обследовании обнаружен инфильтрат, затемнение или язва, которые могут оказаться предопухолевыми, в связи с чем необходима консультация онколога.
Онкологические больные, подлежащие специальному лечению. Перед врачом стоит задача направить больного в онкологическое учреждение и психологически подготовить его к мысли о возможности операции или другого специального лечения. Система убеждений может быть построена по такому же принципу, что и при подозрении на рак, но в дополнение к этому следует остановиться на возможности оперативного или лучевого лечения. Говорить об этом как о бесспорном факте нецелесообразно, так как из-за распространенности процесса или сопутствующих заболеваний такое лечение в специализированном учреждении может быть отвергнуто. Лучше ориентировать больного на то, что окончательное решение о выборе метода лечения будет принято специалистом после дополнительного обследования.
На практике встречаются случаи, когда врач в силу недостаточной подготовки или случайно приобретенного отрицательного личного опыта негативно относится к лечению той или иной злокачественной опухоли. Недопустимо, чтобы эта отрицательная установка вольно или невольно индуцировалась больному.
Мотивы отказов от лечения. Несмотря на значительные усилия, прилагаемые врачами для убеждения больных, последние порою отказываются от лечения. Можно выделить четыре наиболее часто встречающиеся мотивы отказов.
Страх перед предстоящим лечением. Больной понимает необходимость лечения, но боязнь операции настолько велика, что он не находит мужества подвергнуться ей. Врач должен выяснить причину страха. У пожилых больных боязнь за исход операции может быть обусловлена сопутствующими или перенесенными заболеваниями сердца или других органов. Игнорировать такие опасения нельзя. Нужно, не затягивая времени, провести обследование и по возможности начать в амбулаторных условиях коррекцию имеющихся нарушений. Лицам с повышенной возбудимостью целесообразно назначить лечение бромидами, нейроплегиками, транквилизаторами. Больному следует разъяснить, что в стационаре перед решением вопроса об операции ему проведут соответствующее лечение, которое обеспечит безопасность оперативного вмешательства.
Больные нередко отказываются от калечащих операций с удалением конечности, молочной железы и др. Их пугает последующее неполноценное существование. Такие переживания обоснованны, они вызывают всяческое сочувствие. Но поскольку иной возможности излечения нет, врач, стараясь не раскрывать истинного характера заболевания, должен убедить больного в необходимости оперативного вмешательства. Наряду с этим следует максимально смягчить тревогу больного по поводу дальнейшего существования.
Иногда это удается путем убеждения в необходимости сохранить жизнь и здоровье для блага семьи и детей, в других случаях решающим оказывается объяснение характера работы, которую сможет выполнять заболевший, или разъяснение, каким путем другим больным удается скрыть от окружающих имеющийся дефект.
Мотивом отказов может явиться неверие больного в возможность излечения. Такое состояние чаще бывает у людей, тем или иным путем узнавших о наличии злокачественной опухоли и считающих эту болезнь неизлечимой. Иногда они основываются на случайных наблюдениях за лицами, погибшими от такого же злокачественного новообразования. Такие больные, как правило, нахолятся в подавленном состоянии. С ними должна быть проведена спокойная разъяснительная беседа, в процессе которой нужно убедить больного, что окончательный диагноз станет ясным только после исследования препарата под микроскопом и если будет обнаружен рак, то опухоль, безусловно, окажется в ранней стадии, когда она может быть полностью излечена. В то же время отказ от лечения и потеря времени приведут к распространению процесса и тогда возможность излечения станет сомнительной.
Причиной отказа может явиться необоснованное, но очень стойко сохраняющееся среди части населения представление о возможности излечиться травами или домашними, нередко ядовитыми средствами. К сожалению, об этом больные стараются врачам не говорить. Вылечить злокачественную опухоль народными средствами невозможно. Об этом свидетельствует накопленный многолетний опыт и специальные научные исследования. Сложность положения врача заключается в том, что больной ориентирован на наличие доброкачественного процесса, при котором те или иные народные средства могут использоваться.
В таких случаях следует заострить внимание больного на опасных осложнениях, указав в зависимости от пораженного органа на возможность кровотечения, перфорации, перитонита, в том числе на вероятность возникновения злокачественной опухоли. Иногда основным мотивом отказа от лечения является реакция отрицания, при которой больной в связи с хорошим самочувствием не верит в необходимость лечения.
Таким больным нужно разъяснить серьезность положения, подчеркнув, что заболевание будет прогрессировать, и объяснить, что риск операции намного меньше, чем опасность самой болезни. Если в подобных случаях приходится говорить об опухоли, то это должно быть сказано не в виде достоверности, а только как серьезное предположение. В безвыходной ситуации, если иным путем не удается побудить больного к лечению, врач может оказаться вынужденным сказать правду. В такой ситуации следует привести доказательства, что опухоль выявлена в ранней, вполне излечимой стадии.
Лица излеченные от рака. В процессе лечения ряду больных становится известен истинный диагноз. Поэтому после выписки из стационара у выздоровевших нередко наблюдается астеническое состояние, чувство тревоги, подавленности, повышенной мнительности. Излечение от рака не излечивает от страха перед ним. Повышенная мнительность ведет к тому, что всякое нарушение самочувствия человек склонен расценивать как признак метастазов. Легкое недомогание, подкожные липомы и фибромы, уплотнение послеоперационных рубцов, кожные высыпание трактуются как рецидив заболевания.
К предъявляемым больными жалобам нужно относиться в высшей степени серьезно. Следует произвести тщательный осмотр, а иногда прибегнуть к консультации специалиста, чтобы не пропустить рецидива или метастазов.
Подавленное состояние после лечения может привести к появлению синдрома самоизоляции, который проявляется потерей интереса к жизни, ощущением одиночества, затрудненным общением с семьей и окружающими. Иногда синдром самоизоляции бывает настолько выражен, что приводит больного к суицидальным попыткам.
Перед врачом стоит задача добиться, чтобы депрессия уступила место синдрому вытеснения болезни, т. е. чтобы излеченный либо отвергал диагноз злокачественной опухоли, либо перестал придавать ему значение.
В этом отношении большую помощь оказывает благоприятная обстановка в семье. Участковый врач должен обсудить с родственниками оптимальную линию поведения. В отношениях с больным они должны избегать как чрезмерной опеки, так и упреков в мнительности при наличии жалоб. Это особенно важно в первые месяцы после излечения больного.
Не менее существенно своевременно и адекватно решить вопрос о трудоустройстве больного. Обычно после излечения от рака внутренних органов и молочной железы больные в течение некоторого времени нетрудоспособны. Продолжительность пребывания на инвалидности зависит от характера проведенного лечения и состояния больного. Своевременное разрешение выполнять определенные виды работ нередко оказывает весьма благотворные влияние, убеждая больного в реальности выздоровления.
Больные с запущенными формами рака. Принципиальной установкой является положение о том, что инкурабельных онкологических больных не существует. Больные с запущенными формами злокачественных опухолей подлежат паллиативному или симптоматическому лечению. Его осуществляют врачи широкого профиля по месту жительства больного. План лечения должен быть согласован с онкологом. При необходимости стационарного лечения больного госпитализируют в общесоматические стационары.
С деонтологических позиций больных с запущенными формами рака можно разделить на три категории, требующие различного подхода.
Цель, которую преследует врач в беседе с родственниками, зависит от конкретной ситуации. Так, если у больного впервые обнаружен рак, родственники должны помочь убедить его в необходимости лечения. Задачей родственников лиц, излеченных от рака или страдающих запущенными формами опухоли, является создание оптимального микроклимата в семье и внушение больному надежды на благоприятный исход.
Родственников часто интересует возможная продолжительность жизни больных с запущенными формами рака. Указывать, даже ориентировочно, какие-либо сроки не следует. Конкретный ответ в такой ситуации тяжело воспринимается родными, а естественная ошибка в ту или иную сторону роняет авторитет врача.
Канцерофобия - навязчивое состояние, выражающееся в необоснованном убеждении о наличии злокачественной опухоли. Встречается чаще у женщин. Страдают канцерофобией люди, родственники или знакомые которых заболели или умерли от рака. В других случаях она навеяна сходством имеющихся у больных патологических ощущений или объективных симптомов с известными им признаками злокачественных новообразований.
Больные канцерофобией, как правило, находятся в состоянии депрессии, иногда возбуждены, агрессивны. Утверждение врача об отсутствии у них опухоли воспринимают с недоверием, расценивают как признак недостаточной компетенции врача или как намеренно невнимательное отношение.
Предположение о наличии канцерофобии возникает, если больные на амбулаторном приеме слишком эмоционально и убежденно утверждают о наличии у них злокачественного новообразования. В таких случаях у врача нередко наблюдается неосознанная негативная реакция. С заключением нужно быть весьма осторожным, так как жалобы больных иногда действительно обусловлены злокачественной опухолью. Не следует сразу пытаться разубеждать больного, лучше сначала получить достаточно веские контраргументы. На диагнозе “канцерофобия” можно остановиться только после того, как опухоль полностью исключена в результате всестороннего обследования.
Вызов консультанта. Необходимость приглашения консультанта к онкологическому больному возникает по разным причинам. Вызов консультанта с целью установления окончательного диагноза или убеждения больного в необходимости лечения безусловно оправдан. Обоснованным является приглашение онколога для выработки тактики симптоматического лечения или для психологического воздействия на больных с запущенными злокачественными опухолями. В некоторых случаях к помощи консультанта приходится прибегать у лиц с канцерофобией, если лечащему врачу не удается разубедить их в наличии рака. В далеко зашедших случаях, если консультант не может дать дополнительных рекомендаций по лечению или оказать психологическое воздействие на больного, приглашение его нецелесообразно. Такая консультация окончательно отнимает у больного веру в возможность благоприятного исхода и усугубляет состояние обреченности.
Общие требования к студентам. Существуют строгие деонтологические правила, которых должен придерживаться студент во время пребывания в онкологической клинике.
Студент не должен являться для больного источником неблагоприятной информации. Он не имеет права говорить больному о диагнозе, о сомнительном или неблагоприятном прогнозе. Следует помнить, что все сведения о диагнозе, методах лечения и прогнозе могут исходить только от лечащего врача. Студент не должен сообщать конкретных данных о результатах исследований, демонстрировать больным рентгеновские снимки, сканограммы и т. д. Это может создать у больного превратное представление об имеющихся у него нарушениях и затруднить работу врача с больным. Имея доступ к медицинской документации, студент должен исключить возможность ознакомления больного с историей болезни и другими медицинскими документами.
1. Первичные больные, у которых отдаленные метастазы и запущенность процесса обнаружены во время обследования в поликлинике. От таких больных часто удается скрыть истинный диагноз и прогноз заболевания. При этом заявление лечащего врача или онколога о том, что нет необходимости в специальном лечении в онкологическом диспансере, больной рассматривает как доказательство, что диагноз рака отвергнут. Перед врачом стоит задача убедить больного в наличии другого, неонкологического заболевания и в том, что назначенное лечение, проводимое достаточно упорно в течение длительною времени, приведет к выздоровлению.
Безосновательное направление таких больных в онкологический диспансер является грубым нарушением деонтологических правил. Больной воспринимает это как подтверждение диагноза злокачественной опухоли, а невозможность лечения в диспансере как признак неизлечимости процесса.
2. Больные, у которых запущенность установлена после обследования или лечения в стационаре. Таких больных сориентируют на наличие какого-либо неонкологического заболевания. В зависимости от результата проведенного лечения больному говорят, что заболевание либо излечено, либо подлежит дальнейшему лечению по месту жительства. Районный онколог и участковый врач должны знать, как ориентирован больной, и придерживаться той же версии. Это удается выяснить из справки, выданной на руки больному, при беседе с родственниками или с самим больным. В затруднительных случаях следует связаться с врачом онкологического учреждения, лечившим больного.
3. Больные с рецидивами и метастазами после проведенного ранее радикального лечения. Эти люди больше контактируют с наблюдавшим их онкологом и полагаются на его заключение. Он избирает деонтологически оправданный вариант объяснений, которого следует придерживаться участковому врачу.
Информирование родственников. Врач не имеет права разглашать сведения об онкологическом больном посторонним лицам. Исключение делается лишь для родственников и наиболее близких больному людей. Ближайшие родственники должны быть поставлены в известность об истинной природе заболевания и его прогнозе. Разговор с ними должен проходить в отсутствие больного. Их следует предупредить о нежелательности огласки сведений о характере заболевания и проинструктировать о том, какой версии следует придерживаться в разговоре с больным.
Родственников нужно информировать объективно, но по возможности оставить надежду на благоприятный исход. Это особенно важно в разговоре с людьми, которые отличаются повышенной возбудимостью или сами страдают заболеваниями нервной, сердечно-сосудистой и других систем.
Доклады на обходах. Докладывая о больных, запрещается в палате употреблять термины “злокачественная опухоль”, “рак”, “саркома”, “метастазы” и т. д. Вместо них используют мало значащие для непосвященного слова: “заболевание”, “органическая патология”, “затемнение” или называют то заболевание, на которое ориентировал больного лечащий врач.
Больные очень внимательно прислушиваются не только к сообщаемым во время обхода сведениям, но даже к интонации голоса докладывающего. Доклад о больном должен быть кратким, но в то же время четким и ясным. В нем нужно отразить жалобы, основные данные из анамнеза, результаты исследований, подтверждающие диагноз, характер планируемого или выполненного лечения, течение и особенности послеоперационного периода
Нельзя на обходах заострять внимание на ошибках врачей, допущенных до поступления больного в клинику, выражать сожаление, что больной поздно обратился за помощью, говорить о плохом качестве рентгеновских снимков и т. д. Все сведения, о которых больной не должен быть информирован, докладываются вне палаты.
Курация больных. В процессе общения с курируемым больным перед студентом стоит задача помочь врачу успокоить больного. Важно учитывать, что период пребывания в стационаре характеризуется многочисленными влияниями на психику больного со стороны окружающих. Обширный поток информации, нередко отрицательного характера, - может вызвать у больного неуверенность, нервозность, подавленное состояние.
+Неряшливый внешний вид, мятый и грязный халат, бестактное поведение, громкие разговоры или смех вызывают отрицательные эмоции у больных и препятствуют установлению контакта с ними.
Студент должен понимать психологию онкологического больного, уметь своевременно заметить и поставить в известность лечащего врача обо всех отклонениях от нормы в реакции больного на ту или иную ситуацию, попытаться успокоить больного.
Информировать родственников о характере заболевания, предполагаемом лечении и прогнозе студент не имеет права. По этим вопросам студент должен направить родственников к лечащему врачу.
Стадии злокачественных опухолей
1-я стадия: образование небольшого размера, расположена на ограниченном участке, не прорастает в стенку соседнего органа, не имеет метастазов.
2-я стадия: образование большого размера, не выходит за пределы органа, возможно наличие одиночных метастазов в регионарные лимфатические узлы.
3-я стадия: образование большого размера, с участком распада, прорастает сквозь всю стенку органа; либо образование небольших размеров с наличием множественных метастазов в регионарных лимфатических узлах.
4-я стадия: опухоль проросла в окружающие ткани, в том числе в те, которые невозможно удалить хирургическим путем (аорта, полая вена и др. ); либо любая опухоль с отдаленными метастазами.
Меланома – поражение кожных покровов
Лейкоз – образование в кроветворной системе
Карцинома – поражение эпителиальной ткани органа
Лимфома– поражение лимфатической системы
Саркома – злокачественная опухоль в нервной, соединительной или опорной ткани тела
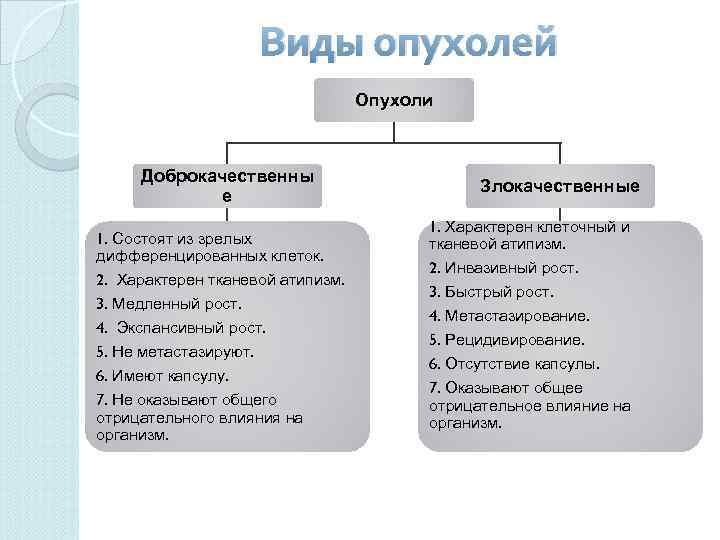
№16.
Симптомы рака молочной железы
Рак груди — это системное заболевание. Он не только разрушает ткани, непосредственно пораженные опухолью, но и разрушительно действует на весь организм в целом. Поэтому и признаки рака груди могут быть связаны не только с пораженным органом, но и с общими симптомами в виде похудения, общей слабости.
В то же время, нередки случаи, когда в начале заболевания опухоль никак не дает о себе знать. В такой ситуации от врача требуется детально знать симптомы рака груди, чтобы выявить болезнь, пока она не перешла в запущенную стадию. Большую ценность имеют инструментальные обследования, такие, как маммография, УЗИ молочных желез или МРТ (в сложных случаях). Женщинам средних лет следует обследоваться регулярно.
Обратиться к врачу нужно при появлении следующих признаков рака груди:
• любое опухолевое образование в груди;
• изменился внешний вид или форма груди;
• из сосков есть выделения:
• изменилась форма соска или ареолы;
• кожа груди покраснела, стала слишком морщинистой или отекает;
• на груди заметны участки со втянутой кожей.
Любой из перечисленных признаков рака груди должен стать поводом для того, чтобы пройти обследование молочных желез. При дальнейшем развитии заболевания симптомы усугубляются, если пациентка не получает должного лечения. Форма груди может существенно искажаться. Появляются признаки интоксикации организма продуктами жизнедеятельности раковых клеток, а метастазы поражают и другие органы. Возникает боль при движении рукой с той стороны, которая поражена опухолью. В запущенных случаях на поверхности кожи груди появляются незаживающие язвы.
Патогенез рака молочной железы
Часто рак груди относится к категории аденокарцином. Так называют опухоли из железистого эпителия. В данном случае это клетки, которые выстилают протоки молочных желез. Внутри них и развивается опухоль, постепенно разрастаясь и захватывая все большее количество тканей. Сначала кожа груди становится морщинистой или втянутой, но если поражение более серьезно, внутренние слои кожи разрушаются, появляется синдром «апельсиновой корки», а затем происходит изъязвление кожного покрова.
Метастазы рака груди распространяются по организму через лимфатическую и кровеносную систему. Прежде всего страдают лимфатические узлы, которые находятся вблизи от пораженных участков (подмышечные, подключичные, надключичиные). Опухоли часто метастазируют в легкие, печень, головной мозг и кости. Врачами неоднократно зафиксированы и случаи отдаленных метастазов, например, в брюшную полость. Именно отдаленные метастазы, а не основное заболевание, нередко становятся причиной гибели пациентов, поскольку они поражают различные системы организма и нарушают их нормальное функционирование.
Характеризуя степень развития заболевания, учитывают:
• размер самой опухоли;
• состояние лимфатических узлов;
• наличие метастазов в различные органы.
Классификация и стадии развития рака молочной железы
Может отличаться и местоположение опухоли. Онкологический процесс поражает одну или обе груди, по-разному располагаясь в молочной железе, проникая в ее дольки и протоки.
У многих пациенток развивается узловой рак. Для этой разновидности характерна округлая опухоль, в которой прощупывается бугристая узелковая структура.
При диффузном раке груди (отечно-инфильтративная форма) подобной структуры не наблюдается, поскольку болезненный процесс охватывает сразу всю железу и начинается, подобно воспалительным заболеваниям груди, с покраснения, подъема температуры и т. д. Диффузный рак быстрее прогрессирует и активнее дает метастазы. Из-за этого бываю трудности с диагностикой данной формы рака.
Отдельную разновидность представляет собой болезнь Педжета. Это злокачественная опухоль, которая поражает сосок и окружающую его область кожи. Обычно оно развивается медленно, постепенно переходя на другие части молочной железы.
Принадлежность опухолевых клеток к тому или иному типу определяется в ходе гистологического исследования, когда кусочек опухолевой ткани исследуется под микроскопом. Для построения тактики лечения необходимо понять, к какому типу относится опухоль.
Выделяют следующие биологические подтипы рака груди:
• люминальный, или гормоночувствительный (HER2-позитивный и HER2-негативный);
• нелюминальный HER2-позитивный;
• трижды негативный.
Наиболее благоприятный по течению — люминальный HER2-негативный рак. В опухоли есть рецепторы к гормонам эстрогену и прогестерону. Данный тип рака отвечает на гормонотерапию, но мало восприимчив к химиотерапии.
HER2-позитивный рак груди — в опухоли есть рецепторы к человеческому эпидермальному фактору роста (HER2). Отвечает на таргетную терапию Трастузумабом.
Самый неблагоприятный по течению рак груди — трижды негативный. В опухоли нет ни гормональных рецепторов, ни рецепторов HER2.
Стадии рака груди
1. К первой стадии относят опухоли размером не больше 2 сантиметров, которые не имеют метастазов.
2. На второй стадии опухоль достигает уже пяти сантиметров. Лимфатическая система может оставаться незатронутой, но могут уже появиться и метастазы в несколько лимфоузлов.
3. На третьей стадии опухоль становится больше 5 сантиметров. Метастазы наблюдаются только в лимфоузлах, в то время как в других внутренних органах их нет.
4. Главный признак четвертой стадии — метастазы в отдаленные органы — печень, легкие, головной мозг, кости.
Осложнения рака молочной железы
Осложнения рака молочной железы могут быть связаны как с влиянием на организм самого заболевания, так и с его лечением, поскольку проведение операции, лучевая терапия или химиотерапия связаны с определенными рисками и побочными действиями. Если опухоль долгое время находится без лечения, возможно изъязвление опухоли и кровотечение из нее. На последних стадиях болезни возникают осложнения, связанные с поражением внутренних органов метастазами. Например, если поражены легкие, возникают дыхательная недостаточность, плеврит.
Оперативное лечение рака груди для многих женщин осложняется психологическими проблемами, ведь часто полное удаление молочной железы оказывается неизбежным. Нередко женщинам сложно это принять. В современной медицине разработаны стратегии борьбы с подобными проблемами, а также хорошо развито протезирование и реконструктивные операции, которые восстанавливают естественный внешний вид груди. Иногда после операции рука остается отечной из-за нарушения оттока лимфы. С этим осложнением борются с помощью специального комплекса упражнений, лимфодренажа, хирургических манипуляций по пересадке лимфоузлов или наложения новых лимфовенозных анастомозов.
После лучевой терапии и химиотерапии часто наблюдаются реакции со стороны кожи. Выпадают волосы, ногти становятся хрупкими, кожа сухая и шелушится. Эти симптомы проходят после окончания терапии, хотя организму понадобится некоторое время на восстановление. Частое осложнение химиотерапии — тошнота, снижение показателей крови – лейкоцитов, тромбоцитов. Это в свою очередь может приводить к выраженному снижению иммунитета и развитию кровотечений.
Диагностика рака молочной железы
При диагностике рака молочной железы ключевой задачей врача является выявление заболевания на начальной стадии заболевания. Своевременно проведя диагностику, можно остановить развитие опухоли еще до того, как она начнет давать метастазы в лимфоузлы и внутренние органы. В результате удастся сократить негативное воздействие на организм.
Осмотр и пальпация
Осмотр молочных желез и их пальпация позволяет врачу обнаружить ассиметрию молочных желез, изменения их формы и положения, а также изменения поверхности кожи, если они есть. Прощупывая молочные железы, врач может не только обнаружить опухоль, но и определить ее диаметр и структуру, локализовать местоположение. Также врач пальпирует лимфоузлы, чтобы определить, являются ли они увеличенными или уплотненными.
Инструментальная диагностика
Среди инструментальных методов диагностики ключевое значение имеет УЗИ (у женщин до 35 лет) и маммография (у женщин после 35 лет) — рентгенологическое исследование молочной железы. Она дает врачу точное представление о положении и размерах опухоли, позволяет увидеть, какие именно части молочной железы пострадали от опухоли. Маммография обнаруживает опухоль, когда она составляет от 0, 5 сантиметров. Это значит, что начать лечение удастся еще на первой или второй стадии заболевания.
Иногда ультразвуковое исследование позволяет выявить опухоли, которые из-за особенностей структуры остаются незаметными на маммограммах.
В сложных случаях диагностика дополняется МРТ молочных желез.
Для создания более полной картины используют и другие исследования. Чтобы определить характер опухоли, назначается биопсия — анализ взятого из опухоли клеточного материала. Галактография и дуктография позволяют проверить состояние протоков молочных желез и понять, насколько они затронуты опухолью. В качестве дополнительного диагностического метода используется УЗИ.
Окончательный диагноз злокачественной опухоли можно поставить только на основании морфологического исследования. Для этого из опухолевого узла нужно взять фрагмент тканей — биопсию — и исследовать его под микроскопом. Это позволит определить тип опухоли и подобрать верную тактику лечения. Более простым вариантом является выполнение тонкоигольной биопсии, но риск ошибочного диагноза будет выше.
Чтобы проверить наличие метастазов в отдаленных органах, необходимо выполнять рентгенологическое исследование легких, УЗИ органов брюшной полости, малого таза и периферических лимфатических узлов, радиоизотопное сканирование костей.
Лабораторная диагностика
Наиболее распространённый онкомаркер при раке груди — СА 15-3. Однако у него довольно низкая специфичность (т. е. результат бывает положительным и у здоровых женщин). Может применяться для оценки эффективности лечения.
Если какие-то симптомы уже появились, очень важно не затягивать с диагностическими процедурами, поскольку в случае агрессивной формы рака груди задержка даже на один месяц может существенно снизить шансы на успешное лечение.
Лечение рака молочной железы
Для лечения рака молочной железы, как правило, используют комплекс различных методов. Их комбинация подбирается индивидуально. Чаще всего речь идет о хирургическом лечении, которое поддерживается химической или лучевой терапией, применением гормональных препаратов и других противоопухолевых средств.
Хирургическое лечение
Хирургические операции для лечения рака груди были впервые разработаны больше века назад. С тех пор их техника неоднократно улучшалась и дорабатывалась, но суть остается прежней: хирург полностью удаляет молочную железу вместе с близлежащими лимфатическими узлами. В современной практике используются радикальная мастэктомия, квадрантэктомия и лампэктомия [8]. Все эти операции предполагают удаление молочной железы или ее части и ближайших лимфатических узлов. В дальнейшем врач может назначить реконструктивную пластическую операцию, чтобы восстановить форму груди пациентки с использованием силиконового протеза или собственных тканей. В настоящее время распространение получила онкопластическая хирургия молочных желез, которая позволяет соблюдать онкологические принципы удаления опухоли и сохранять максимально эстетичную форму груди. Кроме того, существует возможность сохранять лимфатические узлы, если они не поражены опухолью. Для этого требуется выполнить биопсию сигнального лимфоузла.
Лучевая терапия
Лучевая терапия рака молочной железы применяется до и после операции, чтобы предотвратить рецидив (повторное развитие опухоли). Она может использоваться и в качестве самостоятельного метода лечения, если операция по каким-то причинам невозможна.
Химиотерапия
Кроме того, больным назначают и химиотерапию. Выбор конкретной схемы лечения зависит от типа злокачественной опухоли и других факторов в анамнезе больного. Она нацелена и на уничтожение присутствующих в организме злокачественных клеток, и на предотвращение рецидива. Сегодня активно ведется разработка новых препаратов, которые смогут поражать только опухолевые клетки и не повреждать здоровые, в отличие от классической химиотерапии (таргетная терапия).
Западные исследователи отмечают, что поскольку в последнее время рак молочной железы становится скорее хроническим заболеванием, а не угрожающим жизни благодаря успешной ранней диагностике, на практикующих врачах лежит огромная ответственность за выбор методов лечения и их последствия для здоровья пациентки. Так, например, успешное использование больших доз синтетических эстрогенов для лечения постменопаузального рака молочной железы считается первой эффективной " химиотерапией", проверенной в клинических испытаниях для лечения различных видов рака.
Гормональная терапия
Гормонотерапия проводится при люминальном раке груди, при котором в опухоли есть рецепторы к гормонам эстрогену и прогестерону. Если лечение комплексное, то гормоны назначают после хирургического и химиотерапевтического лечения.
Диета
Специальная диета при раке груди не требуется, достаточно сбалансировано питаться. Соблюдать диету нужно, если есть сопутствующие заболевания: болезни ЖКТ, кахексия, осложнения после химиотерапии и т. д.
Прогноз. Профилактика
Особое значение в лечении рака молочной железы имеет его обнаружение на ранних стадиях. Если лечение начато на первой-второй стадии, вероятность благоприятного исхода значительно выше, в то время как четвертая стадия характеризуется высокой смертностью и невозможностью полного выздоровления. Таким образом, прогноз выживаемости напрямую зависит от того, когда рак груди был диагностирован. Выживаемость оценивается исходя и десятилетнего периода, то есть цифра указывает, какой процент пациентов проживет ближайшие десять лет. Прогноз для различных стадий рака груди выглядит следующим образом:
Использование комплексного подхода к лечению значительно улучшает прогноз для всех категорий пациентов.
Самообследование для профилактики рака груди
Одной из главных мер профилактики рака молочных желез является распространение знаний об этом заболевании и обучение женщин простым приемам самообследования, а также регулярное обследование у маммогола 1 раз в год для женщин старше 40 лет. Женщины с раком груди в анамнезе могут сдать анализ на определение наследственной предрасположенности (BRCA 1, BRCA-2, CHEK) и должны более часто наблюдаться у маммолога (1 раз в 6 месяцев)
Ежемесячный осмотр молочных желез перед зеркалом позволит заметить отклонение от нормы и своевременно обратиться к врачу. Самообследование можно производить регулярно при мытье в душе. Для этого круговыми движениями нужно прощупать последовательно все отделы правой и левой груди по часовой стрелке. Также следует нащупать наличие каких-либо уплотнений в подмышечной впадине. Если во время этого вы обнаружили следующие признаки рака молочной железы: уплотнения в груди, изменения на коже груди или в области соска, выделения из соска темного или красного цвета — это повод обратиться к врачу-маммологу. Также помните, что 1 раз год желательно выполнять УЗИ молочных желез, а начиная с 35 лет также и маммографию (1 раз в 2 года).
Кроме того, необходимо следить за здоровьем репродуктивной системы, принимать гормональные лекарства только по назначению врача и избегать воздействия канцерогенных факторов. Важно, чтобы пациентки могли оперативно проходить необходимые обследования, не сталкиваясь с необходимостью длительного ожидания анализов или диагностических процедур.
Рак пищевода — злокачественная опухоль, исходящая из слизистой оболочки пищевода составляет значительную часть от всех заболеваний этого органа. Основными симптомами этого заболевания являются: прогрессивное нарушение глотания (сначала твёрдой пищи, потом жидкой) и непреднамеренное снижение массы тела. По состоянию на 2012 год рак пищевода был восьмым наиболее распространенным онкологическим заболеванием в мире с 456 000 новых случаев заболевания в течение года. У мужчин рак пищевода встречается примерно в 3 раза чаще, чем у женщин.
Этиология
К основным факторам риска, которые могут вызвать возникновение рака пищевода, относятся:
• Постоянный приём горячей, грубой и плохо пережёванной пищи
• Употребление спиртных напитков
• Частое употребление горячих напитков (чай, кофе)[5][6]
• Курение
• Пищевод Барретта
• Эзофагиты
• Дивертикулит
• Термические и химические ожоги пищевода, сопровождающиеся образованием рубцов
• Лейкоплакии
Типы роста опухоли[править | править код]
Встречаются 3 типа рака пищевода:
• Экзофитный (узловой, грибовидный, папилломатозный - рост в просвет органа)
• Эндофитный (язвенный)
• Инфильтративный склерозирующий (циркулярная форма)
Гистологические формы
Чаще всего (97—99 % случаев) обнаруживают плоскоклеточный рак с ороговением и без ороговения. Также встречаются железистые формы рака пищевода и опухоли, происходящие из дистопированного эпителия. Международная классификация также включает мелкоклеточный рак, аденоакантому и карциносаркому. [7]Редко обнаруживают также недифференцированный рак.
Метастазирование
Метастазирование рака пищевода обусловлено развитой лимфатической сетью пищевода. Метастазы распространяются на прилежащие лимфатические сосуды, а затем и лимфатические узлы. Рак шейного отдела пищевода метастазирует в глубокие шейные лимфатические узлы, рак верхнегрудного и среднегрудного отделов пищевода поражает метастазами параэзофагеальные, трахеобронхиальные и задние средостенные лимфоузлы; рак нижнегрудного и брюшного отделов распространяется в поддиафрагменные, параэзофагеальные, паракардиальные лимфатические узлы, а также в лимфоузлы вдоль малой кривизны желудка и левой желудочной артерии. Кроме того, встречаются метастазы в лимфоузлы малого сальника, вдоль левой желудочной артерии и в шейные и надключичные лимфоузлы.
Отдалённые метастазы поражают печень, лёгкие, костную систему.
Клиническая картина
Клинические симптомы рака пищевода можно разделить на три группы: первичные или местные симптомы, обусловленные поражением стенок пищевода; вторичные симптомы, возникающие в результате распространения опухолевого процесса на соседние органы и ткани; общие симптомы, обусловленные интоксикацией и нарушением питания.
К первичным симптомам относятся дисфагия, боли за грудиной, ощущение полноты за грудиной, срыгивание пищей (регургитация), усиленная саливация. Практически все эти симптомы свидетельствуют о достаточно большом распространении патологического процесса по пищеводу.
Типичные симптомы рака пищевода обусловлены феноменом обтурации. Наиболее ярким из них является дисфагия — затруднение прохождения пищи по пищеводу. Дисфагия обусловлена сужением просвета органа растущей опухолью (механическая дисфагия), но иногда она зависит от спазма в вышележащих отделах пищевода (рефлекторная дисфагия).
В большинстве случаев дисфагия нарастает постепенно. Вначале появляются едва заметные задержки при прохождении по пищеводу твёрдой пищи. Больной как бы ощущает твёрдый пищевой комок, продвигающийся по пищеводу. Сужение прогрессирует, и вскоре больной вынужден запивать твёрдую пищу глотком воды или отказываться от приёма вторых блюд. В дальнейшем через несколько недель или месяцев перестаёт проходить полужидкая пища, а затем и жидкость. Такое последовательное развитие дисфагии наблюдается не всегда. Иногда в результате распада опухоли или медикаментозного лечения проходимость пищевода частично или полностью восстанавливается. Улучшение состояния длится недолго, и вскоре дисфагия вновь начинает прогрессировать.
Профилактика
Отказ от курения и приема алкоголя
1. Употребление в пищу овощей (согласно статистическим данным Национального Института Рака (США), употребление в пищу капусты, брокколи, брюссельской капусты коррелирует с уменьшением частоты возникновения рака пищевода)
2. Умеренное употребление кофе статистически коррелирует с уменьшением частоты возникновения рака пищевода
3. Осторожное употребление чрезмерно горячих напитков - чая и кофе[8].
Лечение:
Моноклональные антитела: ниволумаб, пембролизумаб.
• Гастростомия
Рак толстой кишки (колоректальный рак) — это собирательное название для группы злокачественных новообразований, которые развиваются из эпителия кишечной стенки. К ним относят злокачественные опухоли ободочной, сигмовидной и прямой кишки.
Эпидемиология
Заболевание во всём мире считается третьим по распространённости среди различных видов рака, и занимает второе место по смертельным случаям — по данным ВОЗ, больше людей ежегодно умирают только от рака лёгких. Колоректальный рак чаще встречается у мужчин, чем у женщин. Риск заболеть существенно увеличивается с возрастом. В более чем половине случаев опухоль развивается в сигмовидной и прямой кишке.
Провоцирующие факторы
Спровоцировать развитие заболевания могут следующие факторы:
Наличие аденоматозных полипов. Полипы — это относительно доброкачественные новообразования, которые имеют вид нароста, выступающего в просвет полого органа, в данном случае кишечника. Существует несколько видов колоректальных полипов. Одни из них склонны к малингизации (перерождению в злокачественную опухоль), другие нет. Например, фиброзные и гиперпластические полипы не склонны к злокачественной трансформации. Ювенильные и воспалительные могут переродиться в рак при наличии диспластических изменений, а вот аденоматозные полипы однозначно склонны к малигнизации. Максимальные риски возникают в следующих случаях:
• ворсинчатые аденоматозные полипы;
• множественный полипоз;
• полипы крупных размеров, особенно на широком основании;
• длительно существующие полипы.
Пищевые привычки. Чаще всего колоректальный рак располагается в техотделах кишечника, где происходит задержка его содержимого, — в прямой и сигмовидной кишке. Это позволило врачам предположить, что состав кишечного содержимого имеет непосредственное влияние на вероятность развития рака. Дальнейшие исследования подтвердили эту теорию. Наиболее высокие показатели заболеваемости отмечались у населения, склонного употреблять в пищу большое количество животных жиров и белков, а также малое количество клетчатки. Последний момент имеет наиболее важное значение, поскольку именно пищевые волокна составляют основную часть каловых масс, стимулируют перистальтику кишечника и его своевременное опорожнение, тем самым сокращают контакт стенки с пищевыми канцерогенами.
Возраст старше 50 лет. Крайне редко рак толстой кишки диагностируется у молодых людей. С возрастом вероятность обнаружения опухоли увеличивается. Наиболее подвержены риску люди старше 60 лет.
Наследственная предрасположенность. Есть ряд наследственных заболеваний, при которых риск колоректального рака особенно велик. К ним относят наследственные полипозы (синдром Гарднера, Тюрко, Пейтца), а также синдром Линча — наследственный неполипозный рак толстой кишки.
Хронические воспалительные заболевания толстого кишечника — болезнь Крона и неспецифический язвенный колит.
Иммунодефицитные состояния, причём как врожденные (первичные), так и приобретенные.
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением — это опасно для вашего здоровья!
Симптомы рака толстой кишки
Клинические проявления колоректального рака зависят от локализации опухоли и стадии заболевания. Довольно часто на начальных этапах никаких жалоб больные не предъявляют, а опухоль обнаруживается только при специальном обследовании.
Местные симптомы
Скрытое кровотечение — один из ранних симптомов рака толстой кишки. Первоначально оно никак не проявляется, но его можно обнаружить с помощью специального теста на скрытую кровь. Такие анализы используют с целью скрининга.
Довольно часто первым специфическим симптомом позднего рака толстой кишки является кишечная непроходимость. Она возникает из-за того, что просвет кишки перекрывается опухолевыми массами. Симптомы и тяжесть этого состояния обуславливаются локализацией обтурации (закупорки). Если это правый отдел толстого кишечника, просвет которого довольно широкий, то кишечное содержимое будет иметь мягкую или кашицеобразную консистенцию. Непроходимость здесь развивается лишь на терминальных стадиях заболевания.
В сигмовидной и прямой кишке просвет более узкий, и содержимое в нём имеет плотную консистенцию. Поэтому именно здесь обтурация встречается чаще всего. Проявляется она задержкой стула, вздутием живота и схваткообразными болями. Постепенно присоединяются симптомы обезвоживания и дегидратации. Кишечная непроходимость — это жизнеугрожающее состояние, которое требует немедленной медицинской помощи.
В ряде случаев обтурация может иметь компенсированный характер. Сначала больного беспокоит запор, боль и вздутие живота, которые сменяются зловонными диареями, обусловленными действием гнилостной микрофлоры на содержимое приводящего отдела кишки — под ее действием происходит разжижение каловых масс. Постепенно компенсированная непроходимость неизбежно переходит в полную.
Если опухоль имеет большие размеры, ситуация может осложниться ее распадом с образованием выраженных кровотечений. При этом симптомы будут определяться локализацией кала. При локализации источника кровотечения в ободочной кишке в редких случаях возникает мелена — дёгтеобразный (чёрный, по консистенции похожий на кашицу) стул. Он является результатов ферментации крови кишечным содержимым. Если вовлечена прямая или сигмовидная кишка, наблюдается выделение алой крови из заднего прохода. На фоне массированной кровопотери развивается острая постгеморрагическая анемия, сопровождающаяся слабостью, бледностью кожных покровов и головокружением.
При локализации рака в прямой кишке могут наблюдаться патологические выделения из заднего прохода — слизь, кровь, гнойно-некротические массы, фрагменты новообразования.
Неспецифические симптомы
Кроме того, при колоректальном раке могут присутствовать неспецифические симптомы, которые характерны для многих заболеваний, например, общая слабость, снижение веса, потеря аппетита, вздутие живота и запоры.
Рак толстой кишки восходящего отдела
" Рак восходящего отдела толстой кишки" — термин, который обозначает локализацию злокачественной опухоли. Анатомически толстая кишка состоит из нескольких отделов:
1. Слепая кишка находится в правой нижней части живота (правой подвздошной области). От неё отходит червеобразный отросток – аппендикс.
2. От слепой кишки вверх отходит восходящая ободочная кишка.
3. Затем восходящая ободочная кишка изгибается и переходит в поперечную ободочную кишку. Она проходит в верхней части живота справа налево.
4. Затем, в левой части живота, происходит еще один изгиб, и поперечная ободочная кишка переходит в нисходящую.
5. Внизу от нисходящей ободочной кишки отходит сигмовидная. Она переходит в прямую кишку.
6. Злокачественные опухоли правой (слепой, восходящей и поперечной ободочной) и левой (нисходящей ободочной и сигмовидной) части толстой кишки несколько различаются. Некоторые учёные даже призывают считать их двумя разными онкологическими заболеваниями.
Основные особенности злокачественных опухолей восходящей толстой кишки:
• развиваются в более старшем возрасте, чем опухоли в левой части толстой кишки;
• женщины страдают ими чаще, чем мужчины;
• эти опухоли отличаются высокой иммуногенностью (способностью вызывать иммунные реакции) и хорошо поддаются лечению иммунотерапией;
• прогноз более благоприятный, по сравнению с левосторонними опухолями, при I и II стадиях заболевания, но менее благоприятный при III и IV стадиях;
• за счёт того, что восходящая ободочная кишка имеет большую ширину просвета по сравнению с нисходящей, злокачественные опухоли в ней не вызывают симптомов, пока не достигнут больших размеров.
Метахронный рак толстой кишки
Термин " метахронный рак" применяют для описания первично-множественных злокачественных опухолей. У больного выявляют сразу два разных злокачественных новообразования, которые не связаны между собой и не являются метастазами друг друга. Такие опухоли могут находиться в разных частях организма, парных органах (например, правой и левой молочных железах) или в разных местах в одном органе.
Если вторая опухоль возникла не позднее 6 месяцев после того, как обнаружена первая, то это синхронный рак. Если новообразования выявлены с промежутком более полугода, то такой рак называют метахронным.
Такие ситуации встречаются при разных онкологических заболеваниях, в том числе колоректальном раке. Например, он может сочетаться с опухолями желудочно-кишечного тракта, женской репродуктивной системы. С метахронным раком сложнее бороться, тем не менее, при своевременной диагностике зачастую возможно радикальное лечение и наступление ремиссии.
Патогенез рака толстой кишки
В большинстве случаев рак толстой кишки развивается из полипов (чаще всего аденоматозных) — доброкачественных новообразований в толстом кишечнике. Аденоматозный полипоз может иметь генетический характер происхождения из-за наследования мутации гена APC (Adenomatous Polyposis Coli gene, ген-супрессор опухолевого роста). При длительном существовании полипа в его ткани развивается дисплазия (нарушение гистологической структуры). Степень дисплазии нарастает, в результате чего некоторые клетки трансформируются в злокачественные. Они не подвержены апоптозу (запрограммированной гибели клеток) и даже наоборот, склонны к бесконтрольному размножению. Постепенно опухолевая масса нарастает, а само новообразование просачивается в ткани органа (инфильтрирует их), углубляясь всё дальше, и поражает новые слои стенки кишечника.
Классификация и стадии развития рака толстой кишки
Наиболее часто встречающаяся форма колоректального рака — это аденокарцинома. Её диагностируют в 75-80 % случаев. Среди других вариантов рака встречаются:
• перстневидно-клеточный;
• мелкоклеточный;
• плоскоклеточный;
• медуллярный;
• недифференцированные опухоли.
В зависимости особенностей роста новообразования, выделяют:
• экзофитный рак — растёт в просвет кишки и имеет вид полипов и наростов;
• эндофитный рак — растёт инфильтративно внутрь организма, захватывая все слои стенки кишки и распространяясь по её окружности;
• смешанные опухоли, которые растут одновременно экзофитно и эндофитно.
Клинические формы рака ободочной кишки:
1. Токсико-анемическая. Ухудшается общее состояние больного из-за интоксикации – отравления организма веществами, которые выделяются в результате присутствия злокачественной опухоли. Одновременно в анализе крови обнаруживается анемия – снижение уровня эритроцитов и гемоглобина. Возникает лихорадка. Такая клиническая картина характерна для злокачественных опухолей, находящихся в правой части толстой кишки.
2. Энтероколитическая. Напоминает кишечные расстройства, вызванные воспалительным процессом. Проявляется в виде запоров, диареи, болей, вздутия живота. Запоры возникают из-за того, что опухоль блокирует просвет кишки и мешает прохождению каловых масс. Из-за этого в кишечнике начинается брожение, и, как следствие, отходит жидкий зловонный стул.
3. Диспепсическая. Проявляется в виде болей и чувства дискомфорта в животе, вздутия живота, проблем со стулом.
4. Обтурационная. Развиваются симптомы кишечной непроходимости. Эта форма более характерна для рака левой половины толстой кишки, так как она имеет меньшую ширину просвета, и злокачественная опухоль быстрее его перекрывает.
5. Псевдовоспалительная. В брюшной полости обнаруживают признаки воспалительного процесса. Пациента беспокоят боли, развивается лихорадка. Во время осмотра врач обнаруживает признаки раздражения брюшины. В крови повышается уровень лейкоцитов.
6. Опухолевая. Эту форму еще называют атипичной, потому что пациента не беспокоят симптомы. Врач обнаруживает опухоль случайно во время ощупывания живота.
Кроме того, выделяют осложнённые формы — если рак толстой кишки привел к кишечной непроходимости, перфорации (образованию сквозного отверстия) стенки кишки, кровотечению, воспалению в брюшной полости.
Стадии рака прямой кишки
Для определения стадии используется TNM классификация, основанная на степени инфильтрации опухоли, её взаимодействия с окружающими органами и тканями, а также наличии регионарных и отдалённых метастазов. Здесь выделяют:
• 1 стадия — по данным гистологического ответа опухоль не выходит дальше, чем на подслизистую основу стенки кишки;
• 2 стадия — в процесс вовлекается мышечный слой кишечной стенки;
• 3 стадия — поражение захватывает все слои стенки кишки, в процесс могут вовлекаться ткани, окружающие первичный очаг, также могут быть регионарные метастазы;
• 4 стадия — имеются отдаленные метастазы.
По клинической картине невозможно точно сказать, на какой стадии находится заболевание, потому что его течение зависит от множества факторов и в каждом случае индивидуально.
На ранних стадиях рака прямой кишки симптомы, как правило, отсутствуют. Злокачественная опухоль в кишке может расти в течение нескольких лет, не вызывая у больного жалоб. Поэтому всем людям начиная с 50 лет важно проходить скрининговые исследования. В то же время, выраженные симптомы могут наблюдаться уже на этапе предраковых изменений — кишечных полипов.
Обычно первыми проявлениями заболевания становятся запоры, диарея, изменения характера стула, боли и чувство дискомфорта в животе, его вздутие из-за скопления газов (метеоризм).
Когда опухоль достигает больших размеров, она вызывает полную или частичную кишечную непроходимость. Зачастую таким больным требуется экстренная медицинская помощь.
Также может развиться осложнение в виде перфорации стенки кишки – образования в ней сквозного отверстия. При этом возникают сильные боли в животе, напряжение мышц брюшного пресса, тошнота, рвота, повышение температуры тела.
Кровотечение из опухоли приводит к анемии. Больной становится бледным, постоянно чувствует слабость, усталость, беспокоят головные боли, головокружения.
Когда раковые клетки распространяются по поверхности брюшины, развивается состояние, которое называется перитонеальным канцероматозом. Возникает асцит – патологическое скопление жидкости в брюшной полости. При этом увеличивается живот, нарушается работа внутренних органов. Если жидкости скапливается очень много, она начинает ограничивать подвижность диафрагмы, и у больного возникает одышка.
На IV стадии рак толстой кишки метастазирует. При этом возникают симптомы, которые зависят от того, в каких органах находятся метастатические очаги:
• Печень: боли и дискомфорт в верхней части живота справа, отсутствие аппетита, тошнота, рвота. При обширном поражении данного органа развивается желтуха.
• Лёгкие: одышка, упорный хронический кашель, боли в грудной клетке.
• Кости и позвоночник: мучительные боли, патологические переломы.
• Головной мозг: головные боли, головокружения, нарушение координации движений, походки, судороги, другие неврологические расстройства.
Рак толстой кишки восходящего отдела
" Рак восходящего отдела толстой кишки" — термин, который обозначает локализацию злокачественной опухоли. Анатомически толстая кишка состоит из нескольких отделов. Злокачественные опухоли правой (слепой, восходящей и поперечной ободочной) и левой (нисходящей ободочной и сигмовидной) части толстой кишки несколько различаются. Некоторые учёные даже призывают считать их двумя разными онкологическими заболеваниями.
инвазии в кишечную стенку (если материал позволяет) и её молекулярно-биологические характеристики.
Также обнаружение новообразования возможно при помощи ирригоскопии — рентгенологического исследования толстого кишечника после двойного контрастирования. С помощью этого метода определяют форму роста новообразования, его протяжённость, наличие свищей и изъязвлений.
Дополнительные методы диагностики
Для уточнения распространенности процесса и планирования лечения прибегают к дополнительным методам диагностики:
• ультразвуковое исследование (УЗИ) прямой кишки — может показать степень прорастания опухоли сквозь кишечную стенку и в окружающие ткани, наличие метастазов в лимфатических узлах;
• онкомаркеры: для колоректального рака специфическим маркером является РЭА — раковоэмбриональный антиген. Этот анализ используется для контроля лечения, раннего обнаружения рецидивов и для отслеживания динамики течения заболевания. Но для первичной диагностики наличия рака толстой кишки определение данного маркера нецелесообразно из-за его недостаточной чувствительности и специфичности;
• рентгенография органов грудной клетки проводится для поиска метастазов в легких;
• компьютерная томография (КТ), позитронно-эмиссионная компьютерная томография (ПЭТ-КТ), магнитно-резонансная томография (МРТ), сцинтиграфия используются для поиска отдалённых метастазов и микрометастазов.
Окончательное определение стадии проводится после интраоперационной ревизии брюшной полости. Только тогда можно определить истинную распространенность процесса.
Основные особенности злокачественных опухолей восходящей толстой кишки:
• развиваются в более старшем возрасте, чем опухоли в левой части толстой кишки;
• женщины страдают ими чаще, чем мужчины;
• эти опухоли отличаются высокой иммуногенностью (способностью вызывать иммунные реакции) и хорошо поддаются лечению иммунотерапией;
• прогноз более благоприятный, по сравнению с левосторонними опухолями, при I и II стадиях заболевания, но менее благоприятный при III и IV стадиях;
• за счёт того, что восходящая ободочная кишка имеет большую ширину просвета по сравнению с нисходящей, злокачественные опухоли в ней не вызывают симптомов, пока не достигнут больших размеров.
Метахронный рак толстой кишки
Термин " метахронный рак" применяют, когда у пациента выявляют сразу два разных злокачественных новообразования, которые не связаны между собой и не являются метастазами друг друга. Опухоли могут находиться в разных частях организма, парных органах (например, в молочных железах) или в разных местах в одном органе.
Если вторая опухоль возникла не позднее 6 месяцев после того, как обнаружена первая, то это синхронный рак. Если новообразования выявлены с промежутком более полугода, то такой рак называют метахронным. Такие ситуации встречаются в том числе колоректальном раке. Например, он может сочетаться с опухолями желудочно-кишечного тракта и женской репродуктивной системы.
Осложнения рака толстой кишки
Для рака толстой кишки характерно развитие различных осложнений, которые оказывают влияние как на течение заболевания, так и на его прогноз. В части случаев именно осложнения являются причиной гибели больного, в то время как сам онкологический процесс остается локализованным. Наиболее часто встречаются:
• кишечная непроходимость;
• кровотечения;
• гнойно-воспалительные осложнения;
• осложнения со стороны вовлеченных в процесс органов — при метастазировании в печень может наблюдаться желтуха, при поражении головного мозга – нарушение сознания, судороги, неврологическая симптоматика.
Диагностика рака толстой кишки
Когда необходимо обратиться к врачу
На ранних стадиях симптомы, как правило, отсутствуют. Поэтому всем людям начиная с 50 лет важно проходить скрининговые исследования. Обычно первыми проявлениями заболевания становятся запоры, диарея, изменения характера стула, боли и чувство дискомфорта в животе, его вздутие из-за скопления газов (метеоризм). При появлении этих симптомов следует обратиться к врачу.
В рамках диагностики рака толстой кишки необходимо не только определить наличие опухоли как таковой, но и установить её гистологический вариант (клеточную форму), а также стадию заболевания. С этой целью используется комплексная диагностика.
Методы обнаружения опухоли
Для обнаружения опухоли применяют следующие методы:
• анализ кала на скрытую кровь (гемокультуральный тест) — исследовании трёх последовательных порций кала на наличие крови, которая может быть не видна невооруженным глазом (скрытая кровь), обнаружение крови в кале — показание к колоноскопии;
• пальцевое ректальное исследование — с его помощью обнаруживают до 70 % новообразований прямой кишки;
• сигмоскопия — это эндоскопическое исследование кишечника, которое проводят так же, как и колоноскопию, только во время него исследуют лишь конечную часть толстой кишки — сигмовидную кишку; оно менее информативно, так как во время него можно осмотреть лишь меньшую часть толстой кишки;
• ректоскопия — эндоскопическое исследование прямой кишки;
• ректосигмоидоскопия — инструментальный осмотр прямой и сигмовидной кишки, проводится с помощью жёсткого ректороманоскопа;
• колоноскопия — осмотр слизистой всей толстой кишки с помощью гибкого колоноскопа.
При выявлении рака в прямой и сигмовидной кишке в дальнейшем всё равно необходима колоноскопия, поскольку у 5 % пациентов обнаруживаются множественные злокачественные опухоли, локализованные в других отделах кишечника.
Сразу после обнаружения проводится биопсия выявленного новообразования. Полученный материал отправляется на исследование в лабораторию, где определяют гистологический вид опухоли, степень
Лечение рака толстой кишки
Хирургическое лечение
Операция — основной метод радикального удаления опухоли. На ранних стадиях заболевания бывает достаточно только её проведения. При распространенных процессах лечение всегда комплексное: помимо хирургического вмешательства может потребоваться лучевая терапия, химиотерапия и таргетная терапию. При малоинвазивных новообразованиях проводят щадящие органосохраняющие вмешательства, которые выполняются эндоскопически [1]. В остальных случаях проводится резекция (удаление) кишки с соблюдением правил абластики:
• опухоль удаляется единым блоком с вовлеченными в процесс тканями: удалению подлежат в том числе регионарные лимфатические узлы. Помимо лечебной цели, удаление лимфоузлов имеет и ценное диагностическое значение — их морфологическое изучение даёт информацию о наличии метастазов и помогает точно определить стадию процесса. Это оказывает влияние на дальнейшую тактику лечения, в частности необходимость назначения послеоперационной химио- или лучевой терапии;
• должно быть достаточное расстояние от видимого края опухоли до края резекции — в идеале удаляется около 30-40 см кишки. Полученный материал отправляется на срочное гистологическое исследование, чтобы определить наличие в краях резекции опухолевых клеток.
При раке прямой кишки в рамках радикального лечения применяется химиолучевая терапия. В некоторых случаях это позволяет сохранить прямую кишку и анальный сфинктер.
Хирургическое лечение может выполняться в один или два этапа. При одноэтапном лечении удаление опухоли и восстановление непрерывности кишечника проводится в ходе одной операции, когда края резекции соединяются анастомозом. Это возможно при соблюдении нескольких условий:
• соединяемые участки кровоснабжаются в достаточной мере;
• нет натяжения сшиваемых участков;
• низкие риски инфекционных осложнений.
При несоблюдении этих условий существует высокая вероятность развития несостоятельности анастомоза, некроза и инфекционных осложнений. Чтобы этого избежать, проводят двухэтапные вмешательства. На первом этапе удаляется опухоль, а приводящий конец кишки выводится на переднюю брюшную стенку в виде колостомы, через которую будет выходить кишечное содержимое.
После того как больной заканчивает противоопухолевое лечение, результаты которого будут удовлетворительными, врачи проводят реконструктивные вмешательства по восстановлению непрерывности кишечника.
Если имеются отдалённые метастазы, то их рекомендуется удалять хирургически одновременно с первичной опухолью. Такие операции называются симультанными и проводятся комбинированной бригадой с привлечением хирургов смежных специальностей.
Химиотерапия
Химиотерапия при раке толстой кишки проводится после операции (адъювантная) и назначается в следующих случаях:
• наличие регионарных метастазов;
• вовлечение в процесс всей толщи стенки кишки;
• низкодифференцированные опухоли;
• наличие злокачественных клеток в краях резекции.
Также возможно неоадъювантное химиотерапевтическое лечение первично нерезектабельных опухолей. В этом случае назначается несколько курсов химиотерапии, и после их окончания повторно оценивается возможность проведения радикальной операции.
Химиотерапию рекомендуют назначать не позднее, чем через 28 дней от момента операции (при отсутствии противопоказаний). При этом основная терапия длится 3-4 месяца, после чего проводится поддерживающая терапия.
Лечение может дополняться таргетными препаратами — бевацизумаб, цетуксимаб, панитумумаб. Эти препараты действуют на специфические процессы, обусловливающие жизнедеятельность опухолевых клеток. Их назначают после молекулярно-генетического тестирования. Некоторые препараты применяются только с химиотерапией, другие могут использоваться как в монорежиме, так и в рамках комбинированной терапии.
Таргетная терапия
Таргетные препараты действуют на клеточные механизмы, которые обеспечивают канцерогенез — процесс образования и развития злокачественной опухоли. Они не могут полностью уничтожить рак, но существенно замедляют его рост и прогрессирование. Ввиду своего узкоспециализированного действия эти препараты назначаются только после проведения специальных анализов, которые выявляют наличие мутаций, при которых показана, или наоборот, неэффективна таргетная терапия.
Например, добавление к стандартный режимам химиотерапии при лечении метастатического рака толстой кишки бевацизумаба, цетуксимаба или панитумумаба увеличивает общую продолжительность жизни с 18 месяцев до 29. Бевацизумаб ингибирует активность фактора роста эндотелия, что снижает васкуляризацию опухоли. Цетуксимаб и панитумумаб действуют на рецептор эпидермального фактора роста (EGFR), который отвечает за дифференцировку, пролиферацию и выживаемость злокачественных клеток.
Лучевая терапия
Лучевая терапия в основном используется при лечении рака прямой кишки, поскольку другие отделы кишечника обладают выраженной физиологической подвижностью, что делает невозможным четкое позиционирование опухоли для планирования полей облучения. В остальных случаях её используют с паллиативной целью для лечения отдаленных метастазов.
При раке прямой кишки лучевая терапия применяется в рамках комбинированного лечения совместно с химиотерапией. В некоторых случаях это позволяет провести органосохраняющее лечение без выведения колостомы.
Диспансерное наблюдение
После того как лечение рака толстой кишки успешно завершено, сохраняется риск рецидива. Он наиболее высок в течение первых трёх лет, поэтому все пациенты нуждаются в регулярном диспансерном наблюдении. Обычно осмотры врача, УЗИ и анализы крови на раково-эмбриональный антиген (РЭА) проводят со следующей периодичностью:
• в первые 2 года — через каждые 2–3 месяца;
• в течение последующих 3 лет — каждые полгода;
• затем — ежегодно.
Кроме того, раз в два года необходимо проходить колоноскопию. Если во время этих обследований будут обнаружены патологические изменения, то врач назначит компьютерную томографию, сканирование костей и другие методы диагностики.
Особенности реабилитации
После операции при раке толстой кишки врач дает стандартные рекомендации по поводу питания, возвращения к физической активности. Сроки восстановления зависят от вида хирургического вмешательства, способа его проведения (эндоскопический, лапароскопический или открытый через разрез). Если пациенту наложена постоянная колостома, перед выпиской ему объяснят, как за ней правильно ухаживать.
Некоторые побочные эффекты химиопрепаратов сохраняются после завершения курса лечения. В таком случае врач назначит необходимое лечение для их купирования, даст пациенту рекомендации по поводу образа жизни. Многие люди, избавившиеся от рака, испытывают психоэмоциональные проблемы, постоянно боятся рецидива. В таких случаях требуется помощь психолога.
Профилактика
Прогноз при раке кишечника определяется стадией опухоли, гистологическим вариантом новообразования и возможностью проведения радикального лечения.
Наилучшие результаты достигаются при начальных формах заболевания. В этом случае удается добиться пятилетней выживаемости в 70-95 % случаев. При распространённых процессах важно радикально провести лечение. Если оно прошло успешно, пятилетний рубеж переживают около половины пациентов. Если лечение изначально проводилось с паллиативной целью, пятилетняя выживаемость колеблется в пределах 10 %.
Рак толстой кишки является потенциально предотвратимым заболеванием. Если соблюдать определенные правила, можно существенно снизить вероятность его возникновения.
Диета
Первым делом необходимо пересмотреть пищевое поведение. Рекомендуется нормализовать режим питания, отказаться от переедания, контролировать приём жиров животного происхождения. При недостатке в рационе пищевых волокон следует обогатить меню овощами, фруктами и кашами. Из мясных продуктов лучше отдавать предпочтение нежирному белому мясу и рыбе.
Двигательная активность
Важна также и нормальная двигательная активность. Если вы ведете малоподвижный образ жизни, постарайтесь хотя бы делать ежедневные получасовые прогулки. Но лучше оптимизировать свой режим дня, чтобы было достаточно времени на физическую активность и отдых.
Рак толстой кишки является потенциально предотвратимым заболеванием. Если соблюдать определенные правила, можно существенно снизить вероятность его возникновения.
Рак прямой кишки – это злокачественная опухоль дистального отдела толстого кишечника эпителиального происхождения. Клинически проявляется наличием патологических примесей в кале (слизи, крови), кровотечением из прямой кишки, болью в крестце и промежности, слабостью, похуданием, анемией. Методами диагностики являются исследование кала на скрытую кровь, определение лабораторных маркеров, ректороманоскопия, биопсия с морфологическим исследованием. Лечение хирургическое (резекция или экстирпация прямой кишки), с возможным назначением химиотерапии при метастазах рака в регионарные лимфатические узлы.
• Причины
• Классификация
• Симптомы рака
• Осложнения
• Диагностика
• Лечение рака прямой кишки
• Прогноз и профилактика
• Цены на лечение
Общие сведения
Рак прямой кишки – различные по гистологическому строению и локализации злокачественные новообразования прямой кишки. Среди злокачественных поражений ЖКТ данная патология составляет 45%; вместе с тем, 70% случаев рака толстого кишечника локализуется именно в его дистальном отделе. Заболевание чаще встречается в странах с западным характером питания и реже в - Азии и Африке.
Рак прямой кишки в полтора раза чаще возникает у мужчин, риск его развития повышается с возрастом, в группу риска входят лица старше сорока лет. Предположительно это связано с возрастными изменениями в эпителиальных клетках внутрикишечной выстилки. Несмотря на доступность прямой кишки для осмотра и исследования, большинство случаев рака данной локализации диагностируется уже на поздних сроках, когда радикальные методы лечения оказываются малоэффективными. Пятилетняя выживаемость при раке прямой кишки составляет 40-60%, что обусловливает актуальность данной проблемы для специалистов в области практической онкологии и проктологии.
Причины
Отмечена зависимость развития рака прямой кишки от особенностей питания. Болезнь чаще встречается у людей, употребляющих пищу, богатую жирами и бедную растительной клетчаткой. Рацион питания, перегруженный мясными продуктами, способствует возникновению злокачественных образований в толстом кишечнике. Кроме того, факторами, повышающими риск развития раковой опухоли, являются хронические воспалительные заболевания толстого кишечника, болезнь Крона, неспецифический язвенный колит, врожденные патологии (семейный диффузный полипоз, ферментные недостаточности). Обменные заболевания (сахарный диабет, метаболический синдром, ожирение) также являются канцерогенными факторами.
Полипы прямой кишки являются одним из распространенных предраковых состояний, озлокачествляющиеся приблизительно в 4% случаев (риск озлокачествления прямо пропорционален размеру и распространенности полипов), в особенности опасен в отношении малигнизации семейный полипоз. Наследственный фактор также играет определенную роль в заболеваемости раком прямой кишки. Увеличивают риск развития злокачественного процесса и снижают вероятность благоприятного исхода при лечении курение и злоупотребление алкоголем.
Классификация
Рак прямой кишки классифицируется согласно международной классификации TNM, где T – размер опухоли и степень поражения ею стенки кишки, N – поражение регионарных лимфоузлов, а M – наличие метастазов в отдаленных органах.
Помимо этого, в нашей стране нередко применяется классификация рака по стадиям (I; IIa; IIb; IIIa; IIIb; IV) в зависимости от величины опухоли, степени прорастания ею стенки кишечника и окружающих тканей, имеющихся метастазов. Окончательный диагноз рака прямой кишки осуществляется после хирургического удаления и цитологического исследования опухоли и лимфатических узлов.
Симптомы рака
Чаще всего ранние стадии рака прямой кишки протекают без клинической симптоматики, что значительно затрудняет диагностирование и своевременное выявление злокачественного процесса. Со временем прогрессирование опухоли начинает проявляться разнообразными симптомами. Самые распространенные проявления: нарушение дефекации (запоры или поносы), кишечная непроходимость, кровотечение из заднего прохода, примесь крови в кале, анемия неясной этиологии, боль внизу живота, «ленточный» («карандашный») стул. По мере развития онкологического процесса усиливается выраженность общей симптоматики, включающей отсутствие аппетита, общую слабость, недомогание, потерю веса вплоть до кахексии.
Осложнения
Рак прямой кишки осложняется кровотечением, а при регулярных потерях крови – анемией, снижением массы тела вплоть до истощения. Пациенты с онкологическими патологиями поздних стадий страдают от интоксикации организма продуктами некроза опухолевой ткани. Рак прямой кишки может способствовать развитию инфекционного воспаления. Химиотерапия способствует развитию таких побочных эффектов как облысение, слабость, потеря аппетита, диарея, тошнота.
Диагностика
Диагностика рака прямой кишки предполагает опрос больного, выявление жалоб, сбор анамнеза. При этом обращают внимание на канцерогенные риски, имевшие место опухолевые образования и семейный онкоанамнез. Лабораторные методы включают общий и биохимический анализ крови, тестирование на онкомаркеры, копрограмму.
Для раковых опухолей прямой кишки характерно выявление ракового эмбрионального антигена и онкомаркера СА-19-9. Выявление онкомаркеров может также свидетельствовать о неспецифическом язвенном колите, доброкачественных опухолях. Концентрация эмбрионального ракового антигена повышается у заядлых курильщиков.
К инструментальным методам диагностики опухолей толстого кишечника относится ректороманоскопия (обследуется внутренняя стенка прямой и сигмовидной кишки), колоноскопия (эндоскопическое исследование всего толстого кишечника), ирригоскопия (рентгенографическое исследование толстого кишечника с контрастным веществом).
Эндоскопические методики позволяют подробно изучить состояние слизистой оболочки кишечной стенки, имеющиеся опухолевые образования, произвести биопсию для последующего гистологического и цитологического исследования. Диагностика рака прямой кишки производится только на сновании обнаружения раковых клеток при цитологическом исследовании биоптата.
Кроме того, обнаружить опухолевое образование в кишечнике возможно с помощью ультразвукового исследования (для обследования прямой кишки производят интраректальное УЗИ), магнитно-резонансной и компьютерной томографии. Спиральная компьютерная томография (МСКТ) применяется для исследования органов и систем на предмет выявления метастазов, а также позволяет осуществить прицельную биопсию печени при наличии в ней сомнительных в отношении метастазирования участков.
МРТ органов таза. Злокачественная опухоль стенки прямой кишки; выраженное мягкотканное утолщение стенки органа с признаками инфильтративного роста
Методикой с высокой степень специфичности в отношении выявления метастазов является позитронно-эмиссионная томография (ПЭТ). Методика заключается в ведении в организм позитрон-излучающих изотопов и сканирование их распределения в тканях. Пораженные злокачественными клетками ткани склонны накапливать радиоизотопы и определяться при сканировании в виде участков с повышенным излучением. Ангиографию производят для визуализации сосудистой сети перед операцией (во избежание постоперационных осложнений и массированных кровотечений).
Лечение рака прямой кишки
Основной методикой лечения данного злокачественного новообразования является хирургическое удаление опухоли, прилежащих тканей и лимфоузлов. Выбор методики осуществляется хирургом-онкологом в зависимости от стадии заболевания, размера опухоли, степени поражения метастазами лимфатических узлов и других органов и тканей.
При выявлении рака на поздних стадиях с глубоким прорастанием в окружающие ткани и присутствием множественных метастазов, производят паллиативную операцию: удаление опухоли для освобождения просвета кишечника и облегчения состояния пациента. Излечение на поздних стадиях раковых опухолей невозможно. В онкологической практике в большинстве случаев хирургическое удаление опухоли сочетают с химиотерапией или радиолучевой терапией для профилактики рецидивирования и подавления распространения злокачественных клеток.
Метод химиотерапевтического лечения подразумевает использование лекарственных препаратов, подавляющих рост злокачественных клеток. К сожалению, цитотоксические препараты, применяющиеся при химиотерапии, недостаточно специфичны в отношении раковых клеток и такое лечение имеет массу побочных эффектов. Однако комбинированное применение химиотерапии и хирургического лечения при своевременно выявленном раке прямой кишки дает заметный положительный эффект и значительно снижает риск рецидива заболевания, увеличивая выживаемость пациентов.
Лучевая терапия при раке прямой и толстой кишки иногда применяется в качестве дополнительной меры профилактики рецидивов после оперативного удаления опухоли, а также может использоваться для уменьшения размеров образования и облегчения симптоматики.
Прогноз и профилактика
Выявление и удаление рака прямой кишки на ранних стадиях способствует 5-летней выживаемости в 90% случаев. Однако, только 39% выявленных колоректальных злокачественных опухолей находятся на пригодной для успешного излечения стадии, в остальных случаях, даже с применением паллиативного удаления опухоли, прогноз неблагоприятен. Если в течение 5-ти лет после удаления опухоли не отмечено ее рецидива, то подтверждают выздоровление. Рак IV стадии излечению не подлежит.
Профилактические меры включают регулярное обследование лиц, входящих в группу риска (люди старше 50 лет, больные с хроническими заболеваниями толстого кишечника). Особое внимание уделяется пациентам с полипами толстого кишечника. В скрининговые мероприятия входят: ежегодный анализ кала на скрытую кровь, сигмоидоскопия каждые 5 лет, каждые 10 лет – колоноскопия. Лица, страдающие семейным полипозом, подлежат обследованию каждые 2-3 года. План обследования граждан, входящих в группу онкологического риска, обсуждается с врачом индивидуально.
Общие меры профилактики рака прямой кишки включают активный образ жизни, правильное сбалансированное питание, богатое растительной клетчаткой без перегруженности животными жирами, отказ от курения и злоупотребления алкогольными напитками, своевременное выявление и лечение заболеваний, провоцирующих развитие злокачественных опухолей.
№17.
Травмы мочеполовых органов
Повреждения мочеполовой системы составляют 1, 5-3 % в общей структуре травм всех органов человека. В мирное время их причиной у 75-80 % пострадавших являются повреждения во время дорожно-транспортных происшествий и падения с высоты. В 60-70 % случаев травмы являются сочетанными или множественными, по большей части встречаются повреждения почек и мочевыводящих путей.
Классификация. По локализации различают травмы почек, мочеточников, мочевого пузыря, мочеиспускательного канала и мужских половых органов.
В зависимости от наличия раневого канала, сообщающего зону повреждения с внешней средой, выделяют закрытые и открытые травмы.
Травмы могут быть изолированными, множественными и сочетанными. Изолированным считается ранение одного органа мочеполовой системы, множественными - когда помимо травмы мочеполовых органов имеются повреждения других органов в пределах одной анатомической области, например травма почки и органов живота. Сочетанными считаются одновременные повреждения органов, находящихся в различных анатомических областях, например повреждение мочевого пузыря и черепно-мозговая травма.
В зависимости от степени тяжести травмы мочеполовых органов могут быть легкими, средними и тяжелыми, по отношению к полостям тела - проникающими и непроникающими, в зависимости от стороны поражения - одно- и двусторонними.
Повреждения почек
Эпидемиология. Травма почки встречается наиболее часто и составляет около 60-65 % в структуре повреждений органов мочевой системы. В мирное время превалируют закрытые, а в военное - открытые повреждения почек.
Этиология и патогенез. Закрытые повреждения почек, как правило, наступают в результате приложения силы в область поясницы или живота в виде
удара или сдавливания. В механизме разрыва играет роль и гидродинамический фактор, обусловленный значительным преобладанием в паренхиме почки жидкостного компонента (кровь, лимфа, моча), окруженного плотной фиброзной капсулой. Непосредственный удар и детонация жидкости внутри органа приводят к разрыву фиброзной капсулы и паренхимы почки. В бытовых условиях травма чаще возникает вследствие падения поясничной областью на выступающий твердый предмет. Разрыв органа происходит в результате непосредственного удара и повреждающего действия расположенных рядом костных структур - ребер и позвоночника.
Повреждения почек могут возникать в результате малоинвазивных и эндоскопических методов диагностики и лечения урологических заболеваний, получивших в настоящее время широкое распространение. Прежде всего, они связаны с неосторожными или ошибочными действиями врача. После дистанционной ударно-волновой нефролитотрипсии нередко диагностируются субкапсулярные гематомы, а всегда возникающая после нее гематурия может быть следствием не только повреждающего действия на уротелий камня и его фрагментов, но и разрывов форниксов. Травма почечной паренхимы может наблюдаться при катетеризации (стентировании) мочеточника, уретероскопии, нефроскопии, нефробиопсии и даже при паранефральной блокаде.
Заболевания почки (опухоль, киста, гидронефроз) делают ее более подверженной различным травмирующим воздействиям. Тяжелые повреждения патологически измененной почки могут наступить даже при минимальной травме.
Открытые повреждения - ножевые или огнестрельные - обычно носят множественный характер.
Классификация. Клинико-анатомическая классификация закрытых повреждений почки строится на степени тяжести травмы органа. Различают ушибы и разрывы почки. Ушиб характеризуется резким сотрясением (контузией) органа без разрывов паренхимы почки, ее капсулы и полостной системы. Клинически значимое повреждение почки наблюдается только при ее разрывах, от микроскопических надрывов паренхимы и форниксов до размозжения органа. С этих позиций появление субкапсулярных и околопочечных гематом, а также гематурии всегда является следствием пусть даже незначительных, но разрывов паренхимы.
Классификация разрывов почки:
а - наружный разрыв паренхимы почки с образованием субкапсулярной гематомы;
б - наружный разрыв паренхимы и капсулы почки с образованием паранефральной гематомы;
в - внутренний разрыв паренхимы и форниксов, открывающийся в полостную систему почки (гематурия);
г - проникающий разрыв капсулы, паренхимы и полостной системы почки с образованием паранефральной урогематомы (гематурия);
д - размозжение почки: множественные проникающие разрывы капсулы, паренхимы и полостной системы почки с образование паранефральной уроге-матомы (гематурия);
е - отрыв сосудистой ножки с размозжением паренхимы почки.
Виды разрывов почки
Наиболее тяжелыми формами повреждений почки являются ее размозжение, то есть образование множественных, проникающих в чашечно-лоханочную систему разрывов органа с возможным отрывом участков паренхимы (полюса), и разрыв (отрыв) сосудистой ножки. Последний не имеет клинического значения, так как почти всегда сочетается с не менее тяжелыми повреждениями других органов, что делает такого рода повреждения несовместимыми с жизнью.
Симптоматика и клиническое течение. Клиническая картина зависит от степени повреждения почки и наличия травм других органов. Больные жалуются на боли в поясничной области и/или в животе, усиливающиеся при глубоком дыхании, вздутие живота, тошноту, рвоту, общую слабость. Тотальная гематурия наблюдается при тяжелых повреждениях почек (рис. 15. 1, в-е). Макрогематурия служит признаком степени выраженности повреждения органа, в свою очередь являясь одним из определяющих факторов тяжести состояния пострадавшего. Вместе с тем в ряде случаев степень гематурии не соответствует степени повреждения почки. При небольших форникальных разрывах может наблюдаться стойкая выраженная гематурия, и, наоборот, при размозжении почки гематурия
может быть незначительной либо отсутствовать в результате тампонады полостной системы сгустками крови и/или повреждения лоханки, мочеточника и ее сосудистой ножки.
Разрыв богатого сосудами паренхиматозного органа, каким является почка, сопровождается признаками внутреннего кровотечения. В сочетании с выраженной гематурией оно может быстро привести к анемизации и тяжелому состоянию больного, что проявляется бледностью кожных покровов, холодным потом, тахикардией, снижением артериального давления, нарастанием забрю-шинной урогематомы. При объективном исследовании на коже живота и поясничной области могут определяться ссадины, кровоизлияния, отечность тканей, а также выбухание в данной области, обусловленное урогематомой больших размеров. Расположение и ход раневого канала с истечением из него мочи позволяют заподозрить открытое повреждение почки. Пальпация грудной клетки и позвоночника может сопровождаться резкой болезненностью вследствие перелома этих костных образований. При пальпации живота определяются болезненность и защитное напряжение мышц на стороне поражения, а при больших урогематомах - округлое образование в подреберье и поясничной области.
Отдаленными осложнениями закрытых повреждений почек являются организовавшаяся, сдавливающая почку гематома, камнеобразование, гидронефроз, артериальная гипертензия и др.
Диагностика. В диагностике обращают внимание на вид и характер травмы, ее объективные местные и общие проявления. В анализах крови определяется снижение количества эритроцитов и гемоглобина, в более поздние сроки с момента травмы присоединяется лейкоцитоз. В анализе мочи эритроциты покрывают все поле зрения. Суммарную функцию почек позволяет оценить определение остаточного азота, мочевины и креатинина сыворотки крови, что особенно важно знать при повреждении единственной почки и планировании оперативного лечения.
Основными в постановке диагноза разрыва почки являются лучевые методы. Они позволяют, во-первых, определить степень повреждения почки, во-вторых, оценить раздельную функцию поврежденной и контрлатеральной почек, в-третьих, отслеживать динамику раневого процесса с целью ранней диагностики осложнений и производить их своевременную коррекцию. Наиболее доступный, малоинвазивный и быстрый метод диагностики повреждений почек - УЗИ. С его помощью можно выявить суб-капсулярные и паранефральные уро-гематомы, определить размеры, деформацию контуров почки, дефекты паренхимы, деформацию чашечно-лоханочной системы, степень ее эктазии, обнаружить сгустки
Экскреторная урограмма. Затек контрастного вещества (стрелка) в результате разрыва правой почки
крови. Сопоставление результатов УЗИ с анамнезом, данными физи-кального обследования и степенью выраженности кровотечения нередко позволяет установить диагноз и при тяжелом состоянии больного приступить к экстренной операции без других методов обследования.
Во всех случаях больным с подозрением на травму почек следует выполнить обзорную рентгенографию брюшной полости и забрюшинного пространства. С ее помощью можно выявить сколиоз, отсутствие контура почки и большой поясничной мышцы, переломы нижних ребер, поперечных отростков позвонков и костей таза. Экскреторная урография позволяет обнаружить деформацию и сдавливание чашечек и лоханки, затеки контраста на стороне поражения, оценить функцию поврежденной и контрлатеральной почек, что важно при определении
объема экстренного оперативного вмешательства. Применение ее ограничено в случаях сочетанных повреждений и у пострадавших с шоком и нестабильной гемодинамикой (систолическое давление ниже 90 мм рт. ст. ).
В настоящее время ретроградная уретеропиелография в диагностике повреждений почек применяется крайне редко в связи с появлением новых ме-
тодов исследования. Ее можно использовать для уточнения степени повреждения почки, при неинформативности экскреторной урографии и недоступности КТ, МРТ и ангиографии в связи с экстренностью ситуации или отсутствием их в данном стационаре.
Наиболее информативными методами диагностики повреждений почек являются КТ и МРТ. При введении в вену рентгеноконтрастных веществ, как правило, исключается необходимость использования других лучевых методов. КТ и МРТ обеспечивают наивысшую степень точности в оценке анатомических деталей
Экстравазация контрастного вещества в результате разрыва левой почки
травмированной почки. В практике неотложной помощи их точность достигает 98 %. КТ позволяет визуализировать повреждения паренхимы) и сосудов почки, сегментов органа, лишенных кровоснабжения, и обнаружить даже небольшие мочевые затеки, содержащие рент-геноконтрастное вещество (экстравазаты), а также травму других паренхиматозных органов. С помощью КТ иМРТ можно выявить повреждения почки в результате эндоурологических вмешательств.
Лечение травмы мочевого пузыря
Пострадавшего срочно госпитализируют в травматологическое или урологическое отделение, переводят на строгий постельный режим. Консервативное ведение в виде катетеризации (обычно на 3-5 суток до прекращения макрогематурии) возможно только при контузии мочевого пузыря, надрывах слизистой при грубых медицинских манипуляциях, небольших экстраперитонеальных разрывах с сохраненной уровезикальной шейкой. Остальным пострадавшим показано экстренное проведение реконструктивного хирургического вмешательства с дренированием брюшной или тазовой полостей.
На этапе предоперационной подготовки назначаются гемостатические, антибактериальные, противовоспалительные, анальгезирующие препараты, средства для стабилизации гемодинамики. Объем операции зависит от особенностей повреждения. При внутрибрюшинных разрывах мочевой пузырь перед ушиванием раны экстраперитонизируют для прекращения подтекания мочи и проведения полноценной ревизии, после реконструкции поврежденного органа брюшную полость в обязательном порядке санируют.
Внебрюшинные повреждения ушивают без экстраперитонизации. Вне зависимости от типа травмы после восстановления целостности стенки мужчинам накладывают эпицистостому, женщинам устанавливают уретральный катетер. Брюшную или тазовую полость дренируют. После операции продолжают введение антибиотиков, анальгетиков, противошоковую инфузионную терапию.
Прогноз и профилактика
Нарушения целостности стенок мочевого пузыря обоснованно считаются тяжелыми, прогностически неблагоприятными травмами. Соблюдение алгоритма хирургического лечения больных обеспечивает достоверное снижение частоты осложнений даже при тяжелых повреждениях. Профилактика направлена на создание безопасных производственных условий, соблюдение правил дорожного движения, выполнение требований безопасности при занятиях травмоопасными хобби и видами спорта, отказ от злоупотребления алкоголем. Для уменьшения предпосылок к травматизму пациентам с диагностированными заболеваниями простаты, уретры, мочевого пузыря рекомендуется регулярное наблюдение и лечение у уролога.
Травма почки встречается наиболее часто и составляет около 60-65 % в структуре повреждений органов мочевой системы. В мирное время превалируют закрытые, а в военное - открытые повреждения почек.
Этиология и патогенез. Закрытые повреждения почек, как правило, наступают в результате приложения силы в область поясницы или живота в виде удара или сдавливания. В механизме разрыва играет роль и гидродинамический фактор, обусловленный значительным преобладанием в паренхиме почки жидкостного компонента (кровь, лимфа, моча), окруженного плотной фиброзной капсулой. Непосредственный удар и детонация жидкости внутри органа приводят к разрыву фиброзной капсулы и паренхимы почки. В бытовых условиях травма чаще возникает вследствие падения поясничной областью на выступающий твердый предмет. Разрыв органа происходит в результате непосредственного удара и повреждающего действия, расположенных рядом костных структур - ребер и позвоночника. Повреждения почек могут возникать в результате малоинвазивных и эндоскопических методов диагностики и лечения урологических заболеваний, получивших в настоящее время широкое распространение. Прежде всего, они связаны с неосторожными или ошибочными действиями врача. После дистанционной ударно-волновой нефролитотрипсии нередко диагностируются субкапсулярные гематомы, а всегда возникающая после нее гематурия может быть следствием не только повреждающего действия на уротелий камня и его фрагментов, но и разрывов форниксов. Травма почечной паренхимы может наблюдаться при катетеризации (стентировании) мочеточника, уретероскопии, нефроскопии, нефробиопсии и даже при паранефральной блокаде. Заболевания почки (опухоль, киста, гидронефроз) делают ее более подверженной различным травмирующим воздействиям. Тяжелые повреждения патологически измененной почки могут наступить даже при минимальной травме.
Открытые повреждения - ножевые или огнестрельные - обычно носят множественный характер.
Классификация. Клинико-анатомическая классификация закрытых повреждений почки строится на степени тяжести травмы органа. Различают ушибы и разрывы почки. Ушиб характеризуется резким сотрясением (контузией) органа без разрывов паренхимы почки, ее капсулы и полостной системы. Клинически значимое повреждение почки наблюдается только при ее разрывах, от микроскопических надрывов паренхимы и форниксов до размозжения органа. С этих позиций появление субкапсулярных и околопочечных гематом, а также гематурии всегда является следствием пусть даже незначительных, но разрывов паренхимы.
Классификация разрывов почки: а - наружный разрыв паренхимы почки с образованием субкапсулярной гематомы; б - наружный разрыв паренхимы и капсулы почки с образованием паранефральной гематомы; в - внутренний разрыв паренхимы и форниксов, открывающийся в полостную систему почки (гематурия); г - проникающий разрыв капсулы, паренхимы и полостной системы почки с образованием паранефральной урогематомы (гематурия); д - размозжение почки: множественные проникающие разрывы капсулы, паренхимы и полостной системы почки с образование паранефральной урогематомы (гематурия); е - отрыв сосудистой ножки с размозжением паренхимы почки.
Наиболее тяжелыми формами повреждений почки являются ее размозжение, то есть образование множественных, проникающих в чашечно-лоханочную систему разрывов органа с возможным отрывом участков паренхимы (полюса), и разрыв (отрыв) сосудистой ножки. Последний не имеет клинического значения, так как почти всегда сочетается с не менее тяжелыми повреждениями других органов, что делает такого рода повреждения несовместимыми с жизнью.
Клиническая картина зависит от степени повреждения почки и наличия травм других органов. Больные жалуются на боли в поясничной области и/или в животе, усиливающиеся при глубоком дыхании, вздутие живота, тошноту, рвоту, общую слабость. Тотальная гематурия наблюдается при тяжелых повреждениях почек. Макрогематурия служит признаком степени выраженности повреждения органа, в свою очередь, являясь одним из определяющих факторов тяжести состояния пострадавшего. Вместе с тем в ряде случаев степень гематурии не соответствует степени повреждения почки. При небольших форникальных разрывах может наблюдаться стойкая выраженная гематурия, и, наоборот, при размозжении почки гематурия может быть незначительной либо отсутствовать в результате тампонады полостной системы сгустками крови и/или повреждения лоханки, мочеточника и ее сосудистой ножки.
Разрыв богатого сосудами паренхиматозного органа, каким является почка, сопровождается признаками внутреннего кровотечения. В сочетании с выраженной гематурией оно может быстро привести к анемизации и тяжелому состоянию больного, что проявляется бледностью кожных покровов, холодным потом, тахикардией, снижением артериального давления, нарастанием забрюшинной урогематомы. При объективном исследовании на коже живота и поясничной области могут определяться ссадины, кровоизлияния, отечность тканей, а также выбухание в данной области, обусловленное урогематомой больших размеров. Расположение и ход раневого канала с истечением из него мочи позволяют заподозрить открытое повреждение почки. Пальпация грудной клетки и позвоночника может сопровождаться резкой болезненностью вследствие перелома этих костных образований. При пальпации живота определяются болезненность и защитное напряжение мышц на стороне поражения, а при больших урогематомах - округлое образование в подреберье и поясничной области. Отдаленными осложнениями закрытых повреждений почек являются организовавшаяся, сдавливающая почку гематома, камнеобразование, гидронефроз, артериальная гипертензия и др.
Диагностика. В диагностике обращают внимание на вид и характер травмы, ее объективные местные и общие проявления. В анализах крови определяется снижение количества эритроцитов и гемоглобина, в более поздние сроки с момента травмы присоединяется лейкоцитоз. В анализе мочи эритроциты покрывают все поле зрения. Суммарную функцию почек позволяет оценить определение остаточного азота, мочевины и креатинина сыворотки крови, что особенно важно знать при повреждении единственной почки и планировании оперативного лечения. Основными в постановке диагноза разрыва почки являются лучевые методы. Они позволяют, во-первых, определить степень повреждения почки, во-вторых, оценить раздельную функцию поврежденной и контрлатеральной почек, в-третьих, отслеживать динамику раневого процесса с целью ранней диагностики осложнений и производить их своевременную коррекцию. Наиболее доступный, малоинвазивный и быстрый метод диагностики повреждений почек - УЗИ. С его помощью можно выявить субкапсулярные и паранефральные урогематомы, определить размеры, деформацию контуров почки, дефекты паренхимы, деформацию чашечно-лоханочной системы, степень ее эктазии, обнаружить сгустки крови. Сопоставление результатов УЗИ с анамнезом, данными физикального обследования и степенью выраженности кровотечения нередко позволяет установить диагноз и при тяжелом состоянии больного приступить к экстренной операции без других методов обследования. Во всех случаях больным с подозрением на травму почек следует выполнить обзорную рентгенографию брюшной полости и забрюшинного пространства. С ее помощью можно выявить сколиоз, отсутствие контура почки и большой поясничной мышцы, переломы нижних ребер, поперечных отростков позвонков и костей таза. Экскреторная урография позволяет обнаружить деформацию и сдавливание чашечек и лоханки, затеки контраста на стороне поражения, оценить функцию поврежденной и контрлатеральной почек, что важно при определении объема экстренного оперативного вмешательства. Применение ее ограничено в случаях сочетанных повреждений и у пострадавших с шоком и нестабильной гемодинамикой (систолическое давление ниже 90 мм рт. ст. ). В настоящее время ретроградная уретеропиелография в диагностике повреждений почек применяется крайне редко в связи с появлением новых методов исследования. Ее можно использовать для уточнения степени повреждения почки, при неинформативности экскреторной урографии и недоступности КТ, МРТ и ангиографии в связи с экстренностью ситуации или отсутствием их в данном стационаре.
Наиболее информативными методами диагностики повреждений почек являются КТ и МРТ. При введении в вену рентгеноконтрастных веществ, как правило, исключается необходимость использования других лучевых методов. КТ и МРТ обеспечивают наивысшую степень точности в оценке анатомических деталей травмированной почки. В практике неотложной помощи их точность достигает 98 %. КТ позволяет визуализировать повреждения паренхимы и сосудов почки, сегментов органа, лишенных кровоснабжения, и обнаружить даже небольшие мочевые затеки, содержащие рентгеноконтрастное вещество (экстравазаты), а также травму других паренхиматозных органов. С помощью КТ и МРТ можно выявить повреждения почки в результате эндоурологических вмешательств.
Ангиография почек позволяет помимо диагностики повреждения сосудов и паренхимы почки выполнить лечебную процедуру - селективную эмболизацию кровоточащего сосуда. Радиоизотопное сканирование в системе неотложной диагностики ренальных травм менее информативно, чем лучевые методы, требует много времени и специальных условий. Данный метод более целесообразен для оценки последствий перенесенной травмы почек и их функционального состояния.
+Оказание неотложной помощи на догоспитальном этапе при признаках травматического шока и внутреннего кровотечения сводится к противошоковым мероприятиям и к введению гемостатиков (адроксоний, викасол), а также сердечно-сосудистых средств. При изолированных повреждениях почки, субкапсулярных лечебные мероприятия на месте сводятся к введению спазмолитиков, а иногда промедола и других наркотических средств, сердечно-сосудистых препаратов. Эти мероприятия могут быть продолжены и в машине скорой помощи. При тяжелых повреждениях почки с разрывами ее кровотечение продолжается. Необходимо начать капельное введение кровезамещающих и противошоковых растворов, которое нужно продолжить и в стационаре, где возможна и гемотрансфузия. В стационаре хирургическая тактика двоякая. Она зависит от тяжести травмы. При субкапсулярном повреждении проводится консервативная терапия (гемостатические и антибактериальные препараты), назначается строгий постельный режим в течение 3 нед. При разрыве почки производится неотложное оперативное вмешательство, объем которого зависит от степени повреждения (нефрэктомия, резекция нижнего полюса, первичный шов). Основная задача врача скорой помощи - своевременно доставить пострадавшего в стационар, где есть урологическое отделение. При транспортировке проводятся противошоковые мероприятия.
Травма мочевого пузыря — это нарушение целостности стенки органа, вызванное механической травмой, воздействием химических веществ, редко – давлением мочи при некоторых заболеваниях. Проявляется болью в животе, припухлостью и синюшностью кожи над лоном, учащенными ложными позывами к мочеиспусканию, снижением или отсутствием диуреза, макрогематурией, подтеканием мочи из раневого отверстия, нарастанием симптоматики травматического шока. Диагностируется с помощью ретроградной цистографии, катетеризации, УЗИ, КТ, МРТ мочевого пузыря, общего анализа мочи, лапароскопии. В легких случаях возможно консервативное ведение с установкой катетера, при внутрибрюшинных и крупных внебрюшинных разрывах выполняется реконструктивная пластика органа.
• Причины
• Патогенез
• Классификация
• Симптомы
• Осложнения
• Диагностика
• Лечение травмы мочевого пузыря
• Прогноз и профилактика
• Цены на лечение
Общие сведения
В структуре общего травматизма механические повреждения мочевого пузыря составляют от 0, 4 до 15% (в России — от 1 до 7%). В последние годы отмечается более частое травмирование органа, что связано с усилением интенсивности транспортного сообщения, износом автопарка, увеличением количества тяжелых техногенных катастроф и локальных военных конфликтов.
Пик травматизации наблюдается в 21-50-летнем возрасте, около 75% пострадавших — мужчины. Особенностью травм является преимущественно сочетанный характер поражения (в 100% открытых ранений и в 85% тупых травм кроме мочевого пузыря повреждаются кости таза, позвоночник, другие органы). Актуальность своевременной диагностики и экстренных лечебных мероприятий обусловлена неблагоприятным прогнозом – в соответствии с оценочными шкалами 31, 4% пострадавших относятся к категории тяжелых, 49, 2% — крайне тяжелых больных, уровень смертности превышает 25%.
Причины
У большинства пациентов травматическое повреждение мочевого пузыря связано с воздействием на его стенку внешних механических факторов различного происхождения. В редких случаях травма обусловлена влиянием агрессивных химических веществ, инсталлированных в мочевой пузырь, или наличием заболеваний, препятствующих мочеиспусканию. Причинами травм являются:
• Дорожно-транспортные происшествия. Более чем в четверти случаев мочевой пузырь травмируется во время ДТП. Повреждение возникает при прямом ударе в проекцию органа, сильном сдавлении в транспортном средстве, ранении осколками тазовых костей, конструктивными элементами автомобиля, предметами окружающей среды.
• Ятрогенные факторы. 22-23% пациентов получают травму во время медицинских манипуляций. Стенка органа может повреждаться при его катетеризации, бужировании уретры, выполнении операций — трансуретральных вмешательств, кесарева сечения, экстирпации матки, миомэктомии, аденомэктомии, резекции толстой кишки и др.
• Бытовой и производственный травматизм. В 10% случаев повреждение происходит из-за падения с высоты на твердый предмет. При наличии предпосылок (переполнении мочой, рубцовых изменениях и др. ) возможен разрыв органа из-за резкого сотрясения тела при прыжке. У 4, 2% пострадавших травма возникает под действием производственных факторов.
• Насильственные действия. Целостность мочевого пузыря может нарушаться при тупых ударах в живот, ранении ножом или другими острыми предметами в драках, при криминальных абортах. В военное время в 3-4 раза увеличивается количество огнестрельных травм и открытых ранений органа осколками взрывных боеприпасов.
• Урологические заболевания. Крайне редко самопроизвольный разрыв мочевого пузыря отмечается у пациентов, которые страдают заболеваниями, нарушающими мочеиспускание, — аденомой и раком простаты, стенозом уровезикальной шейки, стриктурами уретры. Чаще урологическая патология играет роль предрасполагающего фактора, усиливая растяжение органа.
Риск возникновения наиболее тяжелых повреждений — частичных или полных разрывов — зависит не только от силы травматического воздействия, но и от места его приложения, направления, внезапности. Вероятность получения травмы существенно возрастает при алкогольном опьянении, которое способствует переполнению мочевого пузыря из-за притупления позывов к мочеиспусканию и провоцирует травмоопасное поведение. Предполагающими факторами также являются опухолевые поражения, фиброзные изменения стенки органа после перенесенных операций, лучевой терапии, воспалительных заболеваний.
Патогенез
Механизм травмы мочевого пузыря зависит от типа факторов, вызвавших повреждение. При тупом ударе в надлобковую область, противоударе о крестец, сдавлении резко повышается внутрипузырное давление, усиливается нагрузка на мочепузырную стенку. Возникновение гидродинамического эффекта способствует внутрибрюшинному разрыву органа на участке наименее развитой мускулатуры (обычно по задней стенке пузыря возле его верхушки).
Рана обычно рваная, с неровными краями. При меньшей силе механического воздействия удар вызывает закрытые повреждения (ушибы, кровоизлияния в стенку). Аналогичный патогенез характерен при наличии урологических заболеваний с нарушением пассажа мочи. Значительное смещение пузыря при механических травмах приводит к резкому натяжению поддерживающих боковых и пузырно-простатических связок с внебрюшинным разрывом мягко-эластичной стенки органа. Сильный удар способен вызвать разрыв связок, мочепузырных кровеносных сосудов, отрыв шейки.
При закрытых и открытых повреждениях везикальных оболочек острыми предметами, инструментами, осколками костей происходит поверхностное, глубокое надсечение или сквозное рассечение стенки. Рана при этом обычно линейная. Сочетание с гидродинамическим ударом при огнестрельных и оскольчатых ранениях приводит к дополнительным радиальным надрывам круглого раневого отверстия.
Классификация
Критериями систематизации травматических повреждений являются степень тяжести, возможное сообщение с окружающей средой, расположение разрыва по отношению к брюшине, сочетание с травмами других органов. Такой подход позволяет спрогнозировать течение патологического процесса и вероятные осложнения, выбрать оптимальную тактику ведения пациента. В зависимости от тяжести повреждения мочепузырной стенки травмы могут быть глухими (ушиб, поверхностное ранение наружной оболочки, надрыв слизистой) или сквозными (полный разрыв, отрыв шейки). В свою очередь, сквозные повреждения разделяют на три группы:
• Интраперитонеальные разрывы. Наблюдаются более чем у 60% пострадавших. Обычно обусловлены прямыми ударами в переполненный мочевой пузырь. Из-за истечения мочи в брюшную полость быстро осложняются перитонитом.
• Экстраперитонеальные разрывы. Возникают в 28% случаев. Чаще провоцируются избыточным натяжением поддерживающего связочного аппарата. Травмированный мочевой пузырь не сообщается с брюшной полостью, моча истекает в малый таз.
• Комбинированные разрывы. Наблюдаются у 10% пострадавших. Множественное повреждение стенки органа обычно сочетается с переломами тазовых костей. Сообщение между мочевым пузырем, брюшной и тазовой полостями обуславливает особую тяжесть патологии.
До 90% травм мирного времени являются закрытыми, благодаря сохранению целостности кожи поврежденный мочевой пузырь не сообщается с внешней средой. В военный период, при насильственных действиях с использованием холодного и огнестрельного оружия возрастает частота открытых травм, при которых нарушается целостность кожи, возникает сообщение между оболочками или полостью органа и окружающей средой. По наблюдениям специалистов в сферах травматологии и клинической урологии, сочетанные повреждения превалируют над изолированными. У 40-42% пациентов выявляются переломы костей таза, у 4-10% — разрывы кишечника, у 8-10% — травмы других внутренних органов.
Симптомы
Важная клиническая особенность данного повреждения — частое преобладание общей симптоматики над локальной. Из-за выраженного болевого синдрома и кровотечения у пострадавших нарастают признаки гемодинамических нарушений, у 20, 3% наблюдается травматический шок: снижается уровень АД, ускоряется частота сердечных сокращений, кожные покровы бледнеют, покрываются липким холодным потом, возникает слабость, головокружение, оглушенность, спутанность, а затем и потеря сознания.
Из-за раздражения брюшины мочой пациенты с интраперитонеальными разрывами ощущают интенсивную боль в надлонной области, в нижней части брюшной полости, которая впоследствии распространяется на весь живот, сопровождается тошнотой, рвотой, задержкой газов и стула, напряжением брюшной мускулатуры. Специфические симптомы травмы мочепузырной стенки — боль и локальные изменения области повреждения, дизурия. При открытых ранениях на передней стенке живота, реже — в зоне промежности выявляется зияющая рана, из которой может истекать моча.
Для закрытых внебрюшинных травм характерно образование болезненной припухлости над лобком, в паху, синюшный цвет кожных покровов из-за их пропитывания кровью. Пострадавшие испытывают частые ложные позывы к мочеиспусканию со значительным уменьшением либо полным отсутствием диуреза, выделением капель крови из мочеиспускательного отверстия. При сохранении мочевыделения у пациентов с надрывами слизистой моча окрашена кровью.
Осложнения
Летальность при травматических повреждениях мочевого пузыря, особенно открытых и сочетанных, достигает 25% и более. Причинами смерти обычно являются запущенные формы перитонита, болевой, инфекционно-токсический, геморрагический шок, сепсис. Сквозные травмы стенки мочевого пузыря быстро осложняются вовлечением в процесс других органов. Анатомические особенности паравезикальной, забрюшинной клетчатки, фасциальных пространств способствуют мочевой инфильтрации, распространению затеков, образованию урогематом.
При внутрибрюшинном разрыве возникает уроасцит. Вторичное инфицирование приводит к формированию абсцессов, флегмон. У 28, 3% пациентов развивается мочевой перитонит, у 8, 1% — уросепсис. Восходящее распространение инфекции провоцирует начало острого пиелонефрита. В 30% случаев при сочетании травмы пузыря с повреждениями других органов наблюдается ДВС-синдром. В отдаленном периоде у больных иногда формируются мочевые свищи, наблюдается недержание мочи.
Диагностика
С учетом серьезности прогноза всем пациентам с подозрением на травму мочевого пузыря назначают комплексное обследование, позволяющее выявить разрывы мочепузырной стенки, определить их особенности и количество, обнаружить возможное повреждение смежных органов. Рекомендованными методами лабораторной и инструментальной диагностики являются:
• Общий анализ мочи. Исследование удается провести только при сохраненном мочеиспускании. Объем разовой порции зачастую уменьшен. В анализе в большом количестве присутствуют эритроциты, подтверждающие наличие кровотечения.
• УЗИ. По данным эхографии мочевого пузыря, орган обычно уменьшен в объеме, рядом с ним определяются скопления крови. Исследование дополняют УЗИ почек, при проведении которого обнаруживаются признаки постренального нарушения оттока мочи, и УЗИ брюшной полости для выявления свободной жидкости.
• Рентген. Ретроградная цистография считается «золотым стандартом» диагностики этого вида травм. Разрывы органа проявляются затеками рентгеноконтрастного вещества в пузырно-прямокишечную ямку, околопузырную клетчатку, область крыльев подвздошной кости, полость брюшины.
• Томография мочевого пузыря. С помощью КТ удаётся получить трехмерное изображение поврежденного органа, в ходе МРТ он изучается послойно. Результаты томографии позволяют точно оценить повреждения, объем урогематом, выявить сочетанные травмы.
• Диагностическая лапароскопия. Осмотр мочевого пузыря через лапароскоп дает возможность определить особенности травмированной стенки, обнаружить затеки мочи, крови. При выполнении лапароскопии визуализируются повреждения соседних органов.
Большое диагностическое значение играет катетеризация мочевого пузыря, дополненная вливанием в него жидкости (проба Зельдовича). О наличии разрывов свидетельствует отсутствие мочевыделения через катетер или поступление небольшого количества мочи с кровью. Жидкость, введенная в травмированный орган, обратно выделяется слабой струей и не в полном объеме. При интраперитонеальных разрывах возможно отхождение в 2-3 раза большего объема жидкости, что обусловлено проникновением катетера в брюшную полость и выделением ранее попавшей в нее мочи.
Экскреторную урографию назначают с осторожностью, чтобы не спровоцировать развитие контраст-индуцированной нефропатии на фоне шоковых изменений гемодинамики. Цистоскопия обычно не проводится из-за риска занесения инфекции. В общем анализе крови определяются признаки анемии — эритропения, снижение уровня гемоглобина, возможен умеренный лейкоцитоз и повышение СОЭ.
Дифференциальная диагностика проводится с повреждением заднего отдела уретры, травмами печени, селезенки, различных отделов кишечника, разрывами сосудов брыжейки. Кроме врача-уролога пациента осматривает травматолог, хирург, анестезиолог-реаниматолог, терапевт, по показаниям — проктолог, гинеколог, кардиолог, гастроэнтеролог, невропатолог, нейрохирург.
Травма почки встречается наиболее часто и составляет около 60-65 % в структуре повреждений органов мочевой системы. В мирное время превалируют закрытые, а в военное - открытые повреждения почек.
Этиология и патогенез. Закрытые повреждения почек, как правило, наступают в результате приложения силы в область поясницы или живота в виде удара или сдавливания. В механизме разрыва играет роль и гидродинамический фактор, обусловленный значительным преобладанием в паренхиме почки жидкостного компонента (кровь, лимфа, моча), окруженного плотной фиброзной капсулой. Непосредственный удар и детонация жидкости внутри органа приводят к разрыву фиброзной капсулы и паренхимы почки. В бытовых условиях травма чаще возникает вследствие падения поясничной областью на выступающий твердый предмет. Разрыв органа происходит в результате непосредственного удара и повреждающего действия, расположенных рядом костных структур - ребер и позвоночника. Повреждения почек могут возникать в результате малоинвазивных и эндоскопических методов диагностики и лечения урологических заболеваний, получивших в настоящее время широкое распространение. Прежде всего, они связаны с неосторожными или ошибочными действиями врача. После дистанционной ударно-волновой нефролитотрипсии нередко диагностируются субкапсулярные гематомы, а всегда возникающая после нее гематурия может быть следствием не только повреждающего действия на уротелий камня и его фрагментов, но и разрывов форниксов. Травма почечной паренхимы может наблюдаться при катетеризации (стентировании) мочеточника, уретероскопии, нефроскопии, нефробиопсии и даже при паранефральной блокаде. Заболевания почки (опухоль, киста, гидронефроз) делают ее более подверженной различным травмирующим воздействиям. Тяжелые повреждения патологически измененной почки могут наступить даже при минимальной травме.
Открытые повреждения - ножевые или огнестрельные - обычно носят множественный характер.
Классификация. Клинико-анатомическая классификация закрытых повреждений почки строится на степени тяжести травмы органа. Различают ушибы и разрывы почки. Ушиб характеризуется резким сотрясением (контузией) органа без разрывов паренхимы почки, ее капсулы и полостной системы. Клинически значимое повреждение почки наблюдается только при ее разрывах, от микроскопических надрывов паренхимы и форниксов до размозжения органа. С этих позиций появление субкапсулярных и околопочечных гематом, а также гематурии всегда является следствием пусть даже незначительных, но разрывов паренхимы.
Классификация разрывов почки: а - наружный разрыв паренхимы почки с образованием субкапсулярной гематомы; б - наружный разрыв паренхимы и капсулы почки с образованием паранефральной гематомы; в - внутренний разрыв паренхимы и форниксов, открывающийся в полостную систему почки (гематурия); г - проникающий разрыв капсулы, паренхимы и полостной системы почки с образованием паранефральной урогематомы (гематурия); д - размозжение почки: множественные проникающие разрывы капсулы, паренхимы и полостной системы почки с образование паранефральной урогематомы (гематурия); е - отрыв сосудистой ножки с размозжением паренхимы почки.
Наиболее тяжелыми формами повреждений почки являются ее размозжение, то есть образование множественных, проникающих в чашечно-лоханочную систему разрывов органа с возможным отрывом участков паренхимы (полюса), и разрыв (отрыв) сосудистой ножки. Последний не имеет клинического значения, так как почти всегда сочетается с не менее тяжелыми повреждениями других органов, что делает такого рода повреждения несовместимыми с жизнью.
Клиническая картина зависит от степени повреждения почки и наличия травм других органов. Больные жалуются на боли в поясничной области и/или в животе, усиливающиеся при глубоком дыхании, вздутие живота, тошноту, рвоту, общую слабость. Тотальная гематурия наблюдается при тяжелых повреждениях почек. Макрогематурия служит признаком степени выраженности повреждения органа, в свою очередь, являясь одним из определяющих факторов тяжести состояния пострадавшего. Вместе с тем в ряде случаев степень гематурии не соответствует степени повреждения почки. При небольших форникальных разрывах может наблюдаться стойкая выраженная гематурия, и, наоборот, при размозжении почки гематурия может быть незначительной либо отсутствовать в результате тампонады полостной системы сгустками крови и/или повреждения лоханки, мочеточника и ее сосудистой ножки.
Разрыв богатого сосудами паренхиматозного органа, каким является почка, сопровождается признаками внутреннего кровотечения. В сочетании с выраженной гематурией оно может быстро привести к анемизации и тяжелому состоянию больного, что проявляется бледностью кожных покровов, холодным потом, тахикардией, снижением артериального давления, нарастанием забрюшинной урогематомы. При объективном исследовании на коже живота и поясничной области могут определяться ссадины, кровоизлияния, отечность тканей, а также выбухание в данной области, обусловленное урогематомой больших размеров. Расположение и ход раневого канала с истечением из него мочи позволяют заподозрить открытое повреждение почки. Пальпация грудной клетки и позвоночника может сопровождаться резкой болезненностью вследствие перелома этих костных образований. При пальпации живота определяются болезненность и защитное напряжение мышц на стороне поражения, а при больших урогематомах - округлое образование в подреберье и поясничной области. Отдаленными осложнениями закрытых повреждений почек являются организовавшаяся, сдавливающая почку гематома, камнеобразование, гидронефроз, артериальная гипертензия и др.
Диагностика. В диагностике обращают внимание на вид и характер травмы, ее объективные местные и общие проявления. В анализах крови определяется снижение количества эритроцитов и гемоглобина, в более поздние сроки с момента травмы присоединяется лейкоцитоз. В анализе мочи эритроциты покрывают все поле зрения. Суммарную функцию почек позволяет оценить определение остаточного азота, мочевины и креатинина сыворотки крови, что особенно важно знать при повреждении единственной почки и планировании оперативного лечения. Основными в постановке диагноза разрыва почки являются лучевые методы. Они позволяют, во-первых, определить степень повреждения почки, во-вторых, оценить раздельную функцию поврежденной и контрлатеральной почек, в-третьих, отслеживать динамику раневого процесса с целью ранней диагностики осложнений и производить их своевременную коррекцию. Наиболее доступный, малоинвазивный и быстрый метод диагностики повреждений почек - УЗИ. С его помощью можно выявить субкапсулярные и паранефральные урогематомы, определить размеры, деформацию контуров почки, дефекты паренхимы, деформацию чашечно-лоханочной системы, степень ее эктазии, обнаружить сгустки крови. Сопоставление результатов УЗИ с анамнезом, данными физикального обследования и степенью выраженности кровотечения нередко позволяет установить диагноз и при тяжелом состоянии больного приступить к экстренной операции без других методов обследования. Во всех случаях больным с подозрением на травму почек следует выполнить обзорную рентгенографию брюшной полости и забрюшинного пространства. С ее помощью можно выявить сколиоз, отсутствие контура почки и большой поясничной мышцы, переломы нижних ребер, поперечных отростков позвонков и костей таза. Экскреторная урография позволяет обнаружить деформацию и сдавливание чашечек и лоханки, затеки контраста на стороне поражения, оценить функцию поврежденной и контрлатеральной почек, что важно при определении объема экстренного оперативного вмешательства. Применение ее ограничено в случаях сочетанных повреждений и у пострадавших с шоком и нестабильной гемодинамикой (систолическое давление ниже 90 мм рт. ст. ). В настоящее время ретроградная уретеропиелография в диагностике повреждений почек применяется крайне редко в связи с появлением новых методов исследования. Ее можно использовать для уточнения степени повреждения почки, при неинформативности экскреторной урографии и недоступности КТ, МРТ и ангиографии в связи с экстренностью ситуации или отсутствием их в данном стационаре.
Наиболее информативными методами диагностики повреждений почек являются КТ и МРТ. При введении в вену рентгеноконтрастных веществ, как правило, исключается необходимость использования других лучевых методов. КТ и МРТ обеспечивают наивысшую степень точности в оценке анатомических деталей травмированной почки. В практике неотложной помощи их точность достигает 98 %. КТ позволяет визуализировать повреждения паренхимы и сосудов почки, сегментов органа, лишенных кровоснабжения, и обнаружить даже небольшие мочевые затеки, содержащие рентгеноконтрастное вещество (экстравазаты), а также травму других паренхиматозных органов. С помощью КТ и МРТ можно выявить повреждения почки в результате эндоурологических вмешательств.
Ангиография почек позволяет помимо диагностики повреждения сосудов и паренхимы почки выполнить лечебную процедуру - селективную эмболизацию кровоточащего сосуда. Радиоизотопное сканирование в системе неотложной диагностики ренальных травм менее информативно, чем лучевые методы, требует много времени и специальных условий. Данный метод более целесообразен для оценки последствий перенесенной травмы почек и их функционального состояния.
№18. Мочекаменная болезнь (уролитиаз) – хроническое заболевание, характеризующееся образованием в почках и мочевых путях камней, имеющие различный состав (фосфаты, ураты, оксалаты и тд. ).
Этиология:
Каузальный генез.
1. Экзогенные:
климатические условия (недостаток УФ-лучей, дефицит витамина D; жара, способствующая обезвоживанию), физико-химические свойства воды;
особенности питания (острая и кислая пища повышает кислотность мочи), чрезмерное и однообразное потребление с пищей большого количества камнеобразующих веществ;
условия быта (однообразный, малоподвижный образ жизни и отдыха);
условия труда (вредные производства, горячие цеха, тяжелый физический труд и др. );
состав питьевой воды (жесткая вода с большим содержанием кальциевых солей).
2. Эндогенные:
Гиперфункция (усиление деятельности органа) околощитовидных желез — гиперпаратиреоз.
Хронические заболевания желудочно-кишечного тракта (гастрит, язвенная болезнь желудкаидвенадцатиперстной кишки).
Костные травмы.
Нарушение барьерных функций печени.
Врожденные или приобретенные энзимопатии (недостаток тех или иных ферментов в организме).
3. Местные (в почках):
факторы, приводящие к застою мочи: например, гидронефроз(расширение почки в связи с нарушением оттока мочи), аденома предстательной железы(доброкачественная опухоль предстательной железы);
воспалительные заболевания почек, например, пиелонефрит(воспаление почек на фоне бактериальной инфекции);
нефроптоз(опущение почки);
нарушение кровоснабжения почки вследствие травмы, шока, кровотечения;
инфекции мочевыводящих путей.
Классификация конкрементов:
Мочекислые камни (ураты) – желто-коричневого цвета, плотной консистенции, с гладкой или мелкозернистой поверхностью.
Кальций-оксалатные камни – темно-бурого, почти черного цвета, очень плотные, с шероховатой поверхностью, усеянной «шипами».
Кальциево-фосфатные камни (инфицированные) – серовато-белого цвета, мягкие, с шероховатой поверхностью, легко крошатся.
Смешанные камни – ядро образуется из одних солей, а оболочка – из других.
Цистиновые камни – светло-коричневого цвета, с гладкой поверхностью.
Вид камня косвенно дает представление о нарушениях обменных процессов, происходящих в организме.
Патогенез: Выше обозначенные факторы приводят к изменению концентрации мочи, ее pH и коллоидного равновесия, что приводит к образованию камня.
По локализации в органах мочевой системы различают:
камни почечной лоханки и чашечек (нефролитиаз),
мочеточников (уретеролитиаз),
мочевого пузыря (цистолитиаз),
уретры (уретролитиаз),
мультифокальный литиаз (различные сочетания указанных локализаций).
по течению:
первичное образование камней (при отсутствии внутренних располагающих факторов, например – нарушение кровоснабжения, аденома простаты),
вторичное образование камней (наличие факторов, способствующих образованию камней, например факторы препятствующие оттоку мочи-гидронефроз).
Клиническая картина:
Почечная колика (боль возникает внезапно, остро, в любое время суток, боль появляется и в покое, и при движении, изменение положения тела не приносит никакого облегчения. Причина - резкое прекращение оттока мочи в следствие закупорки камнем, повышение внутрилоханочного давления, расстройство микроциркуляции почки). Может сопровождаться тошнотой, рвотой, метеоризмом (расстройства со стороны ЖКТ обусловлено рефлекторным раздражением задней париетальной брюшины, прилежащей к передней поверхности почки и лоханки).
Беспокойное поведение. Боли от нескольких часов до нескольких дней с периодическими спадами.
Гематурия отмечается у 75-90 % больных уролитиазом и по большей части носит микроскопический характер. Поступление крови в мочу, так же как и боль, увеличивается при движениях. При камнях почек и мочеточников имеет место тотальная гематурия, а при конкрементах мочевого пузыря наблюдается терминальная гематурия, сопровождающаяся дизурическими явлениями. Гематурия отсутствует при полной обтурации мочеточника камнем, вследствие чего моча из блокированной почки в мочевой пузырь не поступает.
Отхождение камней с мочой является достоверным признаком МКБ. Оно наблюдается у 10-15 % больных уролитиазом. После отхождения камня болевой синдром купируется. Размеры отходящих с мочой конкрементов невелики и колеблются от 0, 2 до 1 см в диаметре. У некоторых больных камни выделяются многократно, в течение длительного времени. Трудно различить тени конкрементов, если они проецируются на кости скелета. Иногда с помощью обзорной рентгенограммы по плотности получаемых теней, их поверхности, величине и форме можно судить даже о химическом составе камня. Эти тени необходимо дифференцировать с тенями от камней желчного пузыря, флеболитов, каловых камней, обызвествленных лимфатических и мио-матозных узлов, очагов поражения при туберкулезе почек, новообразованиях, эхинококкозе и др. Целесообразно выполнение многоосевых рентгеновских снимков (полубоковых, боковых, в положении больного на животе и др. ).
Диагностика:
Сбор анамнеза (характер и длительность болей, сопровождаются тошнотой, рвотой, ознобом, наличие гематурии, отходили ли камни раньше, наследственность).
Осмотр, пальпация (живота, почек, наружных половых органов), глубокая пальпация. Синдром Пастернацкого.
Анализ крови (лейкоцитоз со сдвигом лейкоцитарной формулы влево, повышение СОЭ, ), мочи (умеренное количество белка, единичные цилиндры, лейкоциты, эритроциты, бактерии. Показатель кислотности мочи. Изучают выведение продуктов азотистого обмена (мочевины, креатинина, мочевой кислоты) и электролитов (натрия, калия, кальция, фосфора, хлора, магния Постоянное присутствие кристаллов солей в моче указывает на склонность к образованию камней и их возможный состав).
УЗИ позволяет оценить форму, величину и положение почек, их подвижность, определить локализацию камня и его размеры, степень расширения полостной системы почки и состояние ее паренхимы.
Обзорная и экскреторная урография. Обзорный снимок почек и мочевых путей при обследовании больных с МКБ должен всегда предшествовать рентгеноконтрастным методам исследования. На обзорной рентгенограмме определяют разнообразные по форме, количеству и величине тени, располагающиеся в области проекции почек и мочевыводящих путей. Экскреторная урография позволяет подтвердить или исключить принадлежность тени, выявленной на обзорном снимке, мочевым путям, уточнить локализацию камня, выявить наличие рентгенонегативных конкрементов и получить информацию о раздельном функциональном состоянии почек и мочевых путей.
КТ позволяет уточнить локализацию, особенно рентгенонегативных камней, определить их плотность, изучить состояние почек и мочевых путей. Информативность метода возрастает при использовании таких его модификаций, как спиральная и мультиспиральная КТ с трехмерной реконструкцией изображения и виртуальной эндоскопией.
МРТ позволяет выявить уровень обструкции мочевых путей камнем без использования контрастных веществ, в том числе у пациентов с почечной коликой.
Хромоцистоскопия - наиболее простой, быстрый и достаточно информативный метод определения раздельной функции почек. Он имеет большое значение в дифференциальной диагностике почечной колики с острыми хирургическими заболеваниями органов брюшной полости. Если тень, подозрительная на конкремент, вызывает сомнения, прибегают к катетеризации. При этом катетер может или остановиться около конкремента, или после ощущения препятствия его удается провести выше. После введения катетера производят рентгеновские снимки соответствующего отдела мочевых путей в двух проекциях. Если на рентгенограммах подозрительная на конкремент тень и тень катетера совмещаются, это свидетельствует о камне мочеточника. Диагноз несомненен, если катетером подозрительную тень удается продвинуть вверх по мочеточнику.
Уретероскопия и нефроскопия являются наиболее информативными методами диагностики камней почек и мочеточников.
Лечение: 1. Консервативная терапия.
Коррекция нарушений обмена камнеобразующих веществ:
диетотерапия (ограничить употребление жиров и поваренной соли, исключить алкоголь);
купирование приступа почечной колики (тепловые процедуры, НПВС – диклофенак, спазмолитики – но-шпа. Наиболее эффективным патогенетическим лечением почечной колики в стационарных условиях является восстановление оттока мочи из почки путем катетеризации).
камнеизгоняющая (литокинетическая) терапия: активный режим, лечебная физкультура (ходьба, бег, прыжки), увеличение диуреза (мочегонные препараты, обильное питье или внутривенное введение жидкости), анальгезирующие, спазмолитические препараты, растительные уросептики, антибактериальная терапия, физиотерапия (ультразвуковая стимуляция, локальная вибротерапия и др. )
литолиз (растворение камней) может быть нисходящим и восходящим. Нисходящий литолиз эффективен при уратных камнях и основывается на назначении препаратов, способствующих их растворению (блемарен, уралит-У, магурлит). Восходящий литолиз проводится путем введения препаратов по мочеточниковому катетеру.
2. Хирургическое лечение:
полостная операция по удалению камня (хирургическое вскрытие брюшной полости и удаление камня);
лапароскопическая операция (удаление камня через мини-разрезы, через которые вводятся специальные инструменты — троакары);
дистанционная литотрипсия (дробление камней по средствам ударной волны, которая наводится на камень под рентгеновским или ультразвуковым контролем).
Трансуретральные методы (доступ к камню осуществляется через мочеиспускательный канал путем проведения тонкой металлической трубки с видеокамерой и освещением):
- контактная уретеролитотрипсия — камень разрушается в мочеточнике под контролем глаза хирурга при помощи лазера, пневматического инструмента, ультразвука;
- пиелолитотрипсия — удаление, дробление камней в лоханке почки.
Чрескожный метод: перкутанная нефролитолапаксия — создание хода диаметром 1 см в поясничной области между кожей и чашечно-лоханочной системой почки, через который затем удаляют камни больших размеров (больше 2, 5 см) или коралловидные камни; метод используется как самостоятельный, так и в комбинации с дистанционной литотрипсией в послеоперационном периоде (комбинированное лечение).
Почечная колика – острый болевой приступ, вызванный резким нарушением оттока, мочи из почки и гемодинамики в ней.
Риск возникновения почечной колики в течение жизни составляет 1—10%.
Этиология. Камни мочеточника; опухоль, сгустки крови, слизи, гноя внезапно окклюзирующие просвет мочевых путей и нарушающие пассаж мочи.
Окклюзия мочеточника, почечной лоханки, приводящая к почечной колике, наблюдается при нефролитиазе, гидронефротической трансформации, туберкулезе, гнойных процессах в почке, новообразованиях почки и мочеточника, дискинезии мочевых путей, нефроптозе.
Патогенез. Острая окклюзия верхних мочевых путей, резкое повышение давления в чашечно-лоханочной системе, отек паренхимы, растяжение фиброзной капсулы почки. Боль является следствием гиперактивации барорецепторов чашечно-лоханочной системы и рецепторов фиброзной капсулы, которая по Th1—L1 сегментам спинного мозга передается в виде афферентных импульсов в кору головного мозга, где трансформируется в боль.
Клиника. Приступ острых болей в пояснице и боковых отделах живота с выраженной иррадиацией на внутреннюю поверхность бедра, паховую область и половые органы. Почечная колика может возникнуть в любое время суток, приступ возникает внезапно, развивается очень быстро. Боль резкая, распирающая, имеет постоянный и схваткообразный характер. Иррадиация болей зависит от локализации конкремента в мочевых путях, вызвавшего их окклюзию. При камне, вызвавшем окклюзию лоханки, боли иррадиируют в поясницу и подреберье. Конкремент на границе верхней и средней трети мочеточника вызывает иррадиацию боли в нижние отделы живота, в область пупка. При конкременте в области безымянной линии боль иррадиирует в основном по передней поверхности бедра и в надлобковую область. Камень в юкставезикальном отделе мочеточника вызывает иррадиацию болей у мужчин в мошонку, у женщин – в область больших половых губ. При расположении камня в интрамуральном отделе мочеточника возникает дизурия в виде частого, иногда болезненного мочеиспускания, сопровождающегося иррадиацией боли в область уретры у женщин, в уретру и головку полового члена – у мужчин. По мере нарастания боли почечная колика часто сопровождается рвотой, не приносящей облегчения, парезом кишечника, которые возникают почти одновременно. Характер боли (особенно в первые 1, 5—2 ч) заставляет больного менять положение тела, любое из которых не приносит облегчения. Больной мечется, иногда наклоняет туловище, удерживая ладонь на пояснице со стороны боли. У детей младшего возраста боль в области пупка сопровождается рвотой. Ребенок плачет, испуган; острый приступ болей длится недолго (15—20 мин), сопровождается повышением температуры тела до 37, 2—37, 3 °С. Почечная колика с острой болью в пояснице может развиться у беременных женщин в третьем триместре. При почечной колике наблюдается брадикардия или нормокардия, при других заболеваниях, как правило, отмечается тахикардия. На высоте почечной колики отмечается умеренная артериальная гипертензия. Иногда боль вызывает обморочное состояние. Дизурия характерна, но непостоянна. Легко вызывается симптом Пастернацкого (легкое поколачивание по поясничной области). При наличии единственной почки может наступить анурия или олигоурия. Язык обложен белым налетом; живот участвует в акте дыхания. Нередко при почечной колике наблюдаются симптомы, характерные для острых заболеваний органов брюшной полости: могут появиться симптомы раздражения брюшины (симптом Щеткина—Блюмберга, Ровзинга). Более чем в половине случаев почечная колика сопровождается повышением температуры тела, что вызвано пиеловенозным рефлюксом в результате проникновения мочи в ток крови. Длительность приступа почечной колики колеблется от нескольких минут до нескольких часов.
Диагностика. Распознавание ПК основано на данных анамнеза (наличии мочекаменной болезни или других заболеваний, в патогенезе которых возможно развитие острой обструкции верхних мочевых путей), клиники заболевания, на физикальном осмотре, ультразвуковом исследовании почек и мочевых путей, радиоизотопных и рентгенологических методов исследования. Пальпаторно удается определить увеличение и болезненность почки. При почечной колике, которая обусловлена преимущественно окклюзией верхних мочевых путей, состав мочи на высоте почечной колики всегда бывает нормальным, поскольку практически исследуется моча здоровой контралатеральной почки. После купирования почечной колики в моче обнаруживаются следующие изменения: протеинурия (как правило, незначительная), эритроцитурия (свежие неизмененные эритроциты), лейкоцитурия, макрогематурия. Если гематурия появляется после почечной колики, то это указывает на наличие камня лоханки или мочеточника; если гематурия возникла в самом начале почечной колики, и затем приступ боли резко усилился, то это говорит об опухолевом процессе в почке, лоханке, мочеточнике, в таком случае колика обусловлена окклюзией верхних дыхательных путей сгустками крови. Отмечается умеренное повышение мочевины в крови. В анализе периферической крови возможно умеренное повышение количества лейкоцитов. УЗИ – идеальное первичное обследование. В серо-шкальном режиме выявляет камни в лоханочно-мочеточниковом сегменте и интрамуральном отделе мочеточника. Трансректальное и трансвагинальное УЗИ позволяет визуализировать конкременты в юкставезикальном отделе мочеточника. УЗИ легко выявляет пиелоэктазию. Экскреторная урография и хромоцистоскопия выявляют нарушение функции почки и эвакуации мочи. Своевременное выделение в течение 3—5-минутного введения внутривенно 0, 4%-ного раствора индигокармина в количестве 5 мл позволяет отказаться от предполагаемого диагноза почечной колики. Обзорный рентгеновский снимок выявляет тени рентгенопозитивных камней. Диагностические трудности возникают при выявлении невидимых мочекислых конкрементов, которые позволяет решить компьютерная томография. Экскреторная урография особенно показана в тех случаях, когда возникает необходимость оперативного вмешательства (конкремент больших размеров, сомнения в наличии контралатеральной почки, ее функциональной способности). При экскреторной урограмме отсутствует контраст в почке на стороне поражения, на нефрограмме хорошо выражена белая почка.
Дифференциальная диагностика. Почечную колику нужно дифференцировать от острого холецистита при локализации боли в правом подреберье. Для печеночной колики характерна иррадиация болей в область соска правой молочной железы, в правую лопатку, плечо, шею; они усиливаются при вдохе и при пальпации области желчного пузыря, легком поколачивании по правой реберной дуге, чего не наблюдается при почечной колике. При печеночной колике выявляется френикус-симптом, в правом подреберье определяется ригидность мышц передней брюшной стенки и иногда признаки раздражения брюшины, в то время как при почечной колике эти симптомы отсутствуют. Хромоцистоскопия позволяет дифференцировать заболевания. Дифференцировать почечную колику и острый аппендицит может быть трудно, особенно при ретроцекальном расположении отростка. При остром аппендиците обычно боли возникают в подложечной области (симптом Кохера), а затем локализуются в правой подвздошной области, где пальпаторно определяется ригидность мышц передней брюшной стенки, небольшое вздутие живота, могут появляться симптомы раздражения брюшины. При почечной колике более выражен болевой синдром, более характерна иррадиация болей, в отличие от беспокойного поведения больного при почечной колике больные с острыми процессами в брюшной полости стремятся сохранить неподвижность, принимают вынужденное, щадящее положение в постели. При остром аппендиците рвота появляется спустя длительное время после возникновения болей, при почечной колике эти симптомы появляются практически одновременно. Если при почечной колике нельзя полностью исключить острый аппендицит, то выполняют лапароскопию или даже лапаротомию. При кишечной колике имеет место постоянный характер болей на протяжении приступа, отсутствие длительных интервалов между отдельными схватками, резко выраженный метеоризм. При почечной колике интенсивность болей значительно большая. Могут возникать трудности при дифференциальной диагностике кишечной непроходимости и почечной колике. Такие признаки, как отсутствие стула, неотхождение газов, резкие боли по всему животу, могут наблюдаться при почечной колике, хотя они характерны для кишечной непроходимости. Не всегда могут наблюдаться симптомы, характерные для кишечной непроходимости, даже если имеется признак Валя и местное вздутие живота. Рвота характерна как для кишечной непроходимости, так и для почечной колики. При трудностях в распознавании почечной колики и кишечной непроходимости приходится прибегать к дополнительным методам исследования. Боли при кишечной непроходимости мучительные, непрекращающиеся, захватывают всю область живота, перистальтика сохранена, усилена в начале заболевания. Больные находятся в состоянии тяжелой интоксикации, лицо осунувшееся, щеки впалые. При паралитической и механической непроходимости выявляется сильное вздутие живота. Высокая механическая непроходимость проявляется рвотой кишечным содержимым. Такие заболевания, как перфоративная язва желудка и двенадцатиперстной кишки, имеют достаточно характерные признаки, позволяющие сравнительно легко дифференцировать их с почечной коликой. Кинжальная боль в животе, развитие признаков перитонита характерны для заболеваний органов брюшной полости. Боль при межреберной невралгии не имеет схваткообразного характера, зависит от положения тела (уменьшается в покое и неглубоком дыхании) в отличие от таковой при почечной колике. Крайне редко почечная колика возникает с противоположной стороны по отношению к окклюзированному мочеточнику. Этот феномен описан Л. Д. Кларком и Норманом.
Осложнения. Осложнения почечной колики: острый гнойный пиелонефрит, бактериемический шок.
+Лечение почечной колики предполагает устранение боли и ликвидацию обструкции. Купировать боль позволяет диклофенак натрия, который является антагонистом синтеза простагландинов, что способствует снижению фильтрации и таким образом, внутрилоханочного давления; а также уменьшает воспаление и отек в зоне окклюзии, ингибирует стимуляцию гладкой мускулатуры мочеточника, что блокирует его перистальтику. Аналгетический эффект одинаков с таковым у морфина при его внутривенном введении. Парентеральная дозировка 75 мг, ректальные свечи содержат 100 мг. При почечной колике показаны также тепловые процедуры (горячие ванны или грелки на поясницу и живот), обезболивающие препараты, новокаиновая блокада семенного канатика у мужчин и блокада круглой связки матки у женщин или внутритазовая блокада по Школьникову. При безуспешности перечисленных мероприятий – катетеризация мочеточника для восстановления пассажа мочи.
В ряде случаев (конкремент больших размеров, осложнения в виде острого гнойного пиелонефрита) выполняются уретеролитотомия, пиело– или нефростомия в сочетании с декапсуляцией почки. После устранения почечной колики необходимо детальное урологическое обследование.
№19. Более 90% от всех видов ожогов приходится на долю термических повреждений. Чаще всего это травмы, полученные в быту или на производстве в результате несоблюдения техники безопасности и обычной человеческой невнимательности.
Степени тяжести ожогов
В зависимости от глубины поражений выделяют 4 степени ожогов, каждая из которых характеризуется определенными симптомами.
Ожоги I степени — легкие, поверхностные поражения, сопровождающиеся гиперемией, незначительными отеками и болями.
Ожоги II степени повреждают кожу вплоть до росткового слоя. Симптоматика дополняется возникновением волдырей преимущественно небольших размеров с серозной жидкостью внутри.
Ожоги III степени разделяются на 2 категории: А и Б. Характеризуются частичным повреждением дермы или полным ее разрушением соответственно. При травмах III-А степени в месте поражения образуется струп, возникают крупные пузыри (буллы). III-Б повреждения сопровождаются отмиранием тканей – некрозами.
Ожоги IV степени считаются смертельно опасными. Происходит обугливание всех слоев кожи вместе с подкожно-жировой клетчаткой, мышцами, сухожилиями и костями.
Среди термических травм встречаются повреждения всех степеней тяжести.
Виды поражающих факторов
Термические ожоги – это повреждения, возникающие под влиянием высоких температур. Любое воздействие тепла температурой выше 45°С, продолжающееся более 1 минуты, приводит к гипертермии и последующему разрушению тканей. Особенность термических ожогов заключается в том, что после прекращения контакта с источником поражения перегревание клеток в тканях продолжается, а иногда даже усиливается.
К термическим ожогам приводит контакт с открытым огнем, горячей жидкостью или паром, расплавленным металлом или пластмассой, раскаленными предметами.
Пламя
Является причиной 60% всех термических ожогов. Травмы возникают в результате неосторожного обращения с огнем, воспламенения горючих жидкостей, например, бензина. Нередко к ожоговым повреждениям приводит некачественная пиротехника либо нарушение правил ее использования. Самые тяжелые ожоги с большой площадью поражения возникают при пожарах.
Термические ожоги от контакта с пламенем, как правило, имеют относительно обширную площадь повреждений, но небольшую глубину. Разрушение кожных покровов чаще всего происходит до росткового слоя, поэтому подобные травмы преимущественно относят к ожогам II степени. Нередко дополнительные ранения можно получить при удалении с обожженных участков фрагментов одежды. Случайно оставленные в ране нити и волокна ткани способны привести к развитию инфекции.
Травмы III и IVстепени, порой несовместимые с жизнью, можно получить, находясь в горящем здании или автомобиле, когда нет возможности своевременно покинуть зону действия открытого огня. Ситуация может усугубиться потерей сознания человека, что неизбежно приведет к обгоранию значительной площади тела, большой глубине поражений и, как следствие, к инвалидности или смерти пострадавшего.
Зачастую под воздействием пламени происходит повреждение глаз и верхних дыхательных путей.
Жидкость
В отличие от ожогов пламенем, повреждения кипятком или горячим маслом характеризуются небольшой площадью, но значительной глубиной. Чаще подобные травмы относят ко II или III степени тяжести.
Глубина ожогов зависит от времени, в течение которого человек контактировал с горячей жидкостью. При этом температура воды или масла необязательно должна равняться 90 – 100 °С. Так, в результате воздействия на кожу жидкости 50 °С на протяжении 10 минут может возникнуть довольно глубокий ожог.
Статистические данные указывают на то, что жидкостью чаще всего обжигаются дети и пожилые люди. Среди малышей до 5 лет ожоги горячей водой составляют 80% от всех видов термических ранений.
Подобные травмы в большинстве случаев возникают в бытовых условиях. Случайно опрокинутая кастрюля с супом, неаккуратно налитый чай, внезапно брызнувшее со сковороды масло – все это наиболее распространенные причины термических повреждений различной степени тяжести. Реже ожоги становятся следствием аварийных ситуаций на теплотрассах или при прорыве батарей отопления.
Пар
Ожоги паром обычно охватывают значительную площадь кожи, но не затрагивают ее глубокие слои, что свойственно I и II степени поражения.
Обычно травмы от воздействия пара причисляются к бытовым и являются следствием нарушений правил безопасности при приготовлении пищи. Достаточно наклониться к кипящей воде или пронести над ней руку, чтобы получить ожог кожи, слизистых оболочек или глаз.
Горячий пар – частая причина термических повреждений верхних дыхательных путей. Особенно часто поражается гортань во время ингаляций при ОРВИ.
При контакте с паром происходит его оседание на кожу. В результате образуются капельки воды, температура которых повышается по сравнению с изначальной температурой пара. Это приводит к более серьезным повреждениям, чем при воздействии на ткани горячей жидкости, которая при попадании на тело человека охлаждается.
Раскаленные предметы
Тяжесть ожогов зависит от длительности контакта с источником поражения и варьируется от II до IV степени. Площадь поврежденной поверхности будет соответствовать размерам предмета и иметь достаточно четкие очертания.
Причиной подобных ожогов в быту может оказаться прикосновение к раскаленной сковороде, кастрюле, чайнику или горячим электроприборам. В этом случае травма не будет глубокой, так как человеку на рефлекторном уровне свойственно убирать руку от источника высоких температур. Осложнения возникают тогда, когда во время удаления нанесшего травму предмета происходит отслоение пораженных участков кожи.
Расплавленный металл
Попадание на кожу доведенного до жидкого состояния металла всегда приводит к ожогам III либо IV степени.
Минимальная температура расплавленного металла равняется 800 °С, а максимальная 1500 °С. Поэтому избежать сильнейших ожоговых травм при контакте с ним невозможно.
Ожоги возникают преимущественно на производстве среди литейщиков и рабочих доменных цехов. Повреждения обычно локализуются на нижних конечностях, реже на лице или руках. Состояние пострадавшего значительно ухудшается при затекании металла в обувь или при полном погружении конечности в емкость с источником поражения. Для спасения жизни таких пациентов обычно требуется ампутация.
ожог I степени, когда нет пузырей, соответственно, глубокие ткани не повреждены;
размер повреждения не больше ладони;
отсутствует поражения ступней, кистей, лица;
нет нагноения и воспаления на обожженном участке.
Возможные осложнения термического ожога:
сепсис (когда повреждено больше 20 % поверхности тела);
пневмония;
вторичное инфицирование в виде гангрены, абсцесса.
Патогенез термического ожога
Термический ожог вызывает местные изменения на коже, которые проходят несколько стадий развития.
Наиболее комфортной температурой тела для обеспечения нормальной биологической активности ферментов является +36…+37 ℃. Диапазон +37…+41 ℃ также приемлем, а при +42 ℃ начинается разрушение белка.
При воздействии высоких температур на тело возникают ожоги различных степеней тяжести. Причем важна не только температура поражающего агента, но и время воздействия. Глубина поражения ткани напрямую зависит от времени воздействия поражающего фактора в связи с физическими свойствами кожи. Кратковременное воздействие даже очень горячих предметов и жидкостей может не привести к образованию ожога.
При глубоких ожогах различают три зоны поражения: зона коагуляции, зона паранекроза и периферическая.
Повреждение эпидермального барьера приводит к бактериальному инфицированию, потере жидкости, нарушению терморегуляции. Ожог тканей сопровождается отеком и гипотермией, поскольку терморегуляция по мере повреждения дермы снижается и полностью отсутствует в открытых ранах.
Тяжесть состояния пострадавшего зависит от площади пораженной поверхности и глубины ожога. В первые дни на тяжесть состояния влияет в основном обширность поражения, а в последующие — его глубина.
Причины возникновения термического ожога
Основные причины возникновения термических ожогов — несчастные случаи на производстве и невнимательность в быту. Обжечься можно:
пламенем (чаще всего это II степень ожога, при котором поражаются органы дыхания и зрения);
жидкостью (зачастую это II–III степень повреждения с захватом глубоких тканей);
паром (неглубокий, но обширный ожог);
раскаленным предметом (II–IV степень поражения) с четким контуром и глубоким повреждением и вероятным отслаиванием тканей.
Стадии и симптомы термических повреждений
Оказание первой помощи при термических ожогах проводится с учетом стадии (глубины) поражения тканей. В медицине выделяют четыре стадии:
I — частичное повреждения поверхностного слоя кожи. Сопровождается небольшой отечностью, жжением, покраснением;
II — полное поражение поверхности кожи. Характеризуется волдырями, жгучей болью;
III — поражение достигает глубоких слоев кожи. Различают степени IIIa и IIIb. Первая сопровождается фрагментарным повреждением глубоких слоев, формированием сухих темных корок (струпьев). Вторая характеризуется гибелью слоев эпидермиса, повреждением жировой клетчатки;
IV — самые опасные ожоги, при которых травмируются все слои кожи, мышечные, костные ткани и сухожилия.
В каждом случае, кроме самых легких повреждений кожи, нужно незамедлительно вызывать бригаду скорой помощи. Не следует пытаться самостоятельно нанести лекарственные средства, обработать мест поражения спиртом и проводить другие манипуляции. Главное — облегчить состояние пострадавшего до приезда врачей. Специалисты оценят степень повреждения, окажут профессиональную помощь, при необходимости госпитализируют.
Первая помощь пострадавшему при термических ожогах
Грамотные действия по оказанию первой помощи при термических ожогах снизят риск опасных осложнений и поспособствуют быстрому восстановлению тканей и самого пострадавшего. Экстренная помощь подразумевает следующий алгоритм действиях:
Остановить контакт пораженного участка тела с травмирующим фактором (погасить пламя на одежде).
Поместить место поражения под напор воды из-под крана на 10–15 минут. Важно остановить проникновение температурного воздействия вглубь. Этого удается достичь охлаждением. Лед с этой целью использовать нельзя. Резкий перепад температуры приведет к омертвению клеток.
Если речь об ожоге кипящей жидкостью, необходимо освободить поврежденный участок от одежды, не касаясь раны. Если ткань прилипла к телу, нельзя принудительно отдирать ее, разрешается лишь обрезать лишние куски материи вокруг.
Наложить на рану стерильную повязку, используя специальные аптечные средства.
Дать пострадавшему обезболивающий препарат.
Чтобы снизить интоксикацию из-за попадания в кровь продуктов распада отмерших тканей, пострадавшему дают пить теплую минеральную воду без газа или обычную воду, добавив в нее по 0, 5 ч. л. соли и соды на 1 л.
Перед тем как оказывать пострадавшему первую помощь в домашних условиях, необходимо позвонить в службу скорой помощи.
Лечение при термическом повреждении
Комплексное лечение при ожогах пламенем предусматривает применение местных заживляющих средств, противовоспалительный лекарств, меры по профилактике инфицирования пораженных тканей. Процесс восстановления проходит поэтапно:
Воспалительный процесс. Омертвевшие ткани расплавляются, а рана постепенно очищается от продуктов распада и посторонних частиц.
Восстановительный период. Формируется соединительная и грануляционная ткань.
Эпителизация. Поврежденный участок покрывается кожей, формируется рубец, а ткани заживают.
Чтобы процесс заживления шел по плану и без осложнений, важно еще до приезда врачей предпринять все необходимые меры, чтобы остановить патологическое воздействие. Для этого нужно учитывать ряд запретов, касающихся правил ухода за пострадавшим.
Чего делать ни в коем случае нельзя:
сдирать прилипшую одежду с поврежденной кожи;
прикладывать лед к ожогу (провоцирует обморожение);
трогать рану руками, особенно грязными.
вскрывать пузыри, поскольку в открытые раны быстро проникнет инфекция;
закрывать рану лейкопластырем, если он не предназначен для лечения ожогов;
обрабатывать обожженную кожу кефиром, спиртом, отваром трав и пр.;
прикладывать к ране алоэ;
использовать для очистки раны ватные тампоны (волокна застрянут и вызовут воспаление).
Помимо перечисленного, не следует применять без врачебной консультации любые мази, масла и крема. При неправильном и несвоевременном использовании они только усложнят дальнейший уход за раной и замедлят процесс восстановления. Лечение ожогов должно назначаться и контролироваться врачом.
Препараты
Оказание первой помощи при термических ожогах в большой степени оказывает влияние на дальнейший ход лечения и перспективу восстановления.
В первые сутки внутривенно вводятся анальгезирующие и антигистаминные препараты. В качестве противошокового средства применяют новокаиновые блокады в зависимости от локализации ожога. Если у пострадавшего поражено более 15% тела, независимо от степени ожога, применяют ингаляцию увлажненным кислородом.
В целях выравнивания гемодинамики применяют инфузионную терапию кровезаменителями, а в случаях ослабления сердечной деятельности используют кофеиносодержащие препараты.
Первая помощь в домашних условиях должна быть оказана правильно, каким бы незначительным ни был ожог.
В первую очередь необходимо удалить поражающий фактор и по возможности охладить место ожога. Следует обеспечить пострадавшему обильное питье, при сильном болевом синдроме можно дать безрецептурный анальгетик. В случае тяжелых поражений этим следует ограничиться и дождаться приезда медиков.
В более легких случаях можно очистить место ожога хлоргексидином и наложить специальную атравматичную повязку.
Физиотерапия
Физиотерапевтические методы лечения термических ожогов назначаются в зависимости от стадии лечения.
УФО-терапия направлена на регенерацию тканей. С помощью средств ультразвуковой терапии ускоряется отторжение омертвевших тканей, производится микромассаж подлежащих тканей, что способствует улучшению кровоснабжения. Также они оказывают антибактериальный эффект и усиливают действие лекарственных средств.
Озонотерапия оказывает бактерицидное, иммуномодулирующее, детоксикационное действие, стимулирует образование грануляций и эпителия.
К средствам лечения также относятся магнитотерапия, низкоинтенсивная лазерная терапия, светотерапия, механо-вакуумная терапия, лечение с помощью воздушно-плазменного потока. Помните, что любое лечение и лекарства вам может назначить только врач.
Операция
Хирургическое лечение назначают при термических ожогах тяжелых степеней. Оно предполагает несколько видов оперативного вмешательства:
некротомия — рассечение циркулярного ожогового струпа;
некрэктомия — иссечение нежизнеспособных тканей;
при необходимости ампутация конечностей;
пластическое закрытие ожоговой раны
реконструктивно-пластические мероприятия.
Прогноз термических ожогов
При термических ожогах прогнозирование дальнейшего течения болезни зависит в основном от площади и глубины поражения, а также от наличия сопутствующих заболеваний. Обширные и глубокие ожоги могут представлять серьёзную опасность для здоровья и жизни человека.
При прогнозировании состояния пострадавшего пользуются двумя основными методами: правилом «сотни» и индексом Франка. Правило «сотни» применимо только для взрослых пациентов. Оно состоит в суммировании возраста больного и относительной площади пораженной поверхности к общей площади тела. При значениях:
менее 60 — прогноз благоприятный;
от 61 до 80 — умеренно благоприятный;
от 81 до 100 — сомнительный;
100 — прогноз неблагоприятный.
Возраст пострадавшего играет значительную роль в определении иммунных и репаративных возможностей организма.
Осложнения
Термические ожоги нередко сопровождаются осложнениями, которые принято классифицировать на первичные, вторичные и поздние.
Первичные осложнения, полученные во время травмы, характерны только для ожогов 4 степени. К ним относятся обугливание и мумифицирование мягких тканей, тромбоз крупных артерий и вен.
Вторичные осложнения чаще возникают вследствие инфицирования и могут поражать кожу, мягкие ткани, сосуды и нервы, внутренние органы. К ним относятся гангрена, абсцессы, гепатит, остеомиелит и т. д.
Поздние осложнения развиваются в процессе или после заживления ожоговых ран. Это пиелонефрит, гепатит, нарушение функций суставов и конечностей, в некоторых случаях ожоговый дерматит и экзема.
К местным осложнениям термических ожогов относится образование струпов, контрактур и рубцов. Струпом называют жесткую некротизированную ткань, опоясывающую конечности, шею или туловище, так называемый циркулярный струп. Струп оказывает давление на ткани, провоцируя ишемию — локальное нарушение кровотока, может вызвать проблемы с дыханием. Рубцы и контрактуры образуются при ожогах высоких степеней и могут привести к ограничению подвижности суставов. Не занимайтесь самолечением, обязательно проконсультируйтесь с врачом.
способов оценки площади ожога – «правило ладони». Площадь ладони человека составляет в среднем 1% площади его тела. Так, с помощью ладони можно определить, сколько процентов тела поражено.
Существует также правило «девятки» для взрослых: рука, половина ноги, половина спины, грудь, живот, голова – по 9%, и промежность – 1%. Но у детей голова с шеей составляет около 21% площади тела.



|
|
|
© helpiks.su При использовании или копировании материалов прямая ссылка на сайт обязательна.
|