
- Автоматизация
- Антропология
- Археология
- Архитектура
- Биология
- Ботаника
- Бухгалтерия
- Военная наука
- Генетика
- География
- Геология
- Демография
- Деревообработка
- Журналистика
- Зоология
- Изобретательство
- Информатика
- Искусство
- История
- Кинематография
- Компьютеризация
- Косметика
- Кулинария
- Культура
- Лексикология
- Лингвистика
- Литература
- Логика
- Маркетинг
- Математика
- Материаловедение
- Медицина
- Менеджмент
- Металлургия
- Метрология
- Механика
- Музыка
- Науковедение
- Образование
- Охрана Труда
- Педагогика
- Полиграфия
- Политология
- Право
- Предпринимательство
- Приборостроение
- Программирование
- Производство
- Промышленность
- Психология
- Радиосвязь
- Религия
- Риторика
- Социология
- Спорт
- Стандартизация
- Статистика
- Строительство
- Технологии
- Торговля
- Транспорт
- Фармакология
- Физика
- Физиология
- Философия
- Финансы
- Химия
- Хозяйство
- Черчение
- Экология
- Экономика
- Электроника
- Электротехника
- Энергетика
Реакции окисления альдегидов.
1. Реакция «серебряного зеркала »: это качественная реакция на альдегиды, используется реактив Толленса (аммиачный раствор оксида серебра). Так как в растворе присутствует аммиак, окисление идет не до карбоновой кислоты, а до ее соли:

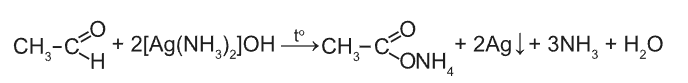
Особое внимание!!! Окисление метаналя аммиачным раствором оксида серебра приводит к образованию карбоната аммония, а не муравьиной кислоты:
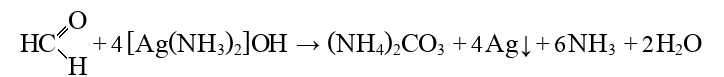
2. Окисление гидроксидом меди (II): происходит при нагревании альдегидов со свежеосажденным гидроксидом меди, при этом образуется красно-кирпичный осадок оксида меди (I) Это — одна из  качественных реакций на альдегиды.
качественных реакций на альдегиды.
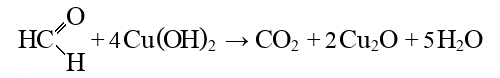
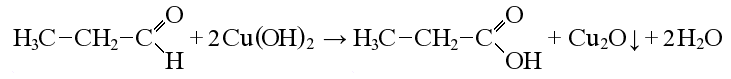
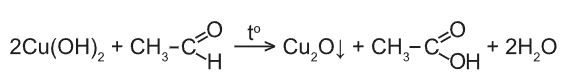
3. Окисление дихроматом калия:
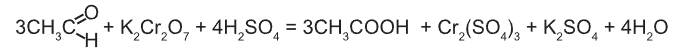
3CH2O +2 K2Cr2O7 + 8H2SO4→ 3 CO2 + 2Сг2(SО4) 3 + K2SO4 + 11H2O
4. Окисление перманганатом калия:
а) в кислой среде до карбоновых кислот:
5СН3 - СНО + 2 KMnO4 + 3H2SO4 = 5CH3COOH + 2MnSO4 + K2SO4 +3H2O
Муравьиный альдегид (формальдегид) окисляется до углекислого газа, потому что соответствующая ему муравьиная кислота неустойчива к действию сильных окислителей:
5HCHO + 4KMnO₄ + 6H₂ SO₄ → 5CO₂ + 4MnSO₄ + 2K₂ SO₄ + 11H₂ O
б) нейтральная среда:
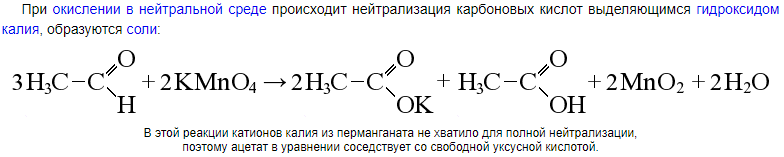
Как известно, продукты восстановления перманганата калия в нейтральной среде, это окисид (IV) и щелочь (KOH). Формальдегид окисляется до диоксида углерода, но в одном растворе кислотный оксид и щелочь вступят в реакцию.
3HCHO + 4KMnO₄ + H₂ O → 2 KHCO₃ + K₂ CO₃ + 4MnO₂ + 3H₂ O
в) щелочная среда:

HCHO + 4KMnO₄ + 6кон → K2CO3 + 4K2MnO4 + 4H2O
Окисление бромной водой:
CH3CHO + Br2 + H2O → CH3COOH + 2HBr
HCHO + 2Br2 + H2O → CO2 + 4HBr
Окисление бромной водой в присутствии щелочи:

HCHO + 2Br2 + 6NaOH → Na2CO3 + 4NaBr + 4H2O
|
|
|
© helpiks.su При использовании или копировании материалов прямая ссылка на сайт обязательна.
|