
- Автоматизация
- Антропология
- Археология
- Архитектура
- Биология
- Ботаника
- Бухгалтерия
- Военная наука
- Генетика
- География
- Геология
- Демография
- Деревообработка
- Журналистика
- Зоология
- Изобретательство
- Информатика
- Искусство
- История
- Кинематография
- Компьютеризация
- Косметика
- Кулинария
- Культура
- Лексикология
- Лингвистика
- Литература
- Логика
- Маркетинг
- Математика
- Материаловедение
- Медицина
- Менеджмент
- Металлургия
- Метрология
- Механика
- Музыка
- Науковедение
- Образование
- Охрана Труда
- Педагогика
- Полиграфия
- Политология
- Право
- Предпринимательство
- Приборостроение
- Программирование
- Производство
- Промышленность
- Психология
- Радиосвязь
- Религия
- Риторика
- Социология
- Спорт
- Стандартизация
- Статистика
- Строительство
- Технологии
- Торговля
- Транспорт
- Фармакология
- Физика
- Физиология
- Философия
- Финансы
- Химия
- Хозяйство
- Черчение
- Экология
- Экономика
- Электроника
- Электротехника
- Энергетика
По природе лиганда
1) Аммиакаты — соединения, в которых лигандами служат молекулы аммиака, например: [Cu(NH3)4]SO4, [Co(NH3)6]Cl3, [Pt(NH3)6]Cl4 и др.
2) Аквакомплексы — в которых лигандом выступает вода: [Co(H2O)6]Cl2, [Al(H2O)6]Cl3 и др.
3) Карбонилы — комплексные соединения, в которых лигандами являются молекулы оксида углерода(II): [Fe(CO)5], [Ni(CO)4].
4) Ацидокомплексы — комплексы, в которых лигандами являются кислотные остатки. К ним относятся комплексные соли: K2[PtCl4], комплексные кислоты: H2[CoCl4], H2[SiF6].
5) Гидроксокомплексы — комплексные соединения, в которых в качестве лигандов выступают гидроксид-ионы: Na2[Zn(OH)4], Na2[Sn(OH)6] и др.
1) В названии комплексного соединения первым указывают отрицательно заряженную часть — анион, затем положительную часть — катион.
2) Название комплексной части начинают с указания состава внутренней сферы. Во внутренней сфере прежде всего называют лиганды — анионы, прибавляя к их латинскому названию окончание «о». Например: Cl− — хлоро, CN− — циано, SCN− — тиоцианато, NO3− — нитрато, SO32− — сульфито, OH− — гидроксо и т. д. При этом пользуются терминами: для координированного аммиака — аммин, для воды — аква, для оксида углерода(II) — карбонил.
3) Число лигандов указывают греческими числительными: 1 — моно (часто не приводится), 2 — ди, 3 — три, 4 — тетра, 5 — пента, 6 — гекса.
4) Затем называют комплексообразователь, используя корень его латинского названия и окончание -ат, после чего римскими цифрами указывают (в скобках) степень окисления комплексообразователя.
5) После обозначения состава внутренней сферы называют внешнюю сферу.
6) В названии нейтральных комплексных частиц комплексообразователь указывается в именительном падеже, а степень его не указывается, так как она однозначно определяется, исходя из электронейтральности комплекса.
Примеры:
K3[Fe(CN)6] — гексацианоферрат(III) калия
(NH4)2[PtCl4(OH)2] — дигидроксотетрахлороплатинат(IV) аммония
[Сr(H2O)3F3] — трифторотриаквахром
[Сo(NH3)3Cl(NO2)2] — динитритохлоротриамминкобальт
[Pt(NH3)4Cl2]Cl2 — хлорид дихлоротетраамминплатины(IV)
[Li(H2O)4]NO3 — нитрат тетрааквалития
В соединениях с комплексным катионом используются русские название элементов:
 [Cu(NH3)4]SO4 [Cu(NH3)4]2+ + SO42-
[Cu(NH3)4]SO4 [Cu(NH3)4]2+ + SO42-
сульфат тетраамминмеди (II)
[Cu(NH3)4]2+ катион тетрамминмеди (внутренняя сфера комплекса)
SO42- сульфат-анион (внешняя сфера комплекса)
Cu2+ комплексообразователь
NH3 лиганды
4 – координационное число (часто, но не всегда, координационное число в два раза больше заряда комплексообразователя)

 Cu2+ + 4NH3 [Cu(NH3)4]2+
Cu2+ + 4NH3 [Cu(NH3)4]2+
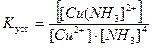
 |
В соединениях с комплексным анионом используются латинские названия элементов:
Al – алюминат,
Ag – аргентат,
Au – аурат,
Co – кобальтат,
Cr – хромат,
Cu – купрат,
Fe – феррат,
Hg – меркурат,
Mo – молибдат,
Ni – никелат,
Sb – антимонат,
Zn - цинкат.
 K4[Fe(CN)6] 4K+ + [Fe(CN)6]4-
K4[Fe(CN)6] 4K+ + [Fe(CN)6]4-
гексацианоферрат (II) калия
[Fe(CN)6]4- гексацианоферрат (II) анион (внутренняя сфера комплекса)
K+ катионы калия (внешняя сфера комплекса)
Fe2+ комплексообразователь
CN- лиганды
6 – координационное число

 Fe2+ + 6CN- [Fe(CN)6]4-
Fe2+ + 6CN- [Fe(CN)6]4-
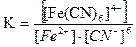
|
|
|
© helpiks.su При использовании или копировании материалов прямая ссылка на сайт обязательна.
|