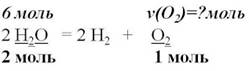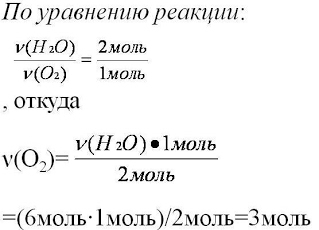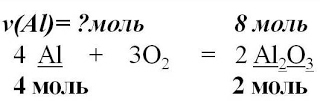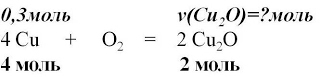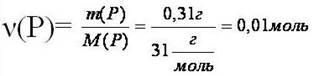Химия 8 класс. Тема. Решение задач.. Домашнее задание.. Решите задачи, используя алгоритмы.. 1. Вычислите количество вещества оксида алюминия, образовавшегося в результате взаимодействия алюминия количеством вещества 0,27 моль с достаточным количеством ки
Химия 8 класс
Тема. Решение задач.
Домашнее задание.
Решите задачи, используя алгоритмы.
1. Вычислите количество вещества оксида алюминия, образовавшегося в результате взаимодействия алюминия количеством вещества 0, 27 моль с достаточным количеством кислорода (4Al +3O2=2Al2O3).
2. Вычислите массу серы, необходимую для получения оксида серы (IV) количеством вещества 4 моль (S+O2=SO2).
3. Вычислите количество вещества сульфида натрия, если в реакцию с натрием вступает сера массой 12, 8 г (2Na+S=Na2S).
АЛГОРИТМ РЕШЕНИЯ РАСЧЕТНЫХ ЗАДАЧ
Алгоритм №1
Вычисление количества вещества по известному количеству вещества, участвующего в реакции.
Пример. Вычислите количество вещества кислорода, выделившегося в результате разложения воды количеством вещества 6 моль.
| Последовательность выполнения действий
| Оформление задачи
| | 1. Записать условие задачи
|  Дано: Решение
ν (Н2О) = 6моль _______________
ν (О2) =? Дано: Решение
ν (Н2О) = 6моль _______________
ν (О2) =?
| | 2. Вычислить молярные массы веществ,
о которых, идёт речь в задаче
| Решение:
М(О2) =32г/моль
| | 3. Запишем уравнение реакции и расставим коэффициенты
| 2Н2О=2Н2+О2
| | 4. Над формулами веществ запишем
количества веществ из условия задачи,
а под формулами –стехиометрические коэффициенты, отображаемые уравнением реакции
| 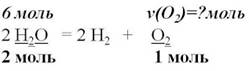
| | 5. Для вычисления искомого количества вещества,
составим соотношение
| 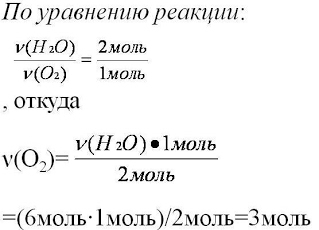
| | 6. Записываем ответ
| Ответ: ν (О2)=3моль
|
Алгоритм №2
Вычисление массы вещества по известному количеству другого вещества, участвующего в реакции.
Пример: Вычислите массу алюминия, необходимого для получения оксида алюминия количеством вещества 8 моль.
| Последовательность выполнения действий
| Оформление решения задачи
| | 1. Записать условие задачи
| Дано:
ν (Al2O3)=8моль
________
Найти:
m(Al)=?
| | 2. Вычислить молярные массы веществ,
о которых, идёт речь в задаче
|
M(Al2O3)=102г/моль
| | 3. Запишем уравнение реакции
и расставим коэффициенты
| 4 Al + 3O2 = 2Al2O3
| | 4. Над формулами веществ запишем
количества веществ из условия задачи,
а под формулами –
стехиометрические коэффициенты,
отображаемые уравнением реакции
|
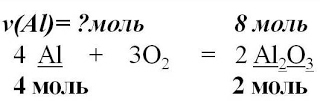
| | 5. Вычислим количества вещества, массу которого
требуется найти. Для этого составим соотношение.
| 
| | 6. Вычисляем массу вещества, которую требуется найти
| m=ν ∙ M,
m(Al)=ν (Al)∙ M(Al)=16моль∙ 27г/моль=432г
| | 7. Записываем ответ
| Ответ: m (Al)=432 г
|
Алгоритм №3
Вычисление количества вещества по известной массе другого вещества, участвующего в реакции.
Пример. Вычислите количество вещества оксида меди (I), если в реакцию с кислородом вступает медь массой 19, 2г.
| Последовательность выполнения действий
| Оформление задачи
| | 1. Записать условие задачи
| Дано:
m(Cu)=19, 2
Найти:
ν (Cu2O)=?
| | 2. Вычислить молярные массы веществ,
о которых, идёт речь в задаче
| М(Cu)=64г/моль
| | 3. Найдём количество вещества, масса которого
дана в условии задачи
|

| | 4. Запишем уравнение реакции
и расставим коэффициенты
|
4 Cu + O2 = 2 Cu2O
| | 5. Над формулами веществ запишем
количества веществ из условия задачи,
а под формулами –
стехиометрические коэффициенты,
отображаемые уравнением реакции
|
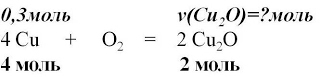
| | 6. Для вычисления искомого количества вещества,
составим соотношение
| 
| | 7. Запишем ответ
| Ответ: ν (Cu2O)=0, 15 моль
|
Алгоритм №4
Вычисление массы вещества по известной массе другого вещества, участвующего в реакции
Пример. Вычислите массу кислорода, необходимую для сгорания фосфора, массой 0, 31г.
| Последовательность выполнения действий
| Оформление задачи
| | 1. Записать условие задачи
| Дано:
m(P)=0, 31г
Найти:
m(O2)=?
| | 2. Вычислить молярные массы веществ, о которых, идёт речь в задаче
| М(P)=31г/моль
M(O2)=32г/моль
| | 3. Найдём количество вещества, масса которого дана в условии задачи
| 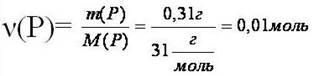
| | 4. Запишем уравнение реакции
и расставим коэффициенты
|
4P + 5O2 = 2P2O5
| | 5. Над формулами веществ запишем
количества веществ из условия задачи,
а под формулами –
стехиометрические коэффициенты,
отображаемые уравнением реакции
| 
| | 6. Вычислим количества вещества, массу которого необходимо найти
| 
| | 7. Найдем массу вещeства, которую требуется вычислить
| m(O2)=ν (O2)∙ M(O2)=
0, 0125моль∙ 32г/моль=0, 4г
| | 8. Запишем ответ
| Ответ: m(O2)=0, 4г
| | | Порядок решения задач:
- Краткая запись условия задачи.
- Запись уравнения химической реакции.
- Запись известных и неизвестных величин над формулами веществ.
- Запись под формулами веществ количества, молярные массы и массы(или молярные объемы и объемы) веществ.
- Составление и решение пропорции.
Запись ответа задачи.
Задача: Сколько граммов оксида меди (II) образовалось при прокаливании 6, 4 г меди.
Дано: Решение:
m(Cu) = 6, 4 кг 6, 4 г Х г
Найти: m(CuO) 2Cu + O2 = 2CuO
ν = 2 моль ν = 2 моль
М = 64г/моль М = 80 г/моль
m = 128г m = 160 г
Составляем пропорцию: 6, 4 г; 128 г = Х г: 160 кг
Х = 6, 4 * 160 / 128 Х = 8 г
Ответ: 8 г. Cu
|

 Дано: Решение
ν (Н2О) = 6моль _______________
ν (О2) =?
Дано: Решение
ν (Н2О) = 6моль _______________
ν (О2) =?