
- Автоматизация
- Антропология
- Археология
- Архитектура
- Биология
- Ботаника
- Бухгалтерия
- Военная наука
- Генетика
- География
- Геология
- Демография
- Деревообработка
- Журналистика
- Зоология
- Изобретательство
- Информатика
- Искусство
- История
- Кинематография
- Компьютеризация
- Косметика
- Кулинария
- Культура
- Лексикология
- Лингвистика
- Литература
- Логика
- Маркетинг
- Математика
- Материаловедение
- Медицина
- Менеджмент
- Металлургия
- Метрология
- Механика
- Музыка
- Науковедение
- Образование
- Охрана Труда
- Педагогика
- Полиграфия
- Политология
- Право
- Предпринимательство
- Приборостроение
- Программирование
- Производство
- Промышленность
- Психология
- Радиосвязь
- Религия
- Риторика
- Социология
- Спорт
- Стандартизация
- Статистика
- Строительство
- Технологии
- Торговля
- Транспорт
- Фармакология
- Физика
- Физиология
- Философия
- Финансы
- Химия
- Хозяйство
- Черчение
- Экология
- Экономика
- Электроника
- Электротехника
- Энергетика
Изучите § 43 стр. 151-155.. Строения атомов лития, натрия и калия.. Физические свойства щелочных металлов.. Литий легче воздуха в 2 раза.. Химические свойства щелочных металлов.
04. 04. 2022
Здравствуйте, ребята!
Тема «Щелочные металлы. Строения атомов лития, натрия и калия. Нахождения в природе. Способы получения. Физические и химические свойства».
Изучите § 43 стр. 151-155.
Предлагаю Вам для лучшего усвоения материала ссылку на видеоурок:
https: //resh. edu. ru/subject/lesson/1602/main/
Мы продолжаем изучать тему «Металлы», сегодня изучим щелочные металлы.
Щелочные металлы в периодической таблице Д. И. Менделеева находятся в главной подгруппе (А - подгруппе) в I группе. Это элементы: Li, Na, K, Rb, Cs, Fr. (см. рисунок)
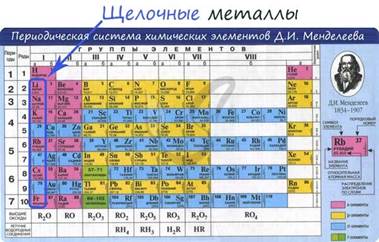
Практическое значение имеют Li, Na, K поэтому мы поговорим о них.
Строения атомов лития, натрия и калия.
Из рисунка видно, что на внешнем энергетическом
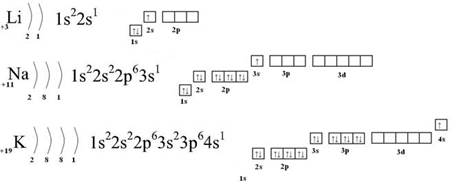
Из рисунка видно, что на внешнем энергетическом уровне элементов 1 электрон, который они легко отдают в химических реакциях и во всех соединениях проявляют степень окисления + 1.
Пример, Na2+1O, Na+1OH, K+2SO4, Li+1NO3.
Физические свойства щелочных металлов.


Литий легче воздуха в 2 раза.
Обратите внимание: щелочные металлы из-за своей активности в лабораториях хранятся под слоем керосина или машинного масла, а также в запаянных ампулах.
Химические свойства щелочных металлов.
Обратите внимание: щелочные металлы являются сильными восстановителями.
1. Металлы и их соединения способны окрашивать пламя:

Обратите внимание: это реакции взаимодействия щелочных металлов с кислородом, причем продукты реакции будут разные:
Li + O2 → Li2O (оксид лития)
2Na + O2 → Na2O2 (пероксид натрия)
K + O2 → KO2 (надпероксид)
2. Взаимодействуют щелочные металлы с неметаллами:

|
|
|
© helpiks.su При использовании или копировании материалов прямая ссылка на сайт обязательна.
|