
- Автоматизация
- Антропология
- Археология
- Архитектура
- Биология
- Ботаника
- Бухгалтерия
- Военная наука
- Генетика
- География
- Геология
- Демография
- Деревообработка
- Журналистика
- Зоология
- Изобретательство
- Информатика
- Искусство
- История
- Кинематография
- Компьютеризация
- Косметика
- Кулинария
- Культура
- Лексикология
- Лингвистика
- Литература
- Логика
- Маркетинг
- Математика
- Материаловедение
- Медицина
- Менеджмент
- Металлургия
- Метрология
- Механика
- Музыка
- Науковедение
- Образование
- Охрана Труда
- Педагогика
- Полиграфия
- Политология
- Право
- Предпринимательство
- Приборостроение
- Программирование
- Производство
- Промышленность
- Психология
- Радиосвязь
- Религия
- Риторика
- Социология
- Спорт
- Стандартизация
- Статистика
- Строительство
- Технологии
- Торговля
- Транспорт
- Фармакология
- Физика
- Физиология
- Философия
- Финансы
- Химия
- Хозяйство
- Черчение
- Экология
- Экономика
- Электроника
- Электротехника
- Энергетика
Функция распределения Максвелла
Функция распределения Максвелла
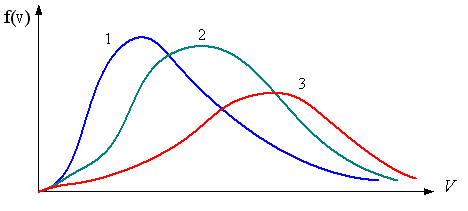 1. В трех одинаковых сосудах находится одинаковое количество одного и того же газа при разных температурах. Функцию распределения молекул по скоростям в сосуде с максимальной температурой будет описывать кривая, обозначенная номером…
1. В трех одинаковых сосудах находится одинаковое количество одного и того же газа при разных температурах. Функцию распределения молекул по скоростям в сосуде с максимальной температурой будет описывать кривая, обозначенная номером…
2. Правильные утверждения о средней квадратичной скорости ( 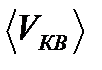 ) частиц системы, подчиняющейся распределению Максвелла:
) частиц системы, подчиняющейся распределению Максвелла:
1) При одинаковой температуре 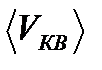 молекул различных идеальных газов одинакова.
молекул различных идеальных газов одинакова.
2) Средняя квадратичная скорость 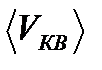 молекул газа при любой температуре меньше наиболее вероятной скорости.
молекул газа при любой температуре меньше наиболее вероятной скорости.
3) Чем больше масса молекулы газа, тем меньше 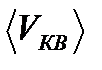 .
.
4) При возрастании температуры системы в четыре раза средняя квадратичная скорость 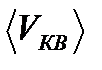 молекул увеличивается в два раза.
молекул увеличивается в два раза.
3. В сосуде находятся одинаковые количества азота N2 (M1 = 28 г/моль) и водорода H2 (M2 = 2 г/моль). Функции распределения молекул этих газов по скоростям будут описываться кривыми, изображенными на рисунке под номером
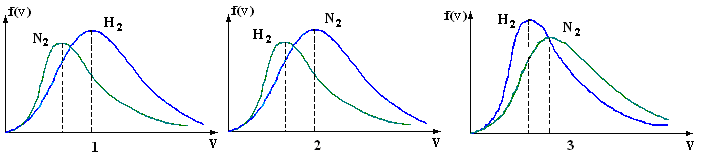
1) 1 2) 2 3) 3 4) правильного рисунка нет
4. Если при нагревании некоторого газа наиболее вероятная скорость молекул газа увеличилась в 2 раза, то средняя квадратичная скорость … раз(а).
1) увеличится в 4 2) уменьшится в 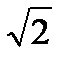 3) уменьшится в 8 4) увеличится в 2
3) уменьшится в 8 4) увеличится в 2
5. Три газа: водород (M1 = 2 г/моль), гелий (M2 = 4 г/моль) и кислород (M3 = 32 г/моль) находятся при одинаковой температуре T. Тогда значение f(Vвер) функции распределения Максвелла, соответствующее наиболее вероятной скорости молекул,..
1)одинаково для всех газов 2) максимально для водорода 3) минимально для гелия 4) максимально для кислорода:
6. В статистике Максвелла функция распределения имеет вид 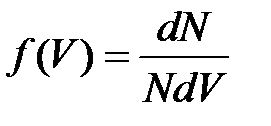 . НЕВЕРНОЕ утверждение о функции Максвелла –
. НЕВЕРНОЕ утверждение о функции Максвелла –
1) f(V) - вероятность того, что скорость данной молекулы находится в единичном интервале скоростей вблизи заданной скорости V.
2) f(V)dV - вероятность того, что скорость данной молекулы заключена в интервале скоростей от V до V+dV.
3) f(V) - относительное число молекул, скорости которых заключены в интервале скоростей от V до V+dV.
4) f(V)NdV - абсолютное число молекул, скорости которых заключены в интервале скоростей от V до V+dV.
7. 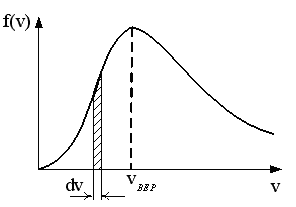 На рисунке представлен график функции распределения молекул идеального газа по скоростям (распределение Максвелла), где
На рисунке представлен график функции распределения молекул идеального газа по скоростям (распределение Максвелла), где 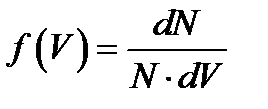 - доля молекул, скорости которых заключены в интервале от
- доля молекул, скорости которых заключены в интервале от 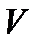 до
до 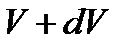 в расчете на единицу этого интервала. Если, не меняя температуры, взять другой газ с большей молярной массой и таким же числом молекул, то
в расчете на единицу этого интервала. Если, не меняя температуры, взять другой газ с большей молярной массой и таким же числом молекул, то
1) величина максимума уменьшится
2) площадь под кривой увеличится
3) максимум кривой сместится влево, в сторону меньших скоростей
4) максимум кривой сместится вправо, в сторону больших скоростей
|
|
|
© helpiks.su При использовании или копировании материалов прямая ссылка на сайт обязательна.
|