
- Автоматизация
- Антропология
- Археология
- Архитектура
- Биология
- Ботаника
- Бухгалтерия
- Военная наука
- Генетика
- География
- Геология
- Демография
- Деревообработка
- Журналистика
- Зоология
- Изобретательство
- Информатика
- Искусство
- История
- Кинематография
- Компьютеризация
- Косметика
- Кулинария
- Культура
- Лексикология
- Лингвистика
- Литература
- Логика
- Маркетинг
- Математика
- Материаловедение
- Медицина
- Менеджмент
- Металлургия
- Метрология
- Механика
- Музыка
- Науковедение
- Образование
- Охрана Труда
- Педагогика
- Полиграфия
- Политология
- Право
- Предпринимательство
- Приборостроение
- Программирование
- Производство
- Промышленность
- Психология
- Радиосвязь
- Религия
- Риторика
- Социология
- Спорт
- Стандартизация
- Статистика
- Строительство
- Технологии
- Торговля
- Транспорт
- Фармакология
- Физика
- Физиология
- Философия
- Финансы
- Химия
- Хозяйство
- Черчение
- Экология
- Экономика
- Электроника
- Электротехника
- Энергетика
Практическая работа № 1 «Приготовление раствора заданной концентрации».
Практическая работа № 1 «Приготовление раствора заданной концентрации».
Теоретическая часть:
Растворы играют важную роль в живой и неживой природе, а также в науке и технике.
Большинство физиологических процессов в организмах человека, животных и в растениях, различных промышленных процессов, биохимических процессов в почвах и т. п. протекают в растворах. Раствор – это гомогенная многокомпонентная система, в которой одно вещество распределено в среде другого или других веществ.
Растворы могут быть в газообразном (воздух), жидком и твердом (сплавы, цветные стекла) агрегатных состояниях. Содержание данного вещества в единице массы или объема раствора называется концентрацией раствора. На практике наиболее часто пользуется такой способ выражения концентрации как массовая доля – отношение массы данного компонента в растворе к общей массе этого раствора. Массовая доля может быть выражена в долях единицы, процентах (%), промилле (тысячная часть %) и в миллионных долях (млнˉ 1). Массовая доля данного компонента, выраженная в процентах, показывает, сколько граммов данного компонента cодержится в 100 г раствора.
Для приготовления определённого раствора нужной концентрации обычно составляют пропорцию, где за x принимают массу вещества, которую необходимо растворить, для получения раствора необходимой концентрации. При этом необходимо вычитать массу растворённого вещества из массы раствора, чтобы найти массу растворителя.
Задание 1. Приготовить 200 г раствора соли, массовая доля которого 20% или 0, 2.
Алгоритм решения
| Дано: m (р-ра) =200 г ω (соли)=20%=0, 2 m (соли) =25 г | Решение
1. Вычисляем массу соли в растворе по формуле:
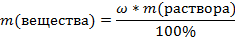 m (Н2О)= m (р-ра) - m (соли)
2. Подставим цифровые данные в эту формулу и произведем расчет
m (соли)=0, 2*200 г=40 г
m (Н2О)= 200 г-40 г= 160 г.
m (Н2О)= m (р-ра) - m (соли)
2. Подставим цифровые данные в эту формулу и произведем расчет
m (соли)=0, 2*200 г=40 г
m (Н2О)= 200 г-40 г= 160 г.
|
Определить  : m (соли) -?
m (Н2О)-? : m (соли) -?
m (Н2О)-?
| m (соли) =40г m (Н2О=160 г. |
Задания для практической работы №1
1. Решить предложенные задачи.
2. Правильно оформить их в тетрадь.
3. Ответить на вопросы для контроля.
|
|
|
© helpiks.su При использовании или копировании материалов прямая ссылка на сайт обязательна.
|