
- Автоматизация
- Антропология
- Археология
- Архитектура
- Биология
- Ботаника
- Бухгалтерия
- Военная наука
- Генетика
- География
- Геология
- Демография
- Деревообработка
- Журналистика
- Зоология
- Изобретательство
- Информатика
- Искусство
- История
- Кинематография
- Компьютеризация
- Косметика
- Кулинария
- Культура
- Лексикология
- Лингвистика
- Литература
- Логика
- Маркетинг
- Математика
- Материаловедение
- Медицина
- Менеджмент
- Металлургия
- Метрология
- Механика
- Музыка
- Науковедение
- Образование
- Охрана Труда
- Педагогика
- Полиграфия
- Политология
- Право
- Предпринимательство
- Приборостроение
- Программирование
- Производство
- Промышленность
- Психология
- Радиосвязь
- Религия
- Риторика
- Социология
- Спорт
- Стандартизация
- Статистика
- Строительство
- Технологии
- Торговля
- Транспорт
- Фармакология
- Физика
- Физиология
- Философия
- Финансы
- Химия
- Хозяйство
- Черчение
- Экология
- Экономика
- Электроника
- Электротехника
- Энергетика
ЛАБОРАТОРНАЯ РАБОТА. ОПРЕДЕЛЕНИЕ ПИЩЕВОЙ УКСУСНОЙ КИСЛОТЫ. МЕТОДОМ КИСЛОТНО-ОСНОВНОГО ТИТРОВАНИЯ. Отчет по работе. 3. Выполнение работы. 1 этап работы
ЛАБОРАТОРНАЯ РАБОТА
ОПРЕДЕЛЕНИЕ ПИЩЕВОЙ УКСУСНОЙ КИСЛОТЫ
МЕТОДОМ КИСЛОТНО-ОСНОВНОГО ТИТРОВАНИЯ
Отчет по работе
Выполнил:
ФИО: Юдакова Арина Сергеевна
Группа: 0482
Проверил:
Воронова О. А., к. х. н., доцент ОХИ ИШПР
1. Цель работы: Определить точную концентрацию пищевой уксусной кислоты.
2. Теоретическая часть:
В основе определения концентрации уксусной кислоты лежит реакция:
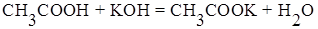
рН раствора в точке эквивалентности определяется присутствием соли CH3COOK, гидролизующейся по аниону, и рассчитывается по формуле:
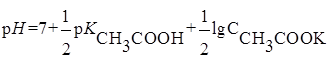

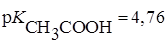 ,
, 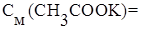 0, 1 моль/л (без учета разбавления).
0, 1 моль/л (без учета разбавления).
Следовательно, при титровании раствора СH3COOH щелочью следует применять фенолфталеин (поскольку рН интервал перехода окраски индикатора составляет 8 – 10, а показатель титрования рТ = 9).
3. Выполнение работы
1 этап работы
Представим себя химиком-лаборантом в экспертной лаборатории, который должен определить являются ли представленные образцы истинной пищевой уксусной кислотой или разбавленным фальсификатом. Исследуемым объектом является пищевая уксусная кислота (70% раствор), приобретенная по контрольной закупке в ряде магазинов.
Прежде чем приступить к непосредственно титрованию, рассчитаем какой объем титранта приблизительно должен пойти на титрование 10 мл исследуемого образца (70% СH3COOH), чтобы узнать какой объем титранта нужно приготовить для работы ( Комментарий: в аккредитованных лабораториях необходимые для работы разбавленные растворы не хранятся, их готовят непосредственно перед работой)
Для этого в таблице плотностей и концентраций кислот находят, какой приблизительной молярной концентрации соответствует 70%-ный раствор СH3COOH. Из таблицы находим, что концентрация 70% соответствует приблизительно концентрации 12. 5 моль-экв/л.
Концентрация титранта щелочи 0. 1 моль-экв/л. Соответственно, рассчитав по закону эквивалентов объем титранта, пошедшего на титрование исследуемого образца получим:
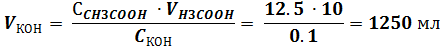
!!! Делаем вывод – чтобы 1 раз оттитровать 10 мл исследуемого образца (70% СH3COOH) необходимо затратить больше 1 л титранта (а с учетом того, что объем бюретки 25 мл, то на титрование придется заполнять бюретку слить как минимум 50 раз). А таких измерений нужно сделать как минимум до трех сходимых результатов. Потратить 4 литра титранта и драгоценное время химик-эксперт не может себе позволить, поскольку таких образцов для экспертизы может быть больше 100 в день (не рентабельно и не экспрессно)
Поэтому существует правило – раствор исследуемого образца разбавляют до концентрации, приблизительно равной концентрации рабочего раствора титранта, чтобы использовать небольшое количество для титрования.
Например, концентрация титранта 0. 1 моль-экв/л, соответственно мы должны приготовить разбавленный раствор уксусной кислоты с концентрацией приблизительно 0. 1 моль-экв/л и взять для титрования аликвоту 10 мл, тогда титранта пойдет следующее количество:

Получаем, что расход титранта не превышает объема одной бюретки (25 мл)
|
|
|
© helpiks.su При использовании или копировании материалов прямая ссылка на сайт обязательна.
|