
- Автоматизация
- Антропология
- Археология
- Архитектура
- Биология
- Ботаника
- Бухгалтерия
- Военная наука
- Генетика
- География
- Геология
- Демография
- Деревообработка
- Журналистика
- Зоология
- Изобретательство
- Информатика
- Искусство
- История
- Кинематография
- Компьютеризация
- Косметика
- Кулинария
- Культура
- Лексикология
- Лингвистика
- Литература
- Логика
- Маркетинг
- Математика
- Материаловедение
- Медицина
- Менеджмент
- Металлургия
- Метрология
- Механика
- Музыка
- Науковедение
- Образование
- Охрана Труда
- Педагогика
- Полиграфия
- Политология
- Право
- Предпринимательство
- Приборостроение
- Программирование
- Производство
- Промышленность
- Психология
- Радиосвязь
- Религия
- Риторика
- Социология
- Спорт
- Стандартизация
- Статистика
- Строительство
- Технологии
- Торговля
- Транспорт
- Фармакология
- Физика
- Физиология
- Философия
- Финансы
- Химия
- Хозяйство
- Черчение
- Экология
- Экономика
- Электроника
- Электротехника
- Энергетика
1.1 Количество вещества. 1.2 Основное уравнение молекулярно-кинетической теории идеального газа. 1.3 Средняя квадратичная скорость молекул идеального газа. 1.4 Средняя кинетическая энергия молекулы одноатомного газа. 1.5 Давление идеального газа. 1.6 Зако
Молекулярная физика Основные формулы
1. Основы молекулярно-кинетической теории. Газовые законы
1. 1 Количество вещества
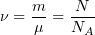
m — масса;
μ — молярная масса вещества;
N — число молекул;
NA = 6, 02·1023 моль-1 — число Авогадро
1. 2 Основное уравнение молекулярно-кинетической теории идеального газа
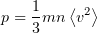
p — давление идеального газа;
m — масса одной молекулы;
n = N/V — концентрация молекул;
V — объем газа;
N — число молекул;
 — среднее значение квадрата скорости молекул.
— среднее значение квадрата скорости молекул.
1. 3 Средняя квадратичная скорость молекул идеального газа
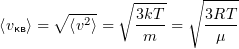
k = 1, 38·10-23 Дж/К — постоянная Больцмана;
R = kNA = 8, 31 Дж/(моль·К) — универсальная газовая постоянная;
T = t+273 — абсолютная температура;
t — температура по шкале Цельсия.
1. 4 Средняя кинетическая энергия молекулы одноатомного газа
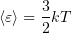
1. 5 Давление идеального газа
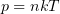
n — концентрация молекул;
k — постоянная Больцмана;
T — абсолютная температура.
1. 6 Закон Бойля-Мариотта

p — давление;
V — объем газа.
1. 7 Закон Шарля

p0 — давление газа при 0 °С;
α = 1/273 °C-1 — температурный коэффициент давления.
1. 8 Закон Гей-Люссака
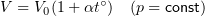
V0 — объем газа при 0 °С.
1. 9 Уравнение Менделеева-Клапейрона
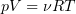
1. 10 Объединенный закон газового состояния (уравнение Клапейрона)

1. 11 Закон Дальтона
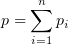
pi — парциальное давление i-й компоненты смеси газов.
2. Основы термодинамики
|
|
|
© helpiks.su При использовании или копировании материалов прямая ссылка на сайт обязательна.
|