
- Автоматизация
- Антропология
- Археология
- Архитектура
- Биология
- Ботаника
- Бухгалтерия
- Военная наука
- Генетика
- География
- Геология
- Демография
- Деревообработка
- Журналистика
- Зоология
- Изобретательство
- Информатика
- Искусство
- История
- Кинематография
- Компьютеризация
- Косметика
- Кулинария
- Культура
- Лексикология
- Лингвистика
- Литература
- Логика
- Маркетинг
- Математика
- Материаловедение
- Медицина
- Менеджмент
- Металлургия
- Метрология
- Механика
- Музыка
- Науковедение
- Образование
- Охрана Труда
- Педагогика
- Полиграфия
- Политология
- Право
- Предпринимательство
- Приборостроение
- Программирование
- Производство
- Промышленность
- Психология
- Радиосвязь
- Религия
- Риторика
- Социология
- Спорт
- Стандартизация
- Статистика
- Строительство
- Технологии
- Торговля
- Транспорт
- Фармакология
- Физика
- Физиология
- Философия
- Финансы
- Химия
- Хозяйство
- Черчение
- Экология
- Экономика
- Электроника
- Электротехника
- Энергетика
Тема урока: Соли и их свойства
Тема урока: "Соли и их свойства"
Соли - это сложные вещества, состоящие из ионов металлов и кислотного остатка.
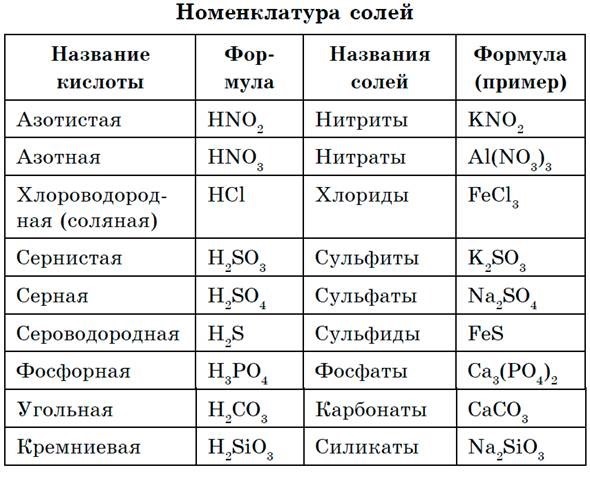
Кислотный остаток образуется, если в формуле кислоты убрать атомы водорода. Заряд кислотного остатка определяется числом атомов водорода в молекуле кислоты.
Нужно уметь называть соли по формулам и строить формулы по названиям.
Алгоритм (1) называния соли по формуле.
1. Определить степени окисления металла и кислотного остатка (по таблице растворимости, по формуле).
2. Определить по кислотному остатку, какой кислоте соответствует соль, каково название соли.
3. К названию соли добавить русское название металла в родительном падеже, указать в скобках римской цифрой степень окисления металла (если она не постоянна).
Пример: Fe2(SO4)3
+3 -2
1. Fe2(SO4)3
2. Сульфат - соль H2SO4 (серной кислоты)
3. Сульфат железа (III).
Упражнение. Назвать FeSO4, Cr(NO3)3, Cr(NO3)2, Cu2SO3, CuCl2.
Алгоритм (2) построения формул солей по названию.
1. Слева записать металл, указанный в названии, над ним - степень окисления (из названия, из таблицы растворимости).
2. По названию соли определить, какой кислоте она соответствует, кислотный остаток записать справа от металла, над ним написать степень окисления (из таблицы растворимости).
3. Снести степень окисления крест-накрест.
4. Если надо, индексы сократить.
! Если после кислотного остатка должен быть индекс, кислотный остаток берется в скобки.
Пример: нитрат меди (II):
+2
1. Сu.
2. Нитрат - соль азотной кислоты HNO3, ее кислотный остаток NO3-.
+2 -1
Сu NO3
+2 -1
3. Сu (NO3)2
Упражнение.Составьте формулы: сульфит магния, бромид хрома (III), ортофосфат бария, сульфат алюминия.
|
|
|
© helpiks.su При использовании или копировании материалов прямая ссылка на сайт обязательна.
|