
- Автоматизация
- Антропология
- Археология
- Архитектура
- Биология
- Ботаника
- Бухгалтерия
- Военная наука
- Генетика
- География
- Геология
- Демография
- Деревообработка
- Журналистика
- Зоология
- Изобретательство
- Информатика
- Искусство
- История
- Кинематография
- Компьютеризация
- Косметика
- Кулинария
- Культура
- Лексикология
- Лингвистика
- Литература
- Логика
- Маркетинг
- Математика
- Материаловедение
- Медицина
- Менеджмент
- Металлургия
- Метрология
- Механика
- Музыка
- Науковедение
- Образование
- Охрана Труда
- Педагогика
- Полиграфия
- Политология
- Право
- Предпринимательство
- Приборостроение
- Программирование
- Производство
- Промышленность
- Психология
- Радиосвязь
- Религия
- Риторика
- Социология
- Спорт
- Стандартизация
- Статистика
- Строительство
- Технологии
- Торговля
- Транспорт
- Фармакология
- Физика
- Физиология
- Философия
- Финансы
- Химия
- Хозяйство
- Черчение
- Экология
- Экономика
- Электроника
- Электротехника
- Энергетика
Тема: Тепловые эффекты химических реакций. Расчёты по термохимическим уравнениям.
Тема: Тепловые эффекты химических реакций. Расчёты по термохимическим уравнениям.
Количество теплоты, которое выделяется или поглощается при химической реакции, называют тепловым эффектом реакции.
Тепловой эффект обозначается Q и измеряется в Дж или кДж.
Химические уравнения, в которых указывается тепловой эффект, называют термохимическими.
Например: 2HgO(тв) = 2Hg(тв) + O2(Г) - 180 кДж, С(тв) + O2(г) = СO2(г) + 394 кДж
Раздел химии, в задачу которого входит определение и изучение тепловых эффектов реакции называется Термохимией.
Реакции протекающие с выделением энергии называются ЭКЗОТЕРМИЧЕСКИМИ(от латинского "экзо" – наружу). Например, горение метана:
CH4 + 2O2 = CO2 + 2H2O + Q
Реакции протекающие с поглощением энергии называются ЭНДОТЕРМИЧЕСКИМИ(от латинского "эндо" - внутрь). Примером является образование оксида углерода (II) CO и водорода H2 из угля и воды, которое происходит только при нагревании.
C + H2O = CO + H2 – Q
Тепловые эффекты химических реакций нужны для многих технических расчетов.
II. Расчёты по термохимическим уравнениям (ТХУ): алгоритмы
Алгоритм №1
Задача 1. По термохимическому уравнению 2Cu + O2 = 2CuO + 310 кДж вычислите количество теплоты, выделившейся в результате окисления 4 моль меди.
Алгоритм решения
1. Над формулами веществ надпишем сведения, взятые из условия задачи, а под формулой – соотношение, отображаемое уравнением реакции
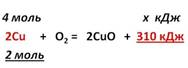
2. Находим выделившееся количество теплоты, решая пропорцию:
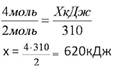
Ответ: количество выделившейся теплоты 620 кДж.
|
|
|
© helpiks.su При использовании или копировании материалов прямая ссылка на сайт обязательна.
|