
- Автоматизация
- Антропология
- Археология
- Архитектура
- Биология
- Ботаника
- Бухгалтерия
- Военная наука
- Генетика
- География
- Геология
- Демография
- Деревообработка
- Журналистика
- Зоология
- Изобретательство
- Информатика
- Искусство
- История
- Кинематография
- Компьютеризация
- Косметика
- Кулинария
- Культура
- Лексикология
- Лингвистика
- Литература
- Логика
- Маркетинг
- Математика
- Материаловедение
- Медицина
- Менеджмент
- Металлургия
- Метрология
- Механика
- Музыка
- Науковедение
- Образование
- Охрана Труда
- Педагогика
- Полиграфия
- Политология
- Право
- Предпринимательство
- Приборостроение
- Программирование
- Производство
- Промышленность
- Психология
- Радиосвязь
- Религия
- Риторика
- Социология
- Спорт
- Стандартизация
- Статистика
- Строительство
- Технологии
- Торговля
- Транспорт
- Фармакология
- Физика
- Физиология
- Философия
- Финансы
- Химия
- Хозяйство
- Черчение
- Экология
- Экономика
- Электроника
- Электротехника
- Энергетика
Закономерности изменения свойств химических элементов и их соединений по периодам и группам
Дата 29.10.2020
Тема: закономерности изменения химических элементов и их соединений по периодам группам свойств элементов
Цели урока:
Обучающая: закрепить знание причины изменения свойств элементов на основании положения в системе; научить обоснованно объяснять и сравнивать свойства элементов, а также образованных ими простых и сложных веществ; научить давать полную характеристику химического элемента в ПСХЭ.
Развивающая: продолжить формирование умений сравнивать, обобщать, прогнозировать и объяснять свойства веществ, устанавливать причинно-следственные связи, делать выводы, уметь выделять главное из общего. Совершенствование коммуникативных умений и информационно-познавательной компетентности, развивать самостоятельность и творчество при решении практических задач.
Воспитательная: воспитание ответственного отношения к учёбе, трудолюбия, работоспособности, правильной самооценки, умение работать в коллективе, осуществление экологического, гигиенического и нравственного воспитания, формирование здорового образа жизни.
Закономерности изменения свойств химических элементов и их соединений по периодам и группам
Химические свойства элементов (а уж тем более их соединений!) напрямую зависят от строения атома.
Не надо учить наизусть химические свойства каждого атома, не надо зазубривать химические реакции… ответ на любой вопрос по химии находится в Периодической системе элементов.
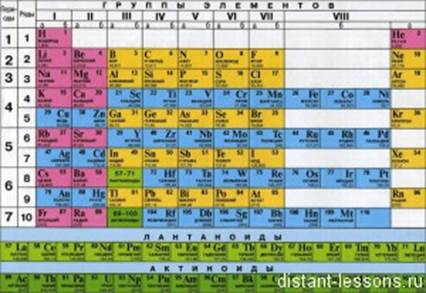
Как изменяются электронные конфигурации s-, p-элементов (по группам и периодам) и d-элементов, тоже можно почитать отдельно.
Давайте рассмотрим, как изменяются свойства химических элементов в группах и в периодах.
1. Изменения свойств химических элементов и их соединений в группах:
В группах все элементы имеют сходное электронное строение. Различий в наполнении внешнего энергетического уровня электронами нет.
· Меняется размер атома —сверху вниз в группе радиусы атомов увеличиваются!
Что это означает? Это означает, что
1) внешние электроны все слабее притягиваются к ядру атома;
2) возрастает способность атома отдавать электроны.
3) способность отдавать электроны=металлические свойства, т.е.
закономерность изменения химических свойств элементов и их соединений в группах:
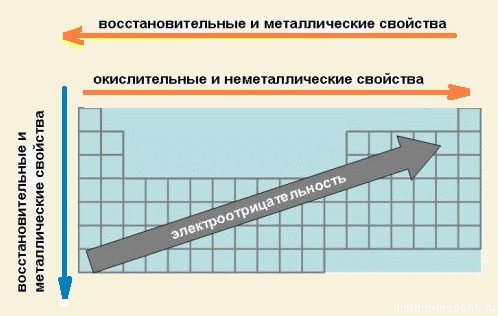
· В группах сверху вниз возрастают металлические свойства элементов
· усиливаются основные свойства их соединений
Изменения химических свойств элементов и их соединений в периодах:
В периодах наблюдается несколько другая картина:
1) Слева направо в периодах радиусы атомов уменьшаются;
2) количество электронов на внешнем слое при этом увеличивается;
3) электроотрицательность элементов = неметаллические свойства увеличивается
закономерности изменения химических свойств элементов и их соединений в периодах:
· В периодах слева направо возрастают неметаллические свойства элементов, электроотрицательность;
· усиливаются кислотные свойства их соединений
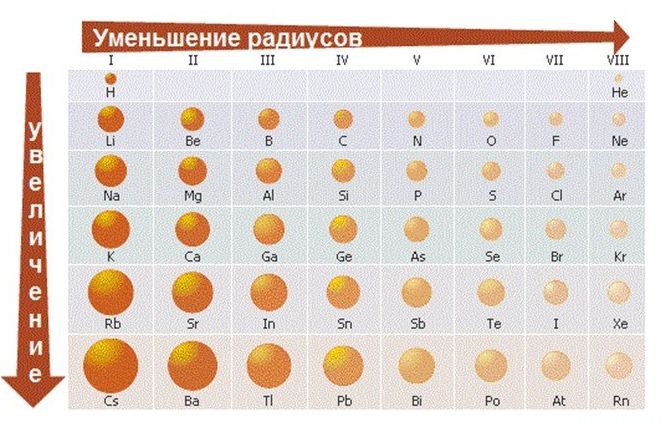

Исходя из этих соображений получается, что звание «Король Неметаллов» у нас присуждается… (барабанная дробь)… F ! Рядом с ним даже кислород (O) проявляет положительную степень окисления: OF2 — бесцветный ядовитый газ с неприятным запахом.
Итак, подведем итог:
С увеличением заряда ядра атомов наблюдается постепенное закономерное изменение свойств элементов и их соединений от металлических к типично неметаллическим, что связано с увеличением числа электронов на внешнем энергетическом уровне.
Есть еще элементы, которые образуют так называемые амфотерные соединения. Они проявляют как металлические, так и неметаллические свойства.
Домашнее задание:
1. Изучить и записать в тетрадь конспект
2. Просмотреть обучающее видео
https://www.youtube.com/watch?v=aIW7Fkw0w9g&feature=emb_title
|
|
|
© helpiks.su При использовании или копировании материалов прямая ссылка на сайт обязательна.
|