
- Автоматизация
- Антропология
- Археология
- Архитектура
- Биология
- Ботаника
- Бухгалтерия
- Военная наука
- Генетика
- География
- Геология
- Демография
- Деревообработка
- Журналистика
- Зоология
- Изобретательство
- Информатика
- Искусство
- История
- Кинематография
- Компьютеризация
- Косметика
- Кулинария
- Культура
- Лексикология
- Лингвистика
- Литература
- Логика
- Маркетинг
- Математика
- Материаловедение
- Медицина
- Менеджмент
- Металлургия
- Метрология
- Механика
- Музыка
- Науковедение
- Образование
- Охрана Труда
- Педагогика
- Полиграфия
- Политология
- Право
- Предпринимательство
- Приборостроение
- Программирование
- Производство
- Промышленность
- Психология
- Радиосвязь
- Религия
- Риторика
- Социология
- Спорт
- Стандартизация
- Статистика
- Строительство
- Технологии
- Торговля
- Транспорт
- Фармакология
- Физика
- Физиология
- Философия
- Финансы
- Химия
- Хозяйство
- Черчение
- Экология
- Экономика
- Электроника
- Электротехника
- Энергетика
Тема: Ковалентная связь. Образуется общая электронная пара
Дата15.10.2020
Тема: Ковалентная связь
ЦЕЛЬ:сформировать у учащихся знания о ковалентной химической связи
Ковалентная связь — химическая связь, образованная перекрытием (обобществлением) пары валентных электронных облаков. Обеспечивающие связь электронные облака (электроны) называются общей электронной парой.

Понятие «металлические свойства» — определяется способностью отдавать электроны — на этом основана металлическая химическая связь. Что происходит, когда встречаются атомы неметаллов?
«Неметаллические свойства» — определяются способностью принимать электроны, отбирать их у других атомов.
Давайте рассмотрим образование молекулы водорода (H2)
Первый вид ковалентной связи — ковалентная неполярная
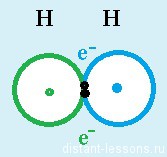
У каждого атома водорода имеется электрон. При сближении двух атомов возникает такой момент, когда оба электрона будут находиться рядом. Что получается?
Образуется общая электронная пара
У левого атома (зеленый) стало 2 электрона на орбитали — очень выгодное энергетическое состояние, и у правого атома (синий) стало 2 электрона — тоже выгодное состояние. Образуется молекула водорода.
При образовании неполярной ковалентной связи плотность равномерно распределена между обоими атомами
Получается, что ковалентная связь «стягивает» атомы в молекулы.
Второй вид ковалентной связи — ковалентная полярная
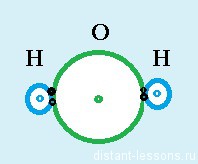
Точно таким же образом образуется молекула воды — кислород добавляет себе пару электронов, что делает его электронную оболочку завершенной, каждый атом водорода тоже становится двухэлектронным — у всех стабильное энергетическое состояние.
Образуются две электронные пары — 2 ковалентные связи.
При образовании полярной ковалентной связи — электронная плотность смещается в сторону одного из атомов. Поляризация возникает в следствии различия электроотрицательностей элементов в паре.
Третий вид химической связи — ковалентная донорно-акцепторная связь
Вообще, нельзя назвать это видом связи, это, скорее, механизм образования связи.
Донорно-акцепторный механизм — способ образования ковалентной химической связи между двумя атомами или группой атомов, осуществляемый за счет неподеленной пары электронов атома-донора и свободной орбитали атома-акцептора
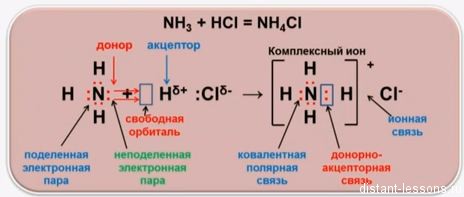
Давайте подведем итог по видам ковалентной связи:
1. Ковалентную неполярную связь образуют одинаковые атомы неметаллов и атомы водорода;
2. Ковалентную полярную химическую связь образуют разные атомы неметаллов и неметаллы с водородом;
3. Донорно-акцепторную ковалентную связь образуют атомы, имеющие неподеленную электронную пару — доноры электронов (например, азот, кислород, фосфор, сера и т.д.) и атомы, образующие пустую орбиталь — акцепторы (например, протон водорода и некоторые d-элементы.
Домашнее задание:
изобразить образование молекул Br2, CCl4
|
|
|
© helpiks.su При использовании или копировании материалов прямая ссылка на сайт обязательна.
|