
- Автоматизация
- Антропология
- Археология
- Архитектура
- Биология
- Ботаника
- Бухгалтерия
- Военная наука
- Генетика
- География
- Геология
- Демография
- Деревообработка
- Журналистика
- Зоология
- Изобретательство
- Информатика
- Искусство
- История
- Кинематография
- Компьютеризация
- Косметика
- Кулинария
- Культура
- Лексикология
- Лингвистика
- Литература
- Логика
- Маркетинг
- Математика
- Материаловедение
- Медицина
- Менеджмент
- Металлургия
- Метрология
- Механика
- Музыка
- Науковедение
- Образование
- Охрана Труда
- Педагогика
- Полиграфия
- Политология
- Право
- Предпринимательство
- Приборостроение
- Программирование
- Производство
- Промышленность
- Психология
- Радиосвязь
- Религия
- Риторика
- Социология
- Спорт
- Стандартизация
- Статистика
- Строительство
- Технологии
- Торговля
- Транспорт
- Фармакология
- Физика
- Физиология
- Философия
- Финансы
- Химия
- Хозяйство
- Черчение
- Экология
- Экономика
- Электроника
- Электротехника
- Энергетика
Закон Гесса.
Закон Гесса.

Задача 1. Вычислить 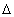 Но298 реакции N2(г) + 3H2(г) = 2NH3(г), используя следующие данные:
Но298 реакции N2(г) + 3H2(г) = 2NH3(г), используя следующие данные:
4NH3(г) + 3O2(г) = 2N2(г) + 6H2O(ж); 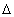 Но1 = -1531,22 кДж;
Но1 = -1531,22 кДж;
2H2O(ж) = O2(г) + 2H2(г); 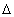 Но2= 571,66 кДж.
Но2= 571,66 кДж.
Определить стандартную энтальпию образования NH3(г).
Решение. Поскольку с термохимическими уравнениями можно производить все алгебраические действия, то искомое уравнение получится, если:
- разделить на два тепловой эффект первого уравнения и изменить его знак на противоположный, т.е:
N2(г) + 3H2O(ж) = 2NH3(г) + 3/2O2(г); 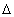 Но = 765,61 кДж;
Но = 765,61 кДж;
- умножить на 3/2 второе уравнение и соответствующую ему величину
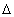 Нo , изменив ее знак на противоположный:
Нo , изменив ее знак на противоположный:
3/2O2(г) + 3H2(г) = 3H2O(ж); 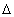 Но = -857,49 кДж;
Но = -857,49 кДж;
- сложить полученные первое и второе уравнения.
Таким образом, тепловой эффект реакции N2(г) + 3H2(г) = 2NH3(г) равен:
D Но298 = (- 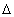 Но1/2) + (- 3/2·
Но1/2) + (- 3/2· 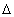 Но2) = 765,61 + (- 857,49) = - 91,88 кДж.
Но2) = 765,61 + (- 857,49) = - 91,88 кДж.
Поскольку в рассматриваемой реакции образуется 2 моль NH3(г), то
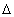 Ноf,298(NH3(г)) = - 91,88/2 = - 45,94 кДж/моль.
Ноf,298(NH3(г)) = - 91,88/2 = - 45,94 кДж/моль.
10.5. Вычислить 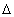 Но298 реакции
Но298 реакции
2C(г) + 2H2(г) = C2H4(г), используя следующие термохимические уравнения:
С(графит) = С(г) ; 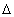 Но298 = +716,67 кДж;
Но298 = +716,67 кДж;
С2H4(г) + 3O2(г) = 2CO2(г) + 2H2O(г); 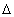 Но298 = - 1322,94 кДж;
Но298 = - 1322,94 кДж;
C(графит) + O2(г) = CO2(г); 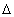 Но298 = - 393,51 кДж;
Но298 = - 393,51 кДж;
H2(г) + 1/2O2(г) = H2O(г); 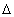 Но298 = - 241,81 кДж.
Но298 = - 241,81 кДж.
(- 1381,04 кДж)
.

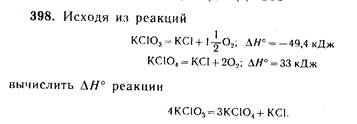
(-297 кДж)
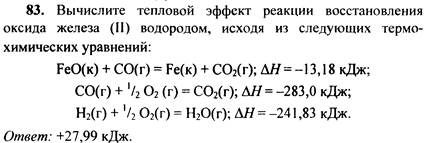



(-104, 15 кДж)
|
|
|
© helpiks.su При использовании или копировании материалов прямая ссылка на сайт обязательна.
|