
- Автоматизация
- Антропология
- Археология
- Архитектура
- Биология
- Ботаника
- Бухгалтерия
- Военная наука
- Генетика
- География
- Геология
- Демография
- Деревообработка
- Журналистика
- Зоология
- Изобретательство
- Информатика
- Искусство
- История
- Кинематография
- Компьютеризация
- Косметика
- Кулинария
- Культура
- Лексикология
- Лингвистика
- Литература
- Логика
- Маркетинг
- Математика
- Материаловедение
- Медицина
- Менеджмент
- Металлургия
- Метрология
- Механика
- Музыка
- Науковедение
- Образование
- Охрана Труда
- Педагогика
- Полиграфия
- Политология
- Право
- Предпринимательство
- Приборостроение
- Программирование
- Производство
- Промышленность
- Психология
- Радиосвязь
- Религия
- Риторика
- Социология
- Спорт
- Стандартизация
- Статистика
- Строительство
- Технологии
- Торговля
- Транспорт
- Фармакология
- Физика
- Физиология
- Философия
- Финансы
- Химия
- Хозяйство
- Черчение
- Экология
- Экономика
- Электроника
- Электротехника
- Энергетика
Решения заданий 10 класса. Тест-7 баллов. Задачи -27 баллов. Всего 8 баллов. Итого 5 баллов
Решения заданий 10 класса
Тест-7 баллов
| вопрос | |||||||
| ответ |
Задачи -27 баллов
1 СН4 + 2 О2 = СО2 + 2 Н2О 1 балл
2 С2Н6 + 7 О2 = 4 СО2 + 6 Н2О 1 балл
•Пусть масса метана в исходной смеси m (CH4) = x, тогда масса этана в смеси
m (C2H6) = (28-x) г.
• По первому уравнению реакции объём образовавшегося оксида углерода (IV):
V1 (CO2) = 22,4 x / 16 = 1,4 x л 1 балл
• По второму уравнению реакции объём образовавшегося оксида углерода (IV):
V2 (CO2) = 4 • 22,4 • (28-x) / (2 • 30) = 1,493 • (28 – x) л 1 балл
• Общий объём оксида углерода:
V (CO2) = V1(CO2) + V2 (CO2) = 1,4 x + 1,493 • (28 - x) = 41,44 (л) 1 балл
1,4 x + 41,804 – 1,493 x = 41,44; x = 4; следовательно,
m (CH4) в исходной смеси 4 г.1 балл
? (СН4) = 4 / 28 • 100% = 14,3 % 1 балл
? (С2Н6) = 100% - 14,3 % = 85,7 % 1 балл
Всего 8 баллов
2. 2KMnO4 + 5H2O2 + 3H2SO4 = K2SO4 + 2MnSO4 + 8H2O + 5O2 3 балла
3. 1.Количество реагентов: углекислого газа 10: 22,4 = 0,466 (моль); щелочи 30 : 40 = 0,75 (моль)(1 балл)
2. Питьевую соду (гидрокарбонат натрия) можно получить так: NaOH + CO2 = NaHCO3.(0,5 балл)
3. 0,446 моль СО2, реагируют с 0,446 моль щелочи, т.е. CO2 у нас недостаток, ведем расчет по нему: m(NaHCO3) = 0,446∙Mr(NaHCO3) = 37,5 (г).(1балл)
4. Кальцинированную соду (карбонат натрия) можно получить так: 2NaOH + CO2 = Na2CO3 + H2O. (0,5 балл)
5.0,75 моль щелочи реагируют с 0,375 моль CO2 , т.е. NaOH недостаток, следовательно: m(Na2CO3) = 0,375 ∙Mr(Na2CO3) = 39,75 (г). (1 балл)
6.Кристаллическая сода - это декагидрат карбоната натрия (Na2CO3∙ 10H2O). (1 балл)
7.Кристаллической соды можно получить столько же, сколько и кальцинированной соды, т.е. 0,375 моль. Её масса составит 0,375∙Mr(Na2CO3∙ 10H2O) = 107,25 (г).(1 балл)
4.Нахождение относительной молекулярной массы искомого вещества
Mr (вещ-ва)= DCH4*Mr(CH4)=4,625*16=74 1 балл
СxHYOZ – общая формула искомого вещества
Нахождение количества атомов элементов, входящих в состав искомого вещества
|
|
x:y:z = 12 1 16 = 4:10:1 С4Н10О – простейшая формула 1 балл
Нахождение истинной формулы
Mr(С4Н10О) = 74 = Mr(вещ-ва)
С4Н10О – истинная формула 1 балл
Структурная формула и название вещества
СН3 – СН2 – СН2 – СН2 – СН2 – ОН бутанол 2 балла
Итого 5 баллов
| Вещества | 1. NaOH | 2 НСl | 3. К2СО3 | 4. Аl2(SO4)3 | Общий результат наблюдения | |
| 1, NaOH | X | — | — | Al(OH)3 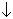
| 1 осадок | |
| 2. НС1 | _ | X | CO2 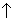
| __ | 1 газ | |
| 3. К2СО3 | — | CO2 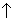
| X | Al(OH)3 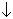 CO2 CO2 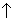
| 1 осадок и 2 газа | |
| 4. Al2(S04)3 | А1(ОН)3 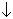
| — | А1(ОН)3 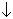 CO2 CO2 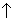
| X | 2 осадка и 1 газ | |
| NaOH + HCl = NaCl + H2O | ||||||
| К2СO3 + 2HC1 = 2КС1 + Н2O + СO2 | ||||||
| 3K2CO3 + Al2(SO4)3 + 3H2O = 2Al(OH)3 | ||||||
| Al2(SO4)3 + 6NaOH = 2Al(OH)3 Al(OH)3 + NaOH + 2H2O = Na[Al(OH)4(H2O)2] ( наличие осадка зависит от порядка сливания и избытка и щелочи) | ||||||
Всего-34балла
|
|
|
© helpiks.su При использовании или копировании материалов прямая ссылка на сайт обязательна.
|