
- Автоматизация
- Антропология
- Археология
- Архитектура
- Биология
- Ботаника
- Бухгалтерия
- Военная наука
- Генетика
- География
- Геология
- Демография
- Деревообработка
- Журналистика
- Зоология
- Изобретательство
- Информатика
- Искусство
- История
- Кинематография
- Компьютеризация
- Косметика
- Кулинария
- Культура
- Лексикология
- Лингвистика
- Литература
- Логика
- Маркетинг
- Математика
- Материаловедение
- Медицина
- Менеджмент
- Металлургия
- Метрология
- Механика
- Музыка
- Науковедение
- Образование
- Охрана Труда
- Педагогика
- Полиграфия
- Политология
- Право
- Предпринимательство
- Приборостроение
- Программирование
- Производство
- Промышленность
- Психология
- Радиосвязь
- Религия
- Риторика
- Социология
- Спорт
- Стандартизация
- Статистика
- Строительство
- Технологии
- Торговля
- Транспорт
- Фармакология
- Физика
- Физиология
- Философия
- Финансы
- Химия
- Хозяйство
- Черчение
- Экология
- Экономика
- Электроника
- Электротехника
- Энергетика
Алгоритм «Составление ионных уравнений»
⇐ ПредыдущаяСтр 2 из 2
Алгоритм «Составление ионных уравнений»
| Программа деятельности | Пример |
| 1. Записатьмолекулярное уравнение а) Определить растворимость каждого вещества | Молекулярное уравнение 3NaOH + FeCl3 = Fe(OH)3↓+ 3 NaCl P P H P |
| 2. Составить полное ионное уравнение коэффициенты перед молекулами = коэффициентам перед ионами а) Найти одинаковые ионы и сократить их в правой и левой части | Полное ионное уравнение 3Na+ + 3OH- + Fe3+ + 3Cl- = Fe(OH)3↓+ Na+ + 3Cl- 3Na+ + 3OH- + Fe3+ + 3Cl- = Fe(OH)3↓+ 3Na+ + 3Cl- |
| 3.Составить сокращенное ионное уравнение а) Выписать формулы оставшихся ионов и веществ б) Сумма зарядов ионов в левой и правой части уравнения должна быть одинакова | Сокращенное ионное уравнение 3OH- + Fe3+ = Fe(OH)3↓ |
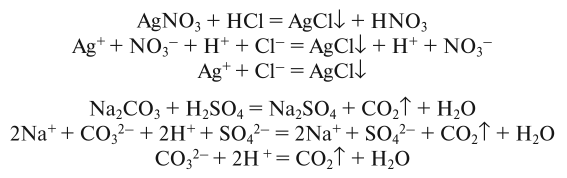
Реакции ионного обмена идут до конца:
Запомните!
Если выделится газ- это раз.
И получитсявода - это два.
А еще - нерастворимый осаждается продукт.
«Есть осадок», - говорим мы.
Это третий важный пункт.
Химик « правила обмена » не забудет никогда:
В результате - непременно будет газ или вода,
Выпадет осадок – вот тогда порядок!
Задание: Какие из реакций обмена будут протекать до конца? Для ответа воспользуйтесь таблицей растворимости гидроксидов и солей в воде.
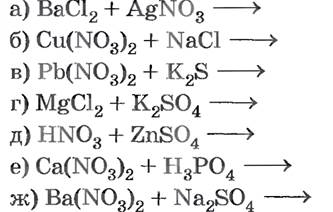
Составьте полное ионное и сокращённое уравнение реакций, протекающих до конца
|
|
|
© helpiks.su При использовании или копировании материалов прямая ссылка на сайт обязательна.
|