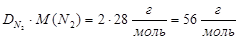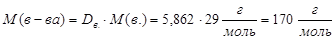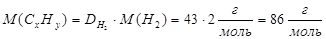- Автоматизация
- Антропология
- Археология
- Архитектура
- Биология
- Ботаника
- Бухгалтерия
- Военная наука
- Генетика
- География
- Геология
- Демография
- Деревообработка
- Журналистика
- Зоология
- Изобретательство
- Информатика
- Искусство
- История
- Кинематография
- Компьютеризация
- Косметика
- Кулинария
- Культура
- Лексикология
- Лингвистика
- Литература
- Логика
- Маркетинг
- Математика
- Материаловедение
- Медицина
- Менеджмент
- Металлургия
- Метрология
- Механика
- Музыка
- Науковедение
- Образование
- Охрана Труда
- Педагогика
- Полиграфия
- Политология
- Право
- Предпринимательство
- Приборостроение
- Программирование
- Производство
- Промышленность
- Психология
- Радиосвязь
- Религия
- Риторика
- Социология
- Спорт
- Стандартизация
- Статистика
- Строительство
- Технологии
- Торговля
- Транспорт
- Фармакология
- Физика
- Физиология
- Философия
- Финансы
- Химия
- Хозяйство
- Черчение
- Экология
- Экономика
- Электроника
- Электротехника
- Энергетика
УРОК 13 Химия ОДБ.10. Количество часов – 1. Специальность 08.01.07 «Мастер общестроительных работ». Группа 4МОС
УРОК 13 Химия ОДБ.10
Количество часов – 1
Дата 14.10.2021
Специальность 08.01.07 «Мастер общестроительных работ»
Группа 4МОС
Тема 2. Углеводороды.
Тема урока: Решение задач на вывод формул.
Цель урока: Ознакомить студентов с алгоритмом решения задач по выведению молекулярных формул органических соединений.
Тип урока: Усвоение новых знаний.
Ход урока.
Алгоритм решения на примере решения задач.
При сгорании неизвестного газообразного углеводорода массой 10,8 г образовался углекислый газ массой 33 г. Определите молекулярную формулу углеводорода, если его плотность при нормальных условиях составляет 3,21 г/дм3.
Дано: Решение:
| m(УВ) = 10,8 г m(CO2) = 33 г ρ(УВ) = 3,21 г/дм3 | М(СО2) = 44 г/моль; ν(СО2) = m(CO2)/M(CO2) = 33 г/44 г/моль = 0,75 моль ν(C) = ν(CO2) = 0,75 моль М(УВ) = ρ(УВ)∙Vm = 3,21 г/дм3∙22,4 дм3/моль = 72 г/моль ν(УВ) = m(УВ)/M(УВ) = 10,8 г/72 г/моль = 0,15 моль Определяем количество атомов углерода: n(C) = ν(С)/ν(УВ) = 0,75 моль/0,15 моль = 5 | |
| Молекулярная формула - ? |
Находим массы углерода и водорода и количество атомов водорода:
m(C) = n(C)∙Mr(C) = 5∙12 = 60 г
m(H) = m(УВ) – m(C) = 72 г – 60 г = 12 г
ν(Н) = m(H)/M(H) = 12 г/1 г/моль = 12 моль
Молекулярная формула С5Н12
Ответ: С5Н12
Определите молекулярную формулу углеводорода, если массовая доля углерода равна 85,75, а водорода –14,3%. Относительная плотность этого вещества по азоту примерно равна 2.
Дано: Решение:
ω(С) = 85,75% или 0,8575
ω(Н) = 14,3% или 0,143
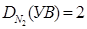
| Находим молярную массу углеводорода: M(N2) = 28 г/моль М(УВ) = |
| Молекулярная формула - ? |
Находим массы и количество атомов углерода и водорода, для расчета примем количество углеводорода за 1 моль:
г
Соотношение атомов С:Н = 4:8
Формула углеводорода С4Н8
Ответ: С4Н8
При сгорании вещества массой 4,25 г образовались углекислый газ массой 13,2 г и воды массой 5,85 г. Плотность паров вещества по воздуху равна 5,862. Определите формулу вещества.
Дано: Решение:
m(в-ва) = 4,25 г
m(CO2) = 13,2 г
m(H2O) = 5,85 г
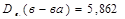
| Находим молярную массу вещества: M(в.) = 29 г/моль
|
| Молекулярная формула - ? |
Для расчета примем количество в-ва за 1 моль, тогда:
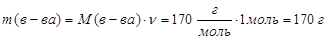
Так как при сгорании в-ва образуется углекислый газ и вода, значит, что в состав данного в-ва входят атомы углерода, водорода и возможно, кислорода. Находим массу и количество атомов, входящих в состав вещества.
М(СО2) =
ν(С) = ν(СО2) = m(CO2)/M(CO2) =
m(C) = ν(C)∙M(C) =
М(Н2О) =
ν(Н) = 2ν(Н2О) =
m(H) = ν(H)∙M(H) = 0,65 моль∙1 г/моль = 0,65 г
m(O) = m(в-ва) – m(C) – m(H) = 4,25 г – 3,6 г – 0,65 г = 0 г, следовательно, в данном веществе отсутствуют атомы кислорода.
Находим отношение атомов углерода и водорода: С:Н = 0,3:0,65 = 6:13
Простейшая формула: С6Н13
Находим молярную массу вещества по простейшей формуле М(С6Н13) = 85 г/моль
Находим, во сколько раз необходимо увеличить индексы: n=M(в-ва)/М(С6Н13) = 170 г/моль/85 г/моль = 2
Следовательно, формула данного вещества С12Н26
Ответ: С12Н26
При сжигании 4,3г углеводорода образовалось 13,2 г СО2. Относительная плотность паров этого вещества по водороду 43. Определите молекулярную формулу.
Дано: Решение.
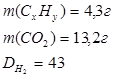
| Находим молярную массу вещества углеводорода:
Находим кол-во углерода и его массу: ν(СО2) = m(CO2)/M(CO2) = 13,2 г/44 г/моль = 0,3 моль Следовательно, ν(С)=ν(СО2); ν(С) = 0,3 моль |
| Молекулярная формула - ? |
m(C) = ν(C)∙M(C) = 0,3 моль∙12 г/моль = 3,6 г
Находим массу атомов водорода и их хим. количество:
m(H) = m(CxHy)-m(C) = 4,3 г – 3,6 г = 0,7 г; ν(Н) = m(H)/M(H) = 0,7 г/1 г/моль = 0,7 моль
Находим отношение атомов углерода и водорода:
С:Н = 0,3:0,7 = 3:7
Простейшая формула С3Н7
Молярная масса углеводорода по простейшей формуле: М(С3Н7) = 43 г/моль
Находим множитель индексов 86:43 = 2, удваиваем индексы простейшей формулы: С6Н14
Истинная формула – С6Н14
Ответ: С6Н14
Домашнее задание. Переписать в рабочую тетрадь, решить задачи на оценку 5 – 3 задачи, на «4» - 2 задачи и на «3» - 1 задачу (любые из пяти):
Задача 1. При сжигании 0.46 г органического вещества было получено 0.88 г оксида углерода (IV) и 0.54 г воды. Плотность паров вещества по водороду равна 23. Определите его молекулярную формулу. (Ответ: С2Н6О).
Задача 2. При сгорании органического вещества массой 2,3 г образовались оксид углерода (IV) объемом 2,24 л и вода массой 2,7 г. Относительная плотность паров этого вещества по воздуху равна 1, 59. Определите его молекулярную формулу. (Ответ: С2Н6О).
Задача 3. При сжигании 1,8 г органического вещества образовалось 2, 016 л оксида углерода (IV) (н.у.) и 2,16 г водяных паров. Напишите структурные формулы и названия всех возможных изомеров этого вещества, если известно. Что 1 л его паров при нормальных условиях имеет массу 2, 679 г (Ответ: С3Н7О).
Задача 4. Выведите формулу вещества, содержащего 52% углерода, кислорода – 35% и 13% водорода. Относительная плотность паров этого вещества по водороду равна 23. (Ответ: С2Н6О).
Задача 5. При сгорании органического вещества массой 13,8 г образовались оксид углерода (IV) объемом 13,44 л и вода массой 16,2 г. Плотность этого вещества равна 2,054 г/мл. Определите его молекулярную формулу. (Ответ: С2Н6О).
|
|
|
© helpiks.su При использовании или копировании материалов прямая ссылка на сайт обязательна.
|