
- Автоматизация
- Антропология
- Археология
- Архитектура
- Биология
- Ботаника
- Бухгалтерия
- Военная наука
- Генетика
- География
- Геология
- Демография
- Деревообработка
- Журналистика
- Зоология
- Изобретательство
- Информатика
- Искусство
- История
- Кинематография
- Компьютеризация
- Косметика
- Кулинария
- Культура
- Лексикология
- Лингвистика
- Литература
- Логика
- Маркетинг
- Математика
- Материаловедение
- Медицина
- Менеджмент
- Металлургия
- Метрология
- Механика
- Музыка
- Науковедение
- Образование
- Охрана Труда
- Педагогика
- Полиграфия
- Политология
- Право
- Предпринимательство
- Приборостроение
- Программирование
- Производство
- Промышленность
- Психология
- Радиосвязь
- Религия
- Риторика
- Социология
- Спорт
- Стандартизация
- Статистика
- Строительство
- Технологии
- Торговля
- Транспорт
- Фармакология
- Физика
- Физиология
- Философия
- Финансы
- Химия
- Хозяйство
- Черчение
- Экология
- Экономика
- Электроника
- Электротехника
- Энергетика
Решение задач на нахождение формулы
Решение задач на нахождение формулы
Нахождение формулы углеводорода по массовым долям элементов и относительной плотности.
Алгоритм решения задачи
1. Вычисляем молярную массу вещества: М(в) = D(x) · М(х) (1)
2. Вычисляем количество атомов элемента:
| а) если w дана в процентах: | n(Э) = | 
| (2) |
| б) если w дана в долях: | n(Э) = | 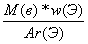
| (3) |
4. Записываем формулу вещества (СаНb), используя количество атомов, найденное в действии (2).
3. Вычисляем молярную массу полученного вещества (СaНb).
4. Если молярная масса полученного вещества (СaНb) отличается от молярной массы, найденной по относительной плотности вещества (1), необходимо разделить молярную массу (1) на молярную массу (СaНb).
5. На полученное целое число умножаем все индексы (СaНb) – это и есть данное вещество.
Пример. Выведите формулу вещества, содержащего 82,75% углерода и 17,25 % водорода. Относительная плотность паров этого вещества по воздуху равна 2.
| Дано: w(C) = 82,75% w(H) = 17,25% D(возд) = 2 | Решение: M(воздуха) = 29г/моль М(СхНу) = 29г/моль · 2 = 58г/моль 1. Применяем формулу (1): M(в-ва) = 29 г/моль · 2 =58 г/моль. |
| Найти: СхНу |
2. Находим количество атомов С и Н по формуле (2)
| n(С) = | 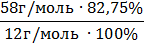
| = 4 | n(Н) = | 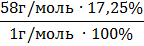
| =10 |
3. Вычисляем молярную массу С4Н10:
М(С4Н10) = 12 · 4 + 1 · 10 = 58г/моль
4. Вычисленная молярная масса совпадает с (1), формула вещества С4Н10.
Ответ: С4Н10
Задача для самостоятельного решения. Найдите молекулярную формулу углеводорода, содержание углерода в котором 80%, а водорода – 20%, относительная плотность по водороду равна 15 (С2Н6). РЕШИТЬ
|
|
|
© helpiks.su При использовании или копировании материалов прямая ссылка на сайт обязательна.
|