
- Автоматизация
- Антропология
- Археология
- Архитектура
- Биология
- Ботаника
- Бухгалтерия
- Военная наука
- Генетика
- География
- Геология
- Демография
- Деревообработка
- Журналистика
- Зоология
- Изобретательство
- Информатика
- Искусство
- История
- Кинематография
- Компьютеризация
- Косметика
- Кулинария
- Культура
- Лексикология
- Лингвистика
- Литература
- Логика
- Маркетинг
- Математика
- Материаловедение
- Медицина
- Менеджмент
- Металлургия
- Метрология
- Механика
- Музыка
- Науковедение
- Образование
- Охрана Труда
- Педагогика
- Полиграфия
- Политология
- Право
- Предпринимательство
- Приборостроение
- Программирование
- Производство
- Промышленность
- Психология
- Радиосвязь
- Религия
- Риторика
- Социология
- Спорт
- Стандартизация
- Статистика
- Строительство
- Технологии
- Торговля
- Транспорт
- Фармакология
- Физика
- Физиология
- Философия
- Финансы
- Химия
- Хозяйство
- Черчение
- Экология
- Экономика
- Электроника
- Электротехника
- Энергетика
Механизм реакции


495. Рассмотрите механизм ацилирования трет-бутилбензола хлорангидридом пропионовой кислоты CH3CH2C(O)Cl по Фриделю-Крафтсу, укажите медленную стадию, рассмотрите строение s-комплекса. Напишите реакцию образования электрофила.
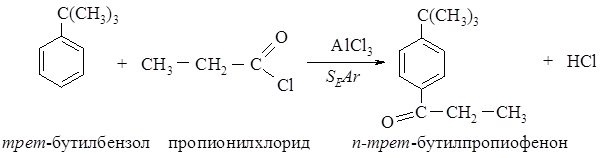
Механизм реакции
Уравнение реакции образование ацилий-катиона – электрофила
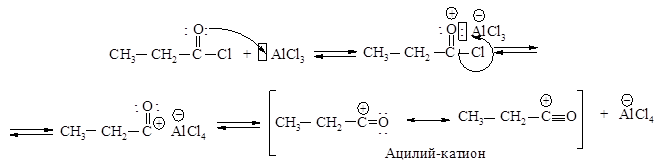
1 стадия – медленная:
Положительно заряженный ацилий-катион – электрофильный реагент или электрофил - атакует доступное p - электронное облако трет-бутилбензола, вытягивая из него пару электронов. За счет этой пары электронов и происходит присоединение атома углерода к атому углерода с образованием s - связи углерод-углерод. Атакуемый атом углерода переходит из sp2- гибридного состояния в sp3- гибридное состояние. При этом возникает карбокатион, называемый также s-комплексом.
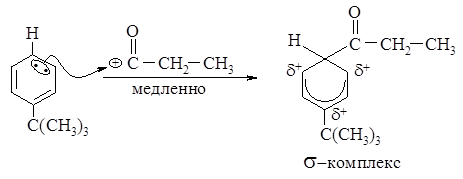
Строение s-комплекса
Четыре p - электрона распределены между пятью атомами углерода,
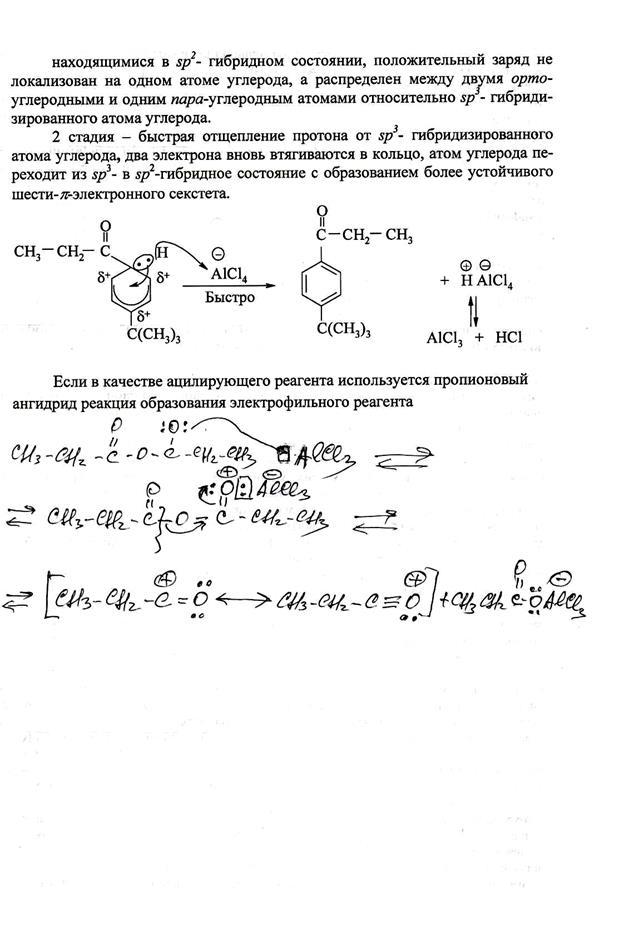
391. Рассмотрите механизм реакции нитрования этилбензола, укажите медленную стадию, рассмотрите строение s-комплекса. Напишите реакцию образования электрофила.
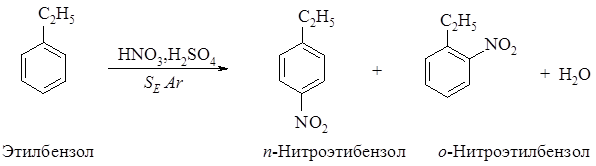
Механизм реакции:
Образование электрофильного реагента - нитроний-катиона NO2 +
Нитрование проводится нитрующей смесью - смесью азотной и серной кислот. Образование электрофильной реагента - нитроний-катиона NO2 + - происходит в реакции между азотной и серной кислотами. Протонированная азотная кислота распадается с образованием нитроний-катиона и молекулы воды.
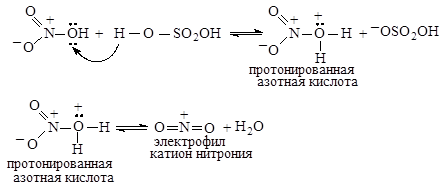
1 стадия – медленная, электрофил - атакует доступное p - электронное облако толуола, вытягивая из него пару электронов. За счет этой пары электронов и происходит присоединение атома азота к атому углерода с образованием s - связи углерод-азот. Атакуемый атом углерода переходит из sp2- гибридного состояния в sp3- гибридное состояние. При этом возникает карбокатион, называемый также s-комплексом.
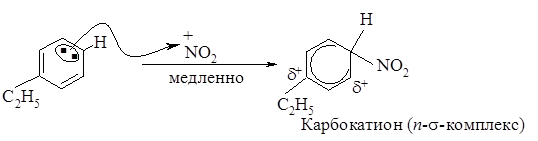
Строение s-комплекса:
Четыре p - электрона распределены между пятью атомами углерода, находящимися в sp2- гибридном состоянии, положительный заряд не локализован на одном атоме углерода, а распределен между двумя орто-углеродными и одним пара-углеродным атомами относительно sp3- гибридизованного атома углерода.
2 стадия – быстрая, отщепление протона от sp3- гибридизованного атома углерода сопряженным анионом электрофила HO3SО¯,два электрона вновь втягиваются в кольцо, атом углерода переходит из sp3- в sp2-гибридное состояние с образованием более устойчивого шести p-электронного секстета.
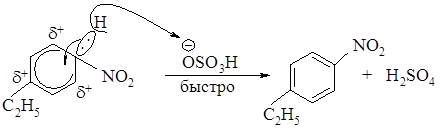
Для о-изомера механизм реакции аналогичен
398. Рассмотрите механизм сульфирования анизола C6H5-O-CH3, укажите медленную стадию, рассмотрите строение s-комплекса. Напишите реакцию образования электрофила.
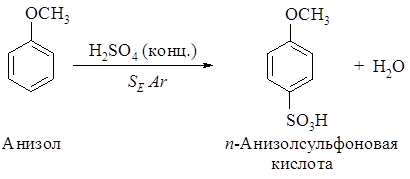
Механизм реакции
Стадия образования электрофильного реагента:
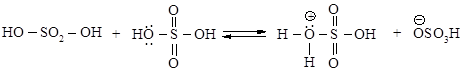
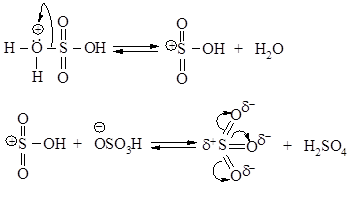
1 стадия – медленная: электрофил - атакует доступное p - электронное облако анизола, вытягивая из него пару электронов. За счет этой пары электронов и происходит присоединение атома серы к атому углерода с образованием s - связи углерод-сера. Атакуемый атом углерода переходит из sp2- в sp3- гибридное состояние. При этом возникает карбокатион, называемый также s-комплексом.
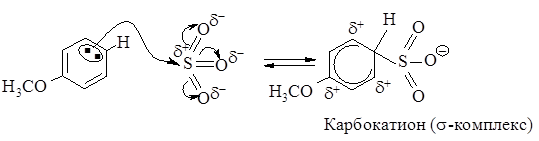
Строение s-комплекса
Четыре p - электрона распределены между пятью атомами углерода, находящимися в sp2- гибридном состоянии, положительный заряд не локализован на одном атоме углерода, а распределен между двумя орто-углеродными и одним пара-углеродным атомами относительно sp3- гибридизованного атома углерода. Распределение положительного заряда между несколькими атомами углерода делает карбокатион более устойчивым, именно благодаря такой стабилизации возможно образование карбокатиона из очень устойчивой молекулы бензола.
2 стадия – быстрая отщепление протона от sp3- гибридизированного атома углерода,два электрона вновь втягиваются в кольцо, атом углерода переходит из sp3- в sp2-гибридное состояние с образованием более устойчивого шести p-электронного секстета.
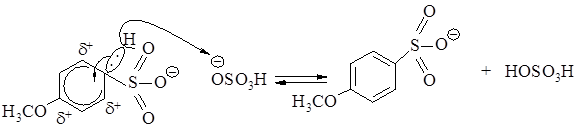
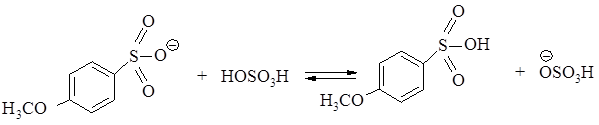
399. Рассмотрите механизм бромирования бензола, укажите медленную стадию, рассмотрите строение s-комплекса. Напишите реакцию образования электрофила.
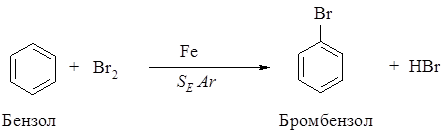
Механизм реакции
Стадия образования электрофильного реагента:
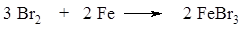
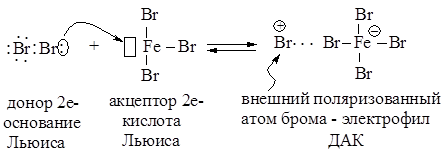
1 стадия - медленная
Электрофил - атакует доступное p - электронное облако бензола, вытягивая из него пару электронов. За счет этой пары электронов и происходит присоединение атома брома к атому углерода с образованием s - связи углерод – бром. Атакуемый атом углерода переходит из sp2- в sp3- гибридное состояние. При этом возникает карбокатион, называемый также s-комплексом.
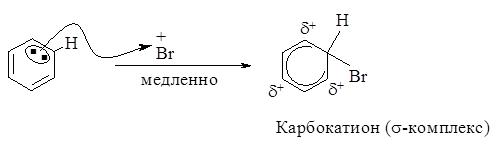
Четыре p - электрона распределены между пятью атомами углерода, находящимися в sp2- гибридном состоянии, положительный заряд не локализован на одном атоме углерода, а распределен между двумя орто-углеродными и одним пара-углеродным атомами относительно sp3- гибридизированного атома углерода.
2 стадия – быстрая отщепление протона от sp3- гибридизованного атома углерода сопряженным анионом электрофила FeBr4¯,два электрона вновь втягиваются в кольцо, атом углерода переходит из sp3- в sp2-гибридное состояние с образованием более устойчивого шести p-электронного секстета.
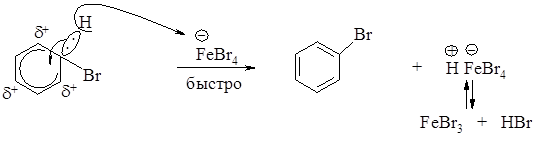
В случае рекции хлорирования механизм аналогичен только в тексте и в рекции образования электрофильно частицы заменить бром на хлор. Другие галогены с бензолом не взаимодействуют только хлор или бром.
Рассмотрите механизм алкилирования бензола хлористым пропилом, укажите медленную стадию, рассмотрите строение s-комплекса. Напишите реакцию образования электрофила.
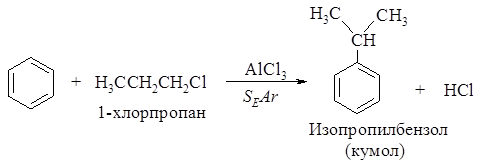
Механизм реакции
Стадия образования электрофильного реагента:
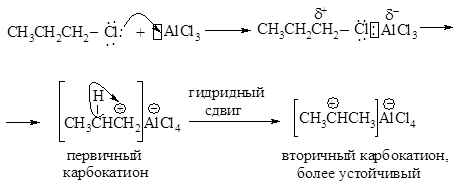
1 стадия - медленная
Электрофил - атакует доступное p - электронное облако бензола, вытягивая из него пару электронов. За счет этой пары электронов и происходит присоединение атома углерода к атому углерода с образованием s - связи углерод- углерод. Атакуемый атом углерода переходит из sp2- в sp3- гибридное состояние. При этом возникает карбокатион, называемый также s-комплексом.
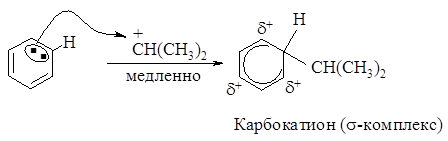
Четыре p - электрона распределены между пятью атомами углерода, находящимися в sp2- гибридном состоянии, положительный заряд не локализован на одном атоме углерода, а распределен между двумя орто-углеродными и одним пара-углеродным атомами относительно sp3- гибридизированного атома углерода. Распределение положительного заряда между несколькими атомами углерода делает карбокатион более устойчивым, именно благодаря такой стабилизации возможно образование карбокатиона из очень устойчивой молекулы бензола.
2 стадия – быстрая отщепление протона от sp3- гибридизованного атома углерода сопряженным анионом электрофила ‒AlCl4,два электрона вновь втягиваются в кольцо, атом углерода переходит из sp3- в sp2-гибридное состояние с образованием более устойчивого шести p-электронного секстета.
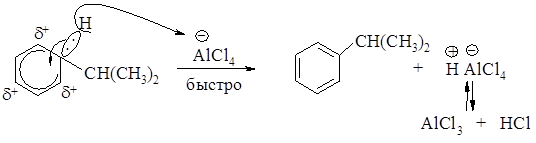
Если в качестве алкилирующих реагентов используются алкен или спирт, в качестве катализатора используется минеральная кислота образование электрофилов протекает по схеме:
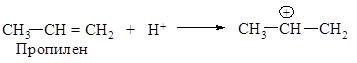
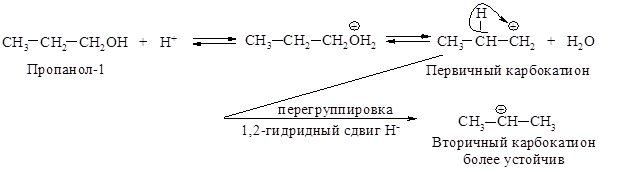
Результат реакции будет аналогичен.
540. Расположите соединения в порядке увеличения реакционной способности в реакции бромирования (механизм SEAr):
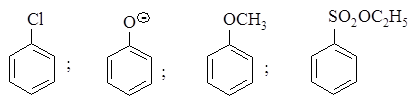
Укажите электронные эффекты ориентантов. Напишите уравнения реакций.
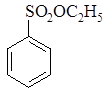
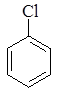
| < 
| < 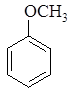
| < 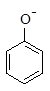
|
| Электроноакцепторная группа, сильно дезактивирующие кольцо, -I, -M | Электроноакцепторная группа, слабо дезактивирующие кольцо, -I > +М | Электронодонорная группа, умеренно активирующие кольцо, +М > -I | Электронодонорная группа, сильно активирующие кольцо, + I, +М |
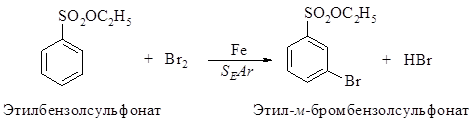
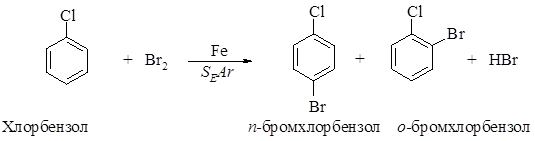
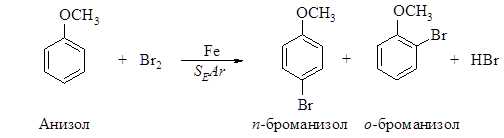
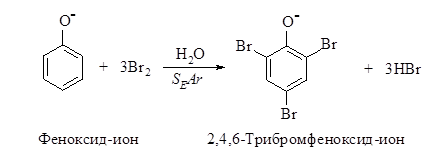
585. Рассмотрите механизм ориентирующего влияния метильной группы -CH3 в реакции сульфирования толуола (механизм SEAr).
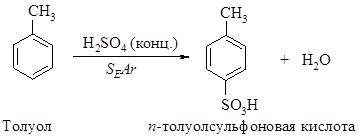
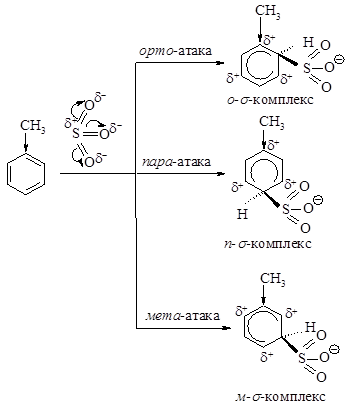
В о- и п-s-комплексах электронодонорная группа – СН3 связана с атомом углерода, несущим положительный заряд. Она подает электроны в кольцо, величина положительного заряда на атоме углерода, связанному с этой группой уменьшается, степень распределения заряда увеличивается, устойчивость s-комплексов возрастает.
В м-s-комплексе эта группа не связана с атомом углерода, несущим положительный заряд, поэтому она не принимает участия в распределении заряда и поэтому заряд в этом s-комплексе будет распределен в меньшей степени. Следовательно этот s-комплекс будет образовываться медленно и он будет неустойчив и поэтому основными продуктами реакции будут продукты реакции о- п-замещения.
574. Рассмотрите механизм ориентирующего влияния нитрогруппы -NO2 в реакции сульфирования нитробензола (механизм SEAr).
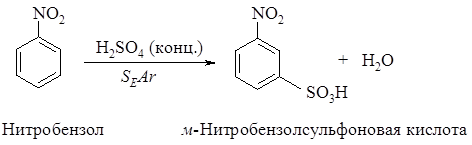

В о- и п-s-комплексах электроноакцепторная группа – NO2 связана с атомом углерода, несущим положительный заряд. Она оттягивает электроны на себя, величина положительного заряда на атоме углерода, связанному с этой группой увеличивается, степень распределения заряда уменьшается, устойчивость s-комплексов уменьшается. Следовательно эти s-комплексы будет образовываться медленно и они будут неустойчивы.
В м-s-комплексе эта группа не связана с атомом углерода, несущим положительный заряд, поэтому она не принимает участия в распределении заряда и поэтому заряд в этом s-комплексе будет распределен в большей степени. Следовательно этот s-комплекс будет образовываться быстро и он будет устойчив и поэтому основным продуктом реакции будет продукт реакции м-замещения.
630. Рассмотрите механизм реакции и совместное влияние двух групп на изомерный состав продуктов в следующих реакциях:
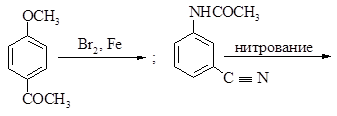
Дайте названия исходным соединениям и продуктам реакции. Укажите согласованную и несогласованную ориентацию.
а)
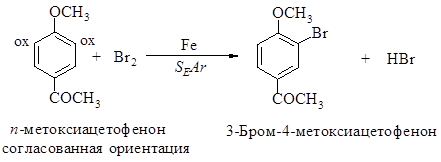
б)
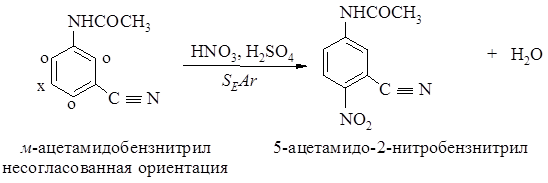
NHCOCH3 – электронодонорная группа умеренно активирующая кольцо
СºN - электроноакцепторная группа, сильно дезактивирующая кольцо
Преимущественное направление атаки определяет электронодонорный заместитель.

|
|
|
© helpiks.su При использовании или копировании материалов прямая ссылка на сайт обязательна.
|