
- Автоматизация
- Антропология
- Археология
- Архитектура
- Биология
- Ботаника
- Бухгалтерия
- Военная наука
- Генетика
- География
- Геология
- Демография
- Деревообработка
- Журналистика
- Зоология
- Изобретательство
- Информатика
- Искусство
- История
- Кинематография
- Компьютеризация
- Косметика
- Кулинария
- Культура
- Лексикология
- Лингвистика
- Литература
- Логика
- Маркетинг
- Математика
- Материаловедение
- Медицина
- Менеджмент
- Металлургия
- Метрология
- Механика
- Музыка
- Науковедение
- Образование
- Охрана Труда
- Педагогика
- Полиграфия
- Политология
- Право
- Предпринимательство
- Приборостроение
- Программирование
- Производство
- Промышленность
- Психология
- Радиосвязь
- Религия
- Риторика
- Социология
- Спорт
- Стандартизация
- Статистика
- Строительство
- Технологии
- Торговля
- Транспорт
- Фармакология
- Физика
- Физиология
- Философия
- Финансы
- Химия
- Хозяйство
- Черчение
- Экология
- Экономика
- Электроника
- Электротехника
- Энергетика
Задания Д24 № 122. Решение.. Задания Д24 № 208
2. Задания Д24 № 122
Равновесие  смещается в сторону исходных веществ при
смещается в сторону исходных веществ при
1) уменьшении давления
2) нагревании
3) введении катализатора
4) добавлении водорода
Решение.
Принцип Ле Шателье — если на систему, находящуюся в равновесии, воздействовать извне, изменяя какое-либо из условий равновесия (температура, давление, концентрация), то в системе усиливаются процессы, направленные на компенсацию внешнего воздействия.
Понижение давление (внешнее воздействие) приведет к усилению процессов увеличивающих давление, значит, равновесие сместится в сторону большего количества газообразных частиц (которые и создают давление), т.е. в сторону продуктов реакции.
При повышении температуры (внешнее воздействие) система будет стремиться понизить температуру, значит, усиливается процесс поглощающий тепло. равновесие сместится в сторону эндотермической реакции, т.е. в сторону продуктов реакции.
Катализатор не влияет на смещение равновесия
Добавление водорода (внешнее воздействие) приведет к усилению процессов расходующих водород, т.е. равновесие сместится в сторону исходных веществ
Ответ: 4
Источник: Яндекс: Тренировочная работа ЕГЭ по химии. Вариант 2.
Раздел кодификатора ФИПИ: 1.4.4 Смещение химического равновесия под действием различных факторов
3. Задания Д24 № 208
В системе
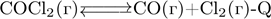
смещению химического равновесия вправо будет способствовать
1) уменьшение температуры
2) увеличение концентрации оксида углерода (II)
3) увеличение давления
4) уменьшение концентрации хлора
|
|
|
© helpiks.su При использовании или копировании материалов прямая ссылка на сайт обязательна.
|