
- Автоматизация
- Антропология
- Археология
- Архитектура
- Биология
- Ботаника
- Бухгалтерия
- Военная наука
- Генетика
- География
- Геология
- Демография
- Деревообработка
- Журналистика
- Зоология
- Изобретательство
- Информатика
- Искусство
- История
- Кинематография
- Компьютеризация
- Косметика
- Кулинария
- Культура
- Лексикология
- Лингвистика
- Литература
- Логика
- Маркетинг
- Математика
- Материаловедение
- Медицина
- Менеджмент
- Металлургия
- Метрология
- Механика
- Музыка
- Науковедение
- Образование
- Охрана Труда
- Педагогика
- Полиграфия
- Политология
- Право
- Предпринимательство
- Приборостроение
- Программирование
- Производство
- Промышленность
- Психология
- Радиосвязь
- Религия
- Риторика
- Социология
- Спорт
- Стандартизация
- Статистика
- Строительство
- Технологии
- Торговля
- Транспорт
- Фармакология
- Физика
- Физиология
- Философия
- Финансы
- Химия
- Хозяйство
- Черчение
- Экология
- Экономика
- Электроника
- Электротехника
- Энергетика
Электрохимия
Электрохимия
13. Назовите виды электродов согласно классификации электродов?
Ответ: Классификация электродов: электроды первого рода, электроды второго рода, окислительно-восстановительные электроды, газовые электроды.
Электроды первого рода. Такие электроды обратимы относительно катиона, а величина их электродного потенциала при прочих равных условиях определяется активностью (концентрацией) ионов металла в растворе. В общем случае в электроде первого рода 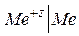 устанавливается электрохимическое равновесие
устанавливается электрохимическое равновесие
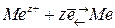
Электроды второго рода. К этому классу относятся электроды, потенциал которых определяется активностью анионов в растворе. Из таких электродов в электрохимических измерениях наиболее часто используются хлорсеребряный  и каломельный
и каломельный 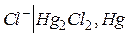 электроды.
электроды.
В каломельном электроде реализуется равновесие
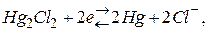 (3)
(3)
Потенциал такого электрода зависит от температуры и активности (концентрации) хлорид-ионов по уравнению
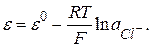 (4)
(4)
Простота конструкции и хорошая воспроизводимость электродных потенциалов обусловили широкое использование хлорсеребряного и каломельного электродов в качестве электродов сравнения.
Окислительно-восстановительные электроды. Редокс-электрод - это инертный металл (Pt), погруженный в раствор, содержащий разновалентные ионы одного и того же металла, например, Fe+3 и Fe+2, Sn+2 и Sn+4.
В электроде Fe+2, Fe+3|Pt реализуется равновесие
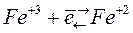
Электродный потенциал такого электрода
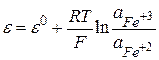 .
.
Газовые электроды. Газовые электроды в отличие от электродов первого и второго рода состоят из инертного металла, к поверхности которого подводится электрохимически активный газ. Например, в водородном электроде 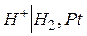 протекает реакция
протекает реакция

Таким образом, электродный потенциал газового электрода зависит не только от состава электролита, но и давления газа.
14. Как найти ЭДС гальванического элемента, зная значения электродных потенциалов?
Ответ:
15. Связь каких двух относительных величин показывает электрохимическое уравнение нернста( при условиях постоянной температуры)?
Ответ:
16. Что такое потенциалобразующая химическая реакция гальванического элемента?
Ответ:
17. Какого условие самопроизвольного протекания электрохимической реакции выраженное через эдс гальванического элемента?
Ответ:
18. как определить константу равновесия электрохимической реакции зная значения стандартных потенциалов электродов гальванического элемента?
Ответ:  ???
???
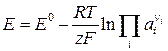
|
|
|
© helpiks.su При использовании или копировании материалов прямая ссылка на сайт обязательна.
|