
- Автоматизация
- Антропология
- Археология
- Архитектура
- Биология
- Ботаника
- Бухгалтерия
- Военная наука
- Генетика
- География
- Геология
- Демография
- Деревообработка
- Журналистика
- Зоология
- Изобретательство
- Информатика
- Искусство
- История
- Кинематография
- Компьютеризация
- Косметика
- Кулинария
- Культура
- Лексикология
- Лингвистика
- Литература
- Логика
- Маркетинг
- Математика
- Материаловедение
- Медицина
- Менеджмент
- Металлургия
- Метрология
- Механика
- Музыка
- Науковедение
- Образование
- Охрана Труда
- Педагогика
- Полиграфия
- Политология
- Право
- Предпринимательство
- Приборостроение
- Программирование
- Производство
- Промышленность
- Психология
- Радиосвязь
- Религия
- Риторика
- Социология
- Спорт
- Стандартизация
- Статистика
- Строительство
- Технологии
- Торговля
- Транспорт
- Фармакология
- Физика
- Физиология
- Философия
- Финансы
- Химия
- Хозяйство
- Черчение
- Экология
- Экономика
- Электроника
- Электротехника
- Энергетика
УГЛЕВОДЫ.
УГЛЕВОДЫ.
Углеводами называют полиоксиальдегиды или полиоксикетоны или соединения, превращающиеся в них при гидролизе. Углевод, который нельзя превратить гидролизом в более простое соединение, называется моносахаридом. Углевод, при гидролизе которого образуется большое число молекул моносахарида, называется полисахаридом.
Класс углеводов включает широко распространенные в природе соединения, одни из которых растворимы в воде и сладкие на вкус, называемые сахарами и другие, родственные им по химическому строению, но более сложные не имеющие сладкого вкуса, такие как крахмал и клетчатка.
Первые исследования показывали, что состав природных сахаров соответствует общей формуле Сn(H2O)m. Однако позднее были обнаружены соединения, относящиеся к этому классу по физическим и химическим свойствам, но не отвечающие брутто-формуле, предложенной ранее.
Например, дезоксирибоза:
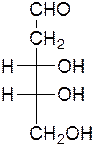 брутто-формула: С5Н10О4.
брутто-формула: С5Н10О4.
Моносахариды- простые углеводы, не подвергающиеся гидролизу. Наиболее важны и чаще всего встречаются в природе монозы состава С5Н10О5. Исследования показали, что строение таких соединений отвечает неразветвленной цепи углеродов, имеющих одну карбонильную группу (альдегидную или кетонную) и несколько гидроксильных групп, то есть соединения относятся к классу оксикарбонильных.
В зависимости от количества углеродных атомов в цепи монозы называют С5 – пентозы, С4 –тетрозы, С6 –гексозы. Моносахариды могут существовать в виде нескольких изомерных форм. Так в кристаллическом виде монозы утрачивают оксикарбонильное и приобретают внутреннее циклическое полуацетальное строение. Только в растворах возможны частичные переходы циклических форм в открытые оксикарбонильные. Таким образом, для моносахаридов характерно явление таутомерии или равновесной изомерии.
Моносахариды, содержащие в оксикарбонильной форме альдегидную группу называют альдозами,а кетонную группу - кетозами.
Изомерия моносахаридов связана с положением карбонильной группы и наличием асимметрических атомов углерода.
В кетозах карбонильная группа обычно находится у второго атома углерода.
При одинаковом количестве атомов углерода альдозы и кетозы изомерны друг другу.
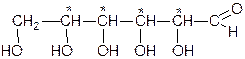
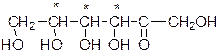
альдогексоза кетогексоза
В альдогексозе 4 асимметрических углерода, 24=16 оптических изомеров, в кетогексозе 3 асимметрических атома углерода и 23=* оптических изомеров.
Пространственное изображение моноз выражают с помощью проекционных формул Фишера.
Таутомерные превращения D-глюкозы:
гликозидный гликозидный
 гидроксил гидроксил
гидроксил гидроксил
 |



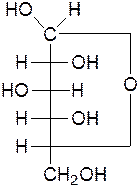
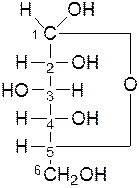
β-D-глюкопираноза α-D-глюкопираноза

 гликозидный
гликозидный 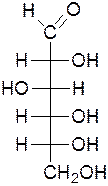 гликозидный
гликозидный
гидроксил D-глюкоза гидроксил
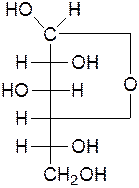
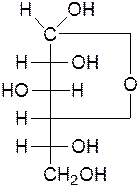
β-D-глюкофураноза α-D-глюкофураноза
α- и β-изомеры называют аномерами.
Явление мутаротации - процесс растворения моносахаридов в воде, сопровождающийся изменением угла вращения плоско поляризованного луча света до некоторой постоянной величины. Для свежеприготовленного раствора D-глюкозы угол вращения +110,1˚, равновесный угол +52,5˚.
Перспективные формулы Хеуорсачаще используются для изображения циклических форм моно- и полисахаридов, так как показывают расположение реакционноспособных групп относительно плоскости цикла Правила перехода от формул Толенса к перспективным формулам Хеуорса следующие: атомы углерода располагают по вершинам правильного шестиугольника согласно указанной нумерации, заместители у атомов углерода располагаются по вертикали, причем те заместители, что в формуле Толенса находились слева – в формуле Хеуорса пишут вверху; а те, что были справа в формуле Толенса – в формуле Хеуорса пишут внизу.
Гликозидный гидроксил находится у первого атома углерода, для α-формы характерно нижнее его расположение, для β-формы – верхнее.
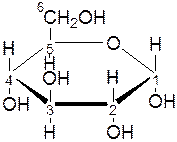
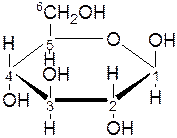
α-D-глюкопираноза β-D-глюкопираноза
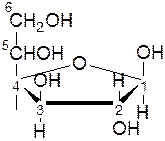 β-D-глюкофураноза
β-D-глюкофураноза
Физические свойства моносахаридов. Это бесцветные твердые вещества. Хорошо растворимы в воде и труднее в спирте. Растворы сладкие на вкус.
Химические свойства.Реакции, протекающие в растворе, могут происходить с участием разных таутомерных форм. Равновесие непрерывно будет сдвигаться в сторону образования той формы, которая вступает в реакцию, до полного исчерпывания моносахарида.
1.Реакции в цепной оксикарбонильной (открытой) форме, это реакции на карбонильную группу:
1.1. Окисление («реакция серебряного зеркала»)
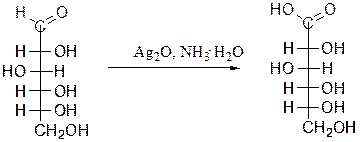
D-глюкоза глюконовая кислота
1.2. Восстановление
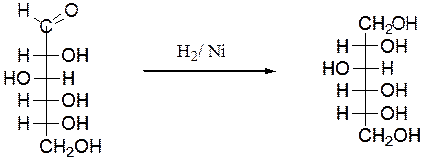
D-глюкоза сорбит
1.3. Взаимодействие с синильной кислотой:

D-глюкоза оксинитрил
1. Реакции в циклической полуацетальной форме (реакции по гидроксильным группам, среди которых наибольшей активностью обладает гликозидный гидроксил)
1.1. Реакция на гликозидный гидроксил
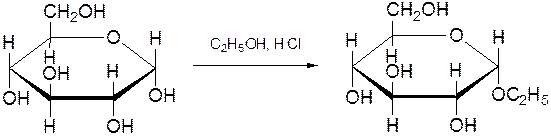
α-D-глюкопираноза этил-α-D-глюкопиранозид
3.2. Алкилирование:
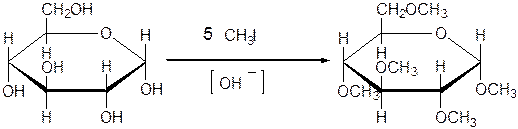
пентаметил-α-D-глюкопираноза
3.3. Ацилирование:

пентаацетил-α-D-глюкопираноза.
|
|
|
© helpiks.su При использовании или копировании материалов прямая ссылка на сайт обязательна.
|