
- Автоматизация
- Антропология
- Археология
- Архитектура
- Биология
- Ботаника
- Бухгалтерия
- Военная наука
- Генетика
- География
- Геология
- Демография
- Деревообработка
- Журналистика
- Зоология
- Изобретательство
- Информатика
- Искусство
- История
- Кинематография
- Компьютеризация
- Косметика
- Кулинария
- Культура
- Лексикология
- Лингвистика
- Литература
- Логика
- Маркетинг
- Математика
- Материаловедение
- Медицина
- Менеджмент
- Металлургия
- Метрология
- Механика
- Музыка
- Науковедение
- Образование
- Охрана Труда
- Педагогика
- Полиграфия
- Политология
- Право
- Предпринимательство
- Приборостроение
- Программирование
- Производство
- Промышленность
- Психология
- Радиосвязь
- Религия
- Риторика
- Социология
- Спорт
- Стандартизация
- Статистика
- Строительство
- Технологии
- Торговля
- Транспорт
- Фармакология
- Физика
- Физиология
- Философия
- Финансы
- Химия
- Хозяйство
- Черчение
- Экология
- Экономика
- Электроника
- Электротехника
- Энергетика
Руководителю организации (где работаете)
Руководителю организации (где работаете)
От
тел.
ЗАЯВЛЕНИЕ
об отказе от вакцинации и от участия в исследовании вакцин против COVID-19
Сегодня «__»__________202_ года мне предложили сделать прививку от COVID-19.
Я отказываюсь от этого поскольку эффективность и безопасность этой «вакцины» не установлена, ее исследования до сих пор продолжаются, и я не хочу в них участвовать, что является моим конституционным правом.
Уже 10 августа 2020 года Ассоциация организаций по клиническим исследованиям (АОКИ) заявила:
«Особо стоит подчеркнуть высокие риски регистрации препарата до завершения фазы III. Именно в ходе этой фазы получаются основные доказательства эффективности, а также собирается информация о нежелательных реакциях, которые препарат может вызвать у отдельных групп пациентов: лиц с ослабленным иммунитетом, людей, имеющих сопутствующие заболевания и т.п.
Разработчики же прямо заявляют, что хотят в первую очередь прививать в том числе пенсионеров как относящихся к группе риска по COVID-19. Хотя на сегодняшний день нет никаких данных о безопасности этой вакцины для пожилых людей, часто имеющих целый ряд сопутствующих заболеваний и нередко – ослабленный иммунитет».
Несмотря на то, что письмо АОКИ датировано августом, ситуация мало в чем изменилась и в декабре 2020, кроме регистрации не прошедших надлежащих испытаний вакцин, и объявления ими «массовой вакцинации».
Так, третья фаза исследований вакцины «Спутник-V» должна закончиться только к 1 Мая 2021 года.
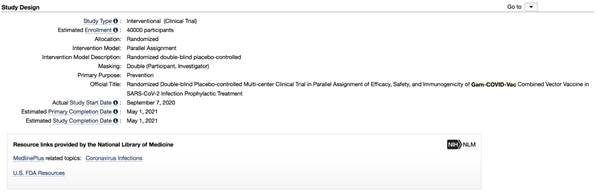
В подтверждение тому, что это – исследование, а не вакцинация, служит такое сообщение в СМИ: "Договоры на страхование 40 тысяч добровольцев уже заключили", - пояснил директор НИЦ имени Гамалеи Александр Гинцбург.
А прививать собираются не 40 тысяч, а миллионы людей.
В отношении вакцины «ЭпиВакКорона» ситуация еще хуже.
Даже в Википедии сказано: Вакцина ещё не прошла III фазу клинических испытаний. Пострегистрационные исследования вакцины «ЭпиВакКорона» начнутся в ноябре-декабре 2020 года и будут продолжаться шесть месяцев после вакцинации последнего участника.
На сайте ClinicalTrials.gov опубликована следующая информация (перевод с английского):
Изучение безопасности, реактогенности и иммуногенности вакцины "ЭпиВакКорона" для профилактики COVID-19 (ЭпиВакКорона)
Фактическая дата начала исследования: 27 Июля 2020 Года
Предполагаемая дата завершения исследования: 28 Сентября 2020 года
Предполагаемая дата завершения исследования: 4 Октября 2020 года
Если добровольцы выбывают из исследования, они не будут заменены.
При этом на этой же странице доступно следующее уведомление:
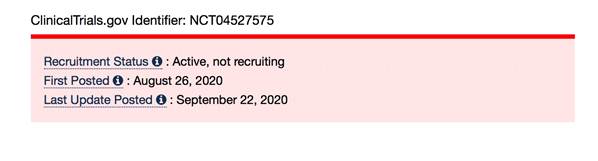
Откуда видно, что последнее обновление на странице было сделано 22 сентября 2020, а, напоминаем, что завершение исследования должно было состоятся 04 октября,но сообщений на указанном сайте о завершении первых двух фаз нет.
На данном сайте нет сообщений о начале третьей фазы исследований. В описании исследования сказано:
Первая фаза клинического исследования-открытое исследование. В исследование будут включены 14 мужчин и женщин в возрасте от 18 до 30 лет включительно, отвечающих критериям включения и не имеющих критериев исключения, данные которых будут использованы для последующего анализа безопасности и иммуногенности.
Вторая фаза клинического исследования-это простое, слепое, плацебо-контролируемое, рандомизированное, параллельное групповое исследование. В исследование будут включены 86 мужчин и женщин в возрасте от 18 до 60 лет включительно, которые соответствуют критериям включения и не имеют критериев исключения, данные которых будут использованы для последующего анализа безопасности и иммуногенности.
Таким образом обе вакцины не исследованы надлежащим образом, и их применение, прежде всего, небезопасно, но может быть и неэффективно.
В пп.4.1.7. Санитарных правил СП 3.3.2.561-96 «Медицинское иммунобиологические препараты. Государственные испытания и регистрация новых медицинских иммунобиологических препаратов» сказано, что государственная регистрация МИБП (включая вакцины) осуществляется на основании результатов всех этапов испытаний препарата, подтверждающих его эффективность, специфическую активность и безопасность, а также при наличии утвержденной нормативно-технической документации.
То есть регистрация этих вакцин прошла с нарушением указанных правил.
На основании изложенного, ст. 21 Конституции РФ (никто не может быть без добровольного согласия подвергнут медицинским, научным или иным опытам) и ч.1 ст. 43 ФЗ РФ № 61 «Об обращении лекарственных средств» я отказываюсь от участия в клиническом исследовании вакцин от COVID-19.
Я так отказываюсь от медицинского вмешательства в форме данной «вакцинации» от COVID-19 на основании:
• ч. 1 ст. 20 ФЗ № 323 от 21.11.2011. «Об основах охраны здоровья граждан в Российской Федерации»;
• пп. 8) ст. 19 ФЗ № 323 от 21.11.2011. «Об основах охраны здоровья граждан в Российской Федерации»;
• ч. 1 ст. 5 ФЗ РФ «Об иммунопрофилактике инфекционных болезней»
Дата. Подпись.
|
|
|
© helpiks.su При использовании или копировании материалов прямая ссылка на сайт обязательна.
|