
- Автоматизация
- Антропология
- Археология
- Архитектура
- Биология
- Ботаника
- Бухгалтерия
- Военная наука
- Генетика
- География
- Геология
- Демография
- Деревообработка
- Журналистика
- Зоология
- Изобретательство
- Информатика
- Искусство
- История
- Кинематография
- Компьютеризация
- Косметика
- Кулинария
- Культура
- Лексикология
- Лингвистика
- Литература
- Логика
- Маркетинг
- Математика
- Материаловедение
- Медицина
- Менеджмент
- Металлургия
- Метрология
- Механика
- Музыка
- Науковедение
- Образование
- Охрана Труда
- Педагогика
- Полиграфия
- Политология
- Право
- Предпринимательство
- Приборостроение
- Программирование
- Производство
- Промышленность
- Психология
- Радиосвязь
- Религия
- Риторика
- Социология
- Спорт
- Стандартизация
- Статистика
- Строительство
- Технологии
- Торговля
- Транспорт
- Фармакология
- Физика
- Физиология
- Философия
- Финансы
- Химия
- Хозяйство
- Черчение
- Экология
- Экономика
- Электроника
- Электротехника
- Энергетика
начало термодинамики, энтропия
2 начало термодинамики, энтропия
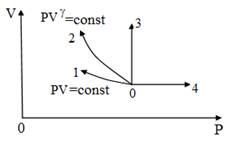 1. Система может перейти из состояния 0 в состояния 1,2,3,4 (см. рисунок; g - показатель адиабаты). Энтропия системы не изменяется в процессе
1. Система может перейти из состояния 0 в состояния 1,2,3,4 (см. рисунок; g - показатель адиабаты). Энтропия системы не изменяется в процессе
1) 0 – 1 2) 0 – 2 3) 0 – 3 4) 0 - 4
2. В изотермическом процессе изменение энтропии идеального газа рассчитывается по формуле
1) 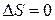 2)
2)  3)
3)  4)
4) 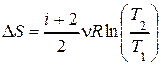
3. Воду массой m = 0,1 кг нагревают от 0°С до 100°С. Удельная теплоемкость воды cУД = 4,19×103 Дж/кг×К. Изменение энтропии при нагревании равно … Дж/К.
1) 131 2) 250 3) 347 4) 589
4. При изотермическом расширении массы m = 6 г водорода (М = 2 г/моль) от давления p1 = 100 кПа до давления p2 = 50 кПа приращение DS энтропии равно … Дж/К.
1) 17,3 2) 52,8 3) 87,6 4) 46,5
5. Масса m = 10 г кислорода (М = 32 г/моль) изохорически нагревается от температуры Т1 = 323 К до температуры Т2 = 423 К, приращение DS энтропии равно … Дж/К. 1) 1,75 2) 2,45 3) 8,76 4) 4,96
6. Масса m = 10 г кислорода (М = 32 г/моль) изобарически нагревается от температуры Т1 = 323 К до температуры Т2 = 423 К, приращение DS энтропии равно… Дж/К. 1) 1,75 2) 2,45 3) 7,63 4) 6,58
7. В процессе изохорического охлаждения постоянной массы идеального газа его энтропия
1) уменьшается 2) увеличивается 3) не изменяется
4) сначала увеличивается, потом уменьшается
8. В процессе адиабатического сжатия постоянной массы идеального газа его энтропия
1) уменьшается 2) увеличивается 3) не изменяется
4) сначала увеличивается, потом уменьшается
9. Энтропия изолированной термодинамической системы в ходе необратимого процесса
1) только увеличивается
2) остается постоянной
3) только убывает
4) сначала увеличивается, потом уменьшается
10. Один моль гелия и один моль азота, находящиеся в закрытых сосудах, нагрели от температуры Т1 до температуры Т2. Выберите правильные утверждения об изменении энтропии в этих процессах
1) изменения энтропий этих газов не зависят от объемов сосудов
2) изменения энтропий этих газов не зависят от скорости нагрева
3) ΔSN2 =ΔSHe
4) ΔSN2 >ΔSHe
11. Воду массой m = 0,1 кг, находящуюся при температуре кипения, превращают в пар. Удельная теплота парообразования воды l = 2,26×106 Дж/К. Изменение энтропии при парообразовании равно … Дж/К.
1) 231 2) 606 3) 347 4) 589
|
|
|
© helpiks.su При использовании или копировании материалов прямая ссылка на сайт обязательна.
|