
- Автоматизация
- Антропология
- Археология
- Архитектура
- Биология
- Ботаника
- Бухгалтерия
- Военная наука
- Генетика
- География
- Геология
- Демография
- Деревообработка
- Журналистика
- Зоология
- Изобретательство
- Информатика
- Искусство
- История
- Кинематография
- Компьютеризация
- Косметика
- Кулинария
- Культура
- Лексикология
- Лингвистика
- Литература
- Логика
- Маркетинг
- Математика
- Материаловедение
- Медицина
- Менеджмент
- Металлургия
- Метрология
- Механика
- Музыка
- Науковедение
- Образование
- Охрана Труда
- Педагогика
- Полиграфия
- Политология
- Право
- Предпринимательство
- Приборостроение
- Программирование
- Производство
- Промышленность
- Психология
- Радиосвязь
- Религия
- Риторика
- Социология
- Спорт
- Стандартизация
- Статистика
- Строительство
- Технологии
- Торговля
- Транспорт
- Фармакология
- Физика
- Физиология
- Философия
- Финансы
- Химия
- Хозяйство
- Черчение
- Экология
- Экономика
- Электроника
- Электротехника
- Энергетика
Законы термодинамики. ВНУТРЕННЯЯ ЭНЕРГИЯ. КОЛИЧЕСТВО ТЕПЛОТЫ
Законы термодинамики
· Нулевой
Если каждая из двух термодинамических систем находится в тепловом равновесии с некоторой третьей, то они находятся в тепловом равновесии друг с другом.
· Первый
Для любого термодинамического цикла сумма чистого тепла, доставленного в систему, и чистой работы, совершённой системой, равна нулю.
· Второй
Энтропия изолированная система не в равновесии имеет тенденцию увеличиваться с течением времени, приближаясь к максимальному значению в равновесии.
· Третий
При стремлении температуры к абсолютному нулю, энтропия системы приближается к постоянному минимуму.
ВНУТРЕННЯЯ ЭНЕРГИЯ
Под внутренней энергией термодинамической системы понимают кинетическую энергию теплового движения ее молекул и потенциальную энергию их взаимодействия. Она зависит от параметров состояния V,T . Внутренняя энергия идеального одноатомного газа прямо пропорциональна его абсолютной температуре:
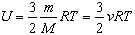
Для газов, состоящих из более сложных молекул, также U ~ Т , но коэффициент пропорциональности другой. Это объясняется тем, что такие молекулы не только движутся поступательно, но и вращаются.
КОЛИЧЕСТВО ТЕПЛОТЫ
Процесс передачи энергии от одного тела к другому без совершения работы называют теплообменом.
Количество теплоты - это энергия, переданная телу в результате теплообмена.
Теплоемкость С - количество теплоты, необходимое для нагревания тела массой m на 1 К. Удельная теплоемкость с - это количество теплоты, которое получает или отдает 1 кг вещества при изменении его температуры на 1 К: c=C/m
Для изменения температуры вещества массой m от Т1 до Т2 ему необходимо сообщить количество теплоты
Коэффициент с в этой формуле называют удельной теплоемкостью: [с]=1 Дж/(кг*К).
При нагревании тела Q > 0, при охлаждении Q < 0.
Для того, чтобы жидкость массы m полностью превратить в пар, ей необходимо передать количество теплоты
Q=rm
где r - удельная теплота парообразования: [r] = 1 Дж/кг .
Удельная теплота парообразования - это количество теплоты, которое необходимо для превращения 1 кг жидкости в пар при постоянной температуре.
Конденсация - процесс, обратный испарению.
Для того, чтобы расплавить полностью тело массой m , ему необходимо сообщить количество теплоты
Q= λm
где - удельная теплота плавления: {λ} = 1 Дж/кг .
Удельная теплота плавления - это количество теплоты, которое необходимо для плавления 1 кг кристаллического вещества при температуре плавления.
Кристаллизация - процесс, обратный плавлению.
Для замкнутой системы, состоящей из N тел, можно записать уравнение теплового баланса:
Q1+...+Qn=0
где Q1, ... , QN - количества теплоты, полученные или отданные телами.
|
|
|
© helpiks.su При использовании или копировании материалов прямая ссылка на сайт обязательна.
|