
- Автоматизация
- Антропология
- Археология
- Архитектура
- Биология
- Ботаника
- Бухгалтерия
- Военная наука
- Генетика
- География
- Геология
- Демография
- Деревообработка
- Журналистика
- Зоология
- Изобретательство
- Информатика
- Искусство
- История
- Кинематография
- Компьютеризация
- Косметика
- Кулинария
- Культура
- Лексикология
- Лингвистика
- Литература
- Логика
- Маркетинг
- Математика
- Материаловедение
- Медицина
- Менеджмент
- Металлургия
- Метрология
- Механика
- Музыка
- Науковедение
- Образование
- Охрана Труда
- Педагогика
- Полиграфия
- Политология
- Право
- Предпринимательство
- Приборостроение
- Программирование
- Производство
- Промышленность
- Психология
- Радиосвязь
- Религия
- Риторика
- Социология
- Спорт
- Стандартизация
- Статистика
- Строительство
- Технологии
- Торговля
- Транспорт
- Фармакология
- Физика
- Физиология
- Философия
- Финансы
- Химия
- Хозяйство
- Черчение
- Экология
- Экономика
- Электроника
- Электротехника
- Энергетика
Федеральное государственное бюджетное образовательное учреждение
Федеральное государственное бюджетное образовательное учреждение
высшего образования «Казанский национальный исследовательский
технический университет им. А.Н. Туполева-КАИ» (КНИТУ-КАИ)
отделение среднего профессионального образования
Курсавая работа на тему:
Явление взрыва.
Выполнил:
Студент группы: 56913
Муртазин Г.В.
Казань
2020
Введение:
· Явление взрыва
· Основные виды превращения взрывчатых систем
· Теплота взрывчатого превращения
· Расчет состава продуктов взрыва
· Заключение
· Список использованных источников
Явление взрыва.
Взрыв представляет собой один из видов физических или химических превращений веществ. В широком смысле слова взрывом называется явление крайне быстрого перехода системы веществ из одного состояния в другое, сопровождающееся столь же быстрым превращением его потенциальной энергии в механическую работу движения или разрушения окружающей среды энергия взрыва может быть различной. Выделение ядерной, химической, электрической, тепловой, кинетической энергии, энергии упругого сжатия способно сопровождаться взрывными процессами.
При ударе движущегося с большой скоростью тела о прочную преграду его кинетическая энергия переходит в тепловую, при достаточном значении энергии могут образоваться сильно сжатые газы. Примером взрывов такой природы является падение крупных метеоритов.
Физическую природу имеют взрывы баллонов со сжатыми газами или взрывы паровых котлов. В первом случае взрыв происходит или за счет чрезмерного повышения давления, например, от случайного разогрева, или вследствие механических повреждений и, как следствие, уменьшения прочности стенок. Во втором случае явление вызвано быстрым переходом перегретой воды в парообразное состояние. При подобных взрывах изменяется только физическое состояние вещества с сохранением неизменности его химического состава.
Примером электрического взрыва могут служить взрывы, которые возникают при мощных искровых разрядах, например, молниях, или при пропускании электрического тока высокого напряжения через тонкие металлические проволочки. При мощных разрядах разность потенциалов выравнивается за промежутки времени порядка 10-6 – 10-7 с, благодаря чему в зоне разряда достигается колоссальная плотность энергии и чрезвычайно высокие температуры (порядка десятков тысяч градусов), что, в свою очередь, приводит к сильному подъему давления воздуха в месте разряда и распространению интенсивного возмущения в окружающей среде.
Примерами взрыва за счет энергии упругого сжатия могут служить гигантские взрывы, протекающие внутри земной коры и приводящие к землетрясениям или разрушению вулканов при их извержении. Накапливаемые в отдельных участках земной коры напряжения могут охватывать весьма большие объемы, а затем, при землетрясении, внезапно освобождаться с выделением огромного количества энергии. Энергия сильнейших землетрясений оценивается в 1016 – 1018 Дж, т.е. превосходит энергию взрыва миллионов тонн взрывчатых веществ (ВВ).
При атомных и термоядерных взрывах, обусловленных реакциями синтеза или деления ядер, достигаются весьма высокие значения параметров продуктов реакции (температуры и давления).
Взрыв может произойти также за счет потенциальной химической энергии, которая превращается в энергию сжатых газов в результате быстрого протекания химической реакции. В данном курсе рассматриваются только взрывы такого рода, т.е. химические взрывы.
Химическую реакцию, сопровождающуюся или способную сопровождаться взрывом, называют взрывчатым превращением. Вещества, способные к взрывчатым превращениям, называют взрывчатыми.
Взрыв в более узком смысле слова представляем собой процесс чрезвычайно быстрого химического превращения вещества, сопровождающийся столь же быстрым выделением тепла и образованием газов.
Взрыв ВВ может протекать в двух различных формах: 1) гомогенного взрыва, 2) самораспространяющегося превращения.
Гомогенный химический взрыв практически не имеет применения во взрывной технике.
Рассмотрим самораспространяющийся взрыв. Пусть в небольшой части заряда ВВ путем сильного разогрева вызвана быстрая химическая реакция. При определенных условиях эта реакция будет самопроизвольно распространяться с большой скоростью от места ее возбуждения до границ заряда. На использовании такого самораспространяющегося взрыва основана вся современная взрывная техника. Следовательно, взрыв ВВ представляет собой самораспространяющееся с большой скоростью химическое превращение, протекающее с выделением большого количества тепла и образованием газов.
Из изложенного следует, что химическая реакция, протекающая в форме взрыва, определяется тремя следующими основными условиями: 1) экзотермичностью химической реакции; 2) наличием газообразных (парообразных) продуктов реакции; 3) большой скоростью химической реакции. У различных ВВ эти свойства могут быть выражены в различной степени, но только их совокупность придает явлению характер взрыва.
Три условия в своем сочетании определяют не только возможность самораспространения химической реакции в форме взрыва, но и механическое действие взрыва. Рассмотрим роль каждого из этих факторов.
Экзотермичность реакции.Выделение тепла является первым необходимым условием, без которого возникновение взрывного процесса вообще невозможно. Теплота химической реакции при взрыве является источником энергии. Если бы реакция не сопровождалась выделением теплоты, самораспространение взрыва было бы исключено. Очевидно, что вещества, требующие для своего разложения притока энергии извне (эндотермическая реакция), не могут обладать взрывчатыми свойствами.
За счет тепловой энергии реакции происходит разогрев газообразных продуктов до температуры в несколько тысяч градусов и последующее их расширение. Чем больше теплота реакции и скорость ее распространения, тем больше разрушительное действие взрыва.
Теплота реакции является важнейшей характеристикой ВВ. Для современных промышленных ВВ теплота взрыва колеблется от 2900 до 7500 кДж/кг.
Образование газов. Высокие давления, возникающие при взрыве, и обусловленный ими разрушительный эффект достигаются вследствие того, что химическая реакция при взрыве сопровождается образованием большого количества газообразных продуктов.
Образование газов делает возможным взрыв. Это определятся тем, что газы имеют значительно меньшую плотность, чем твердые или жидкие вещества, так что переход твердого или жидкого вещества в газы в постоянном объеме приводит к резкому возрастанию давления. Кроме того, газы имеют значительно больший коэффициент объемного расширения, чем твердые или жидкие вещества.
Вследствие этих особенностей газы или пары/ и являются тем непосредственным физическим агентом, который, расширяясь, производит механическую работу. Чем больше объем газов или паров по сравнению с объемом вещества до взрыва, тем (при прочих равных условиях) больше сила взрыва. У промышленных ВВ объем газов, приведенный к нормальным физическим условиям равен 600-1000 л. на 1 кг.ВВ.
Значение фактора газообразования для взрывных процессов может быть проиллюстрировано на ряде реакций, при которых не образуются газообразные продукты. Так, например, даже сильно экзотермическая, но не образующая газов реакция сгорания термитной смеси, проходящая по уравнению
Al +Fe2O3= Al2O3+2Fe+840 кДж, (1)
несмотря на большое количество выделяющегося при реакции тепла, не дает взрыва. Тепловой эффект реакции (1) является достаточным для нагревания конечных продуктов (Fe, Al2O3) до температуры 30000С, при которой они находятся в жидком состоянии.
Наблюдаемый в условиях воспламенения больших количеств термитной смеси довольно сильный взрыв является следствием вторичных явлений, связанных с разогревом и расширением окружающего воздуха, а также воздуха или образующих газы примесей, заключенных в рыхлой массе термитной смеси. Кроме того, может также частично происходить весьма быстрое сгорание распыленного порошкообразного алюминия за счет кислорода воздуха.
Скорость реакции. Самым характерным признаком взрыва, отличающим его от обычных химических реакций, является большая скорость процесса. Переход вещества к конечным продуктам взрыва происходит за стотысячные и миллионные доли секунды. Большая скорость выделения энергии определяет преимущества ВВ по сравнению с обычными горючими веществами, хотя по количеству освобождаемой при реакции взрыва энергии при расчете единицы массы вещества ВВ не имеют перед ними каких-либо преимуществ
Все исследования детонационных и взрывчатых характеристик взрывчатых систем сводятся, по существу к решению трех основных проблем:
- Определение теплоты взрыва, удельного объема и состава продуктов взрывчатого превращения;
- Расчет давлений Р1 и Р2 в плоскостях химического пика и Чемпена-Жуге соответствующих закономерностей их изменения в зоне химических реакций при последующем изоэнтропном расширении;
- Отыскания возможностей прогнозирования детонационных свойств вновь синтезируемых ВВ.
Строгое решение перечисленных вопросов должно базироваться на учете законов гидродинамики, газовой динамики, термохимии и химической кинетики.
Остановимся, прежде всего, на термодинамических и термохимических характеристиках ВВ.
Фундаментальными характеристиками любой термодинамической системы являются внутренняя энергия U, энтальпия i и энтропия S.
Внутренняя энергия характеризует запас энергии системы, включая энергию поступательного, колебательного и вращательного движения атомов и молекул. Важно отметить, что внутренняя энергия не учитывает кинетическую энергию движения системы в целом и потенциальную энергию ее положения. Другими словами, внутренняя энергия замкнутой термодинамической системы не изменяется, при сообщении ей той или иной скорости или перемещения ее в гравитационном поле.
При переходе системы из любого начального состояния (1) в любое конечное состояние (2) изменение внутренней энергии ΔU=U2-U1 всегда одно и то же вне зависимости от пути и способа перехода. Это непосредственно вытекает из закона сохранения энергии.
Следовательно, внутренняя энергия есть однозначная функция состояния системы (параметр состояния), а ее бесконечно малое приращение dU является полным дифференциалом от переменных состояния (давления Р, удельного объема V и температуры Т).
Энтальпия(называется также теплосодержанием или тепловой функцией Гиббса) связана с U соотношением:
i=U+PV, (2)
т е энтальпия представляет собой совокупность внутренней энергии и потенциальной энергии давления (внешней энергии).
Энтропия определяется соотношением:
dS=dQ/T (3), [ккал/кг*град]
Все тепло подводимое к веществу можно представить в виде суммы двух составляющих: внешнего тепла, подводимого извне, и внутреннего тепла, выделяющегося в результате действий сил трения. Внешнее тепло подводится к системе либо отводится, в то время как внутреннее тепло может только выделятся, т.е. всегда положительно. Следовательно, энтропия изолированной системы может только возрастать и лишь для идеальной системы она может оставаться постоянной.
2) Теплота взрыва является энергетической предпосылкой спонтанной взрывной реакции.
Теплота взрыва – важнейшая энергетическая характеристика ВВ. Она одновременно является определяющей характеристикой, т.к. от нее зависят скорость детонации, температура взрыва, работоспособность и общее действие взрыва.
Несмотря на столь большое значение теплоты взрыва, взрывчатники чаще всего изучали такие взрывчато-технические характеристики, как скорость детонации, бризантность или работоспособность, которые непосредственно определяют местное или общее действие взрыва.
Опытное определение теплоты взрыва трудоемко, требует специального и громоздкого оборудования. Кроме того, для одного опыта требуется 50-100 гр. ВВ, которое не всегда имеется в наличии, особенно когда идет речь об исследовании нового ВВ.
Раньше теплоты взрывчатого превращения, как правило, определяли в малых калориметрических или манометрических бомбах и применяли навески 1-2 г. Очевидно, что в этих случаях определялась не теплота детонации, (она нас главным образом и интересует), а теплота взрывчатого превращения, которая для большинства ВВ ниже первой. Вот почему в старой литературе часто можно встретить явно заниженные и разноречивые данные по теплотам взрыва таких ВВ, как тротил, тетрил, пикриновая кислота, и даже гексоген. Эти данные невозможно было применять для расчета других характеристик ВВ или зарядов, т.к.получались совершенно неудовлетворительные результаты. Поэтому, теоретические зависимости, в которых фигурирует величина теплоты взрыва не могут быть эффективно использованы для практических целей.
В последние годы нашли широкое применение большие калориметрические бомбы для непосредственного определения теплот взрыва сравнительно больших зарядов ВВ (50-100 г. диаметр заряда 40-50 мм.). При этом создаются благоприятные условия для протекания в заряде ВВ стационарного детонационного процесса и для закалки реакции. Это позволяет дублировать и контролировать данные калориметрирования с теплотами взрыва, подсчитанными на основании состава продуктов взрыва. Существуют различные конструкции установок, которые позволяют определять теплоты взрыва с точностью до 1-2 %. Применение современной калориметрии позволило получить надежные данные по теплотам взрыва не только штатных ВВ, но и для новых взрывчатых веществ и композиций. Очевидно, что для получения надежных и достоверных данных по теплоте взрыва недостаточно одного или двух опытов, а это связано не только с длительными и трудоемкими экспериментами, но и с большим расходом ВВ.
На практике перед исследователями часто возникают вопросы, связанные с энергетическими характеристиками ВВ, и при этом нет возможности определить их опытным путем либо потому, что имеется малое количество ВВ, либо ВВ еще не синтезировано вовсе, т.е. имеется лишь формула ВВ.
Поэтому задача по теоретическому расчету теплот взрыва и других характеристик ВВ по его формуле имеет не только чисто теоретическое, но и практическое значение, т.к. позволяет оценить достоинства и недостатки не только известных и вновь синтезируемых ВВ, но предсказать характеристики новых, еще не синтезированных ВВ.
В первом случае расчет позволяет сэкономить средства и время, необходимые для опытного определения этих характеристик ВВ, а когда количество ВВ мало, опытное количество вообще невозможно.
Во втором случае оценка свойств ВВ до его синтеза позволяет решить вопрос о целесообразности синтеза того или иного вещества, что также позволяет сэкономить средства и творческие силы исследователей. Таким образом, широкое использование расчетных методов позволяет не только предсказывать ряд свойств ВВ, но ускоряет процесс исследования и тем самым как бы повышает производительность труда исследователя. Этими обстоятельствами можно объяснить многочисленные попытки разработки методов расчета ряда энергетических и взрывчатых характеристик ВВ, в частности теплот взрыва, сгорания и образования. Ближайшей целью этих расчетов является теплота взрыва ибо, как было указано выше, по ней можно вычислить ряд других характеристик.
Химическое превращение ВВ, происходящее при взрыве, сопровождается изменением энергии системы.
Согласно первому принципу термодинамики изменение внутренней энергии системы будет:
ΔU=q-A, (4)
где ΔU – изменение внутренней энергии,
q – выделившееся или поглощенное системой тепло,
A – работа, совершенная системой и равная:
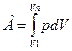 (5)
(5)
При изохорном процессе А=0, тогда ΔU=q.
Таким образом, тепловой эффект реакции, происходящей при V=const, равен изменению внутренней энергии.
Используя обозначения тепловых эффектов, принятые в химии, можно написать, что:
-ΔU=QV (6)
где QV – тепловой эффект при постоянном объеме.
Еще задолго до открытия первого принципа термодинамики в 1840 г. русским академиком Г.И. Гессом был открыт основной закон термохимии, который является частным случаем первого принципа термодинамики.
В соответствии с законом Гесса тепловой эффект реакции зависит только от начального и конечного состояния системы и равен алгебраической сумме теплот промежуточных реакций, т.е.:
Q1,n=Q1,2+Q2,3+Q3,4+…+Qn-1,n (7)
где индексы 1 и n соответственно начальное и конечное состояния, а индексы 2, 3, …, n-1 – промежуточные состояния системы.
Чаще всего число состояний системы берут равным 3, и тогда:
Q1,3=Q1,2+Q2,3 (8)
Термохимия процессов сгорания и взрывчатого превращения ВВ полностью описывается этим уравнением.
В первом случае
Qсг=Qпс-Qобр (9)
Во вором случае
Qвзр=Qп.в.-Qобр. (10)
Где Qсг – теплота сгорания, т.е. количество тепла, выделяющееся при полном окислении одного моля или килограмма ВВ в атмосфере кислорода;
Qпс – сумма теплот образования продуктов сгорания из простых веществ;
Qобр – теплота образования ВВ из простых веществ;
Qвзр – теплота взрывчатого превращения, т.е. количество тепловой энергии, выделяющееся при взрыве ВВ;
Qп.в – сумма теплот образования продуктов взрыва.
Из сказанного следует, что для расчета теплоты взрыва того или иного ВВ необходимо знать теплоту его образования (см. табл. 3) и уравнение реакции взрывчатого превращения.
|
|
|
© helpiks.su При использовании или копировании материалов прямая ссылка на сайт обязательна.
|