
- Автоматизация
- Антропология
- Археология
- Архитектура
- Биология
- Ботаника
- Бухгалтерия
- Военная наука
- Генетика
- География
- Геология
- Демография
- Деревообработка
- Журналистика
- Зоология
- Изобретательство
- Информатика
- Искусство
- История
- Кинематография
- Компьютеризация
- Косметика
- Кулинария
- Культура
- Лексикология
- Лингвистика
- Литература
- Логика
- Маркетинг
- Математика
- Материаловедение
- Медицина
- Менеджмент
- Металлургия
- Метрология
- Механика
- Музыка
- Науковедение
- Образование
- Охрана Труда
- Педагогика
- Полиграфия
- Политология
- Право
- Предпринимательство
- Приборостроение
- Программирование
- Производство
- Промышленность
- Психология
- Радиосвязь
- Религия
- Риторика
- Социология
- Спорт
- Стандартизация
- Статистика
- Строительство
- Технологии
- Торговля
- Транспорт
- Фармакология
- Физика
- Физиология
- Философия
- Финансы
- Химия
- Хозяйство
- Черчение
- Экология
- Экономика
- Электроника
- Электротехника
- Энергетика
Слайд 5-6. Изомерия.По правилам составления структур и названийуглеводородов. Нумерация атомов углерода в формуле начинается с атома углерода функциональной группы.
Слайд 1. Тема Альдегиды
Слайд 2. R –это радикал углеводородный (Вспомните! R – Это частица от углеводородов, имеющая свободную валентность, например CH3- метил,
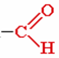 | 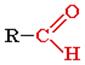 | ||
C 2H5 – этил и т.д. Формула молекулы альдегида состоит из R- функциональной группы. Строение функциональной группы:
Общая форлула по числу атомов углерода и водорода CnH2nO для любого альдегида в гомологическом ряду. Например n=1,формула HСOH, или CH2O, n=2 СH3 – COH→ C2H4O или функциональная группа изображается структурой (как показано выше наискосок)
Слайд 3. Электронное строение молекулы. Показано, что электронная плотность в молекуле сдвигается к кислороду как наиболее отрицательному элементу.
Слайды 4-5. Названия альдегидов. Сокращенное название класса альдегидов – али. Один – аль. (аль- это, по сути, название функциональной группы. Названиепредельных альдегидов состоит из названия алкана по числу атомов углерода, с окончанием аль.
Например,n=1, производное метана, метаналь,n= 2 этаналь, n=3 пропаналь и т.д., по гомологическому ряду алканов.
Слайд 5-6. Изомерия.По правилам составления структур и названийуглеводородов. Нумерация атомов углерода в формуле начинается с атома углерода функциональной группы.
Слайд 7. Физические свойства отличаются от спиртов тем, что между молекулами не образуются водородные связи, поэтому есть газ – первый в гомологическом ряду -метаналь. Плохо растворяются в воде, легко кристализуются из растворов. Например, 40% раствор метаналя ( другое название формальдегид, это тривиальное название он получил за то, что его стуктурная формула представляет со всех сторон функциональную группу *форма альдегида*) – формалин,должен быть свежеприготовленным и при хранении кристаллизуется. Сильный яд. Все альдегиды ядовиты.
Слайд 8-9. Химические свойства.7№. Перечислены названия основных реакций. №8 уравнения реакций: 1). Это реакция восстановления альдегидов в спирты реакцией присоединения водорода по месту разрыва двойной связи C=O, в функциональной группе. Эта группировка является главной в альдегидах и называется карбонильнаяиликарбонил.Получается, как вы видите, спирт одноатомный. Например.
CH3 – COH + H2 → CH3 – CH2OH
Этаналь Этанол
! вспомните что альдегиды можно получить из спиртов.
2). Это реакция окисления – происходит по связи С- Н в функциональной группе. Водородокисляется кислородом или другими окислителями в гидроксильную группу, при этом образуется следующий класс – карбоновые кислоты. CH3 – COH + O2 → CH3 – COOH
Этаналь этановая кислота
Уксусный альдегид уксусная кислота
Ацетальдегид
3) Это реакция окисления. Окисление происходит аммиачным раствором оксида серебра, который представляет комплексную соль. В упрощенном виде из этой соли взаимодействует оксид серебра, который в чистом виде не существует. CH3 – COH + Ag2O→ CH3 – COOH + 2Ag↓
Оксид серебра
Эта реакция – качественная на альдегидную группу. При проведении на стекле выделяется серебро и блестит как зеркало, поэтому она называется *реакция серебряного зеркала*. Эта реакция лежит в основе получения зеркал.
4). Реакция поликонденсации. Реакция отличается от полимеризации тем что побочным продуктом выделяется какое либо низкомолекулярное вещество, например в данном случае вода.
Взаимодействие метаналя с ароматическим спиртом фенолом. Образуется фенолформальдегидная смола.
 |
n —OH + nCH2O → полимер фенолформальдегид.
5). Есть общая реакция альдегидов и многоатомных спиртов, это реакция взаимодействия с гидроксидом меди (II), Cu(OH)2
Эта реакция является качественнойна многоатомные спирты ( вспомните, осадок гидроксида меди (II), Cu(OH)2 ↓ растворяется с образованием раствора яркосинего цвета).
При взаимодействии альдегида с Cu(OH)2 ↓происходит окисление альдегидной группы и восстановление с Cu(OH)2 до оксида меди(I), с Cu2O – осадок кирпично-красного цвета.
CH3 – COH + Cu(OH)2 ↓→ CH3 – COOH + Cu2O↓
|
|
|
© helpiks.su При использовании или копировании материалов прямая ссылка на сайт обязательна.
|