
- Автоматизация
- Антропология
- Археология
- Архитектура
- Биология
- Ботаника
- Бухгалтерия
- Военная наука
- Генетика
- География
- Геология
- Демография
- Деревообработка
- Журналистика
- Зоология
- Изобретательство
- Информатика
- Искусство
- История
- Кинематография
- Компьютеризация
- Косметика
- Кулинария
- Культура
- Лексикология
- Лингвистика
- Литература
- Логика
- Маркетинг
- Математика
- Материаловедение
- Медицина
- Менеджмент
- Металлургия
- Метрология
- Механика
- Музыка
- Науковедение
- Образование
- Охрана Труда
- Педагогика
- Полиграфия
- Политология
- Право
- Предпринимательство
- Приборостроение
- Программирование
- Производство
- Промышленность
- Психология
- Радиосвязь
- Религия
- Риторика
- Социология
- Спорт
- Стандартизация
- Статистика
- Строительство
- Технологии
- Торговля
- Транспорт
- Фармакология
- Физика
- Физиология
- Философия
- Финансы
- Химия
- Хозяйство
- Черчение
- Экология
- Экономика
- Электроника
- Электротехника
- Энергетика
РЯД НАПРЯЖЕНИЙ (АКТИВНОСТИ) МЕТАЛЛОВ
Химические свойства солей. Примеры реакций
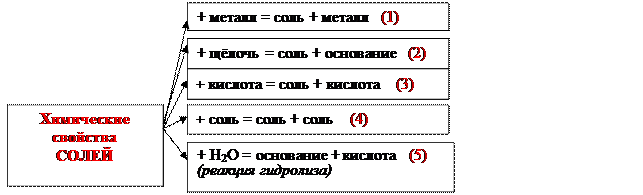
Например:
(1) Активный металл + соль = неактивный металл +соль
Fe + CuSO4 = Cu + FeSO4
Ме слева Ме справа в ряду напряжений (активности) металлов
(cмотреть ряд активности металлов ! стр 49 и стр.108)
РЯД НАПРЯЖЕНИЙ (АКТИВНОСТИ) МЕТАЛЛОВ
Li Rb K Ca Na Mg Al Mn Zn Cr Fe Cd Ni Sn Pb H Cu Hg Ag Au
металлическая активность уменьшается

(2) Соль + щёлочь = соль + основание
AlCl3 + 3NaOH = 3NaCl +Al(OH)3 ↓ (в реакции обмена образование осадка!!!)
Р р р н
(смотреть таблицу растворимости стр. 62 и стр.112 )
(3) Соль + сильная кислота = соль + слабая кислота
FeS + H2SO4 = FeSO4+ H2S↑ (в реакции обмена образование газа!!!)
(смотреть таблицу растворимости стр. 62 и стр.112 )
(4) Соль + соль = соль + соль
BaCl2 + Na2SO4 = BaSO4 ↓+ 2NaCl (в реакции обмена образование осадка!!!)
Р р н р
(смотреть таблицу растворимости стр. 62 и стр.112 )
(5) Соль + Н2О = основание(↓) + кислота (↑)
(реакция гидролиза)
Al2S3 + 6HOH = 2Al(OH)3 (↓) + 3H2S (↑)
(смотреть таблицу растворимости стр. 62 и стр.112 )
А ТЕПЕРЬ РАБОТАЙТЕ НА УРОКЕ САМОСТОЯТЕЛЬНО!!!!!
1) Узнать (у преподавателя) СВОЙ ВАРИАНТ соли.
2)Написать уравнения всех (5) реакций,
3) Назвать вещества, которые участвуют в реакции.
Примеры солей:
1) Al(CN)3 2) Fe2(CO3)3 3) Cr(NO2)3 4) SnSiO3 5) Cr2S3
6) FeSO3 7) CuCO3 8) Al2(SO3)3 9) Zn(HCO3)2 10) Au2(SiO3)3
Домашнее задание Написать все реакции (5 реакций) . По 2 примера для каждой реакции.
Таблица растворимости солей, кислот и оснований в воде (стр.62)
| Катион анион | H+ | NH4+ | K+ | Na+ | Ag+ | Ba2+ | Ca2+ | Mg2+ | Zn2+ | Cu2+ | Hg2+ | Pb2+ | Fe2+ | Fe3+ | Cr3+ | Al3+ |
| OH- | P | P | P | – | P | M | M | H | H | – | H | H | H | Н | H | |
| NO3 - | P | P | P | P | P | P | P | P | P | P | P | P | P | P | Р | P |
| Cl- | P | P | P | P | H | P | P | P | P | P | P | M | P | P | Р | P |
| SO42- | P | P | P | P | M | H | M | P | P | P | – | M | P | P | Р | P |
| CrO42- | P | P | P | P | H | H | M | P | H | H | H | H | – | – | – | |
| SO32- | P* | P | P | P | M | M | M | P | M | – | – | H | M | – | Г | – |
| S2- | P* | P | P | P | H | P | – | – | H | H | H | H | H | H | Г | – |
| CN- | P | P | P | P | H | M | P | Г | H | H | P | M | H | H | Н | Г |
| PO43- | P | P | P | P | H | H | H | H | H | H | H | H | H | H | Н | H |
| СО32- | М* | Р | Р | Р | Н | Н | Н | Г | Г | Г | Г | Г | Н | Г | Г | Г |
| CH3COO- | P | P | P | P | P | P | P | P | P | P | P | P | P | P | Р | P |
| SiO32- | H | Г | Р | Р | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н |
| NO2- | Р* | Р | Р | Р | М | Р | Р | Р | Р | Р | Р | Р | Р | Г | Г | Г |
P - растворимое ( >1 г в 100 г воды);
Р*-разлагается при выделении из раствора.
M - малорастворимое (0,001 г - 1г в 100 г воды);
H - нерастворимое (< 0,001 г в 100 г воды);
– - разлагается водой или не существует.
Г –полный необратимый гидролиз в воде
|
|
|
© helpiks.su При использовании или копировании материалов прямая ссылка на сайт обязательна.
|