
- Автоматизация
- Антропология
- Археология
- Архитектура
- Биология
- Ботаника
- Бухгалтерия
- Военная наука
- Генетика
- География
- Геология
- Демография
- Деревообработка
- Журналистика
- Зоология
- Изобретательство
- Информатика
- Искусство
- История
- Кинематография
- Компьютеризация
- Косметика
- Кулинария
- Культура
- Лексикология
- Лингвистика
- Литература
- Логика
- Маркетинг
- Математика
- Материаловедение
- Медицина
- Менеджмент
- Металлургия
- Метрология
- Механика
- Музыка
- Науковедение
- Образование
- Охрана Труда
- Педагогика
- Полиграфия
- Политология
- Право
- Предпринимательство
- Приборостроение
- Программирование
- Производство
- Промышленность
- Психология
- Радиосвязь
- Религия
- Риторика
- Социология
- Спорт
- Стандартизация
- Статистика
- Строительство
- Технологии
- Торговля
- Транспорт
- Фармакология
- Физика
- Физиология
- Философия
- Финансы
- Химия
- Хозяйство
- Черчение
- Экология
- Экономика
- Электроника
- Электротехника
- Энергетика
ХИМИЧЕСКАЯ ТЕХНОЛОГИЯ СТЕКЛА И СИТАЛЛОВ» Модуль 6. ПРОИЗВОДСТВО СИТАЛЛОВ
«ХИМИЧЕСКАЯ ТЕХНОЛОГИЯ СТЕКЛА И СИТАЛЛОВ» Модуль 6. ПРОИЗВОДСТВО СИТАЛЛОВ
В шестом разделе рассмотрены теоретические основы синтеза ситаллов, свойств и применения технических ситаллов, и ситаллам на основе промышленных отходов и горных пород.
Изучив данный раздел, вы будете иметь представление:
- о природе ситаллов;
- о классификации ситаллов по химическому составу;
- о видах катализаторов в производстве ситаллов.
Вы будете знать:
- основные этапы производства ситаллов;
- свойства ситаллов, зависящих от химического состава;
- требования, предъявляемые к катализаторам;
- режим термической обработки для кристаллизации стекла.
Одним из революционных открытий ХХ в. в технологии стекла явилась разработка стеклокристаллических материалов, названных в СССР ситаллами (в США – пирокерамами).
 Ситалл – искусственный поликристаллический материал, полученный кристаллизацией стекла соответствующего химического состава и обладающий более высокими по сравнению с этим стеклом физико-химическими свойствами.
Ситалл – искусственный поликристаллический материал, полученный кристаллизацией стекла соответствующего химического состава и обладающий более высокими по сравнению с этим стеклом физико-химическими свойствами.
Слово «ситалл» происходит от двух слов – первая буква «с» позаимствована от слова «стекло», затем связывающий союз «и», а вторая часть взята от окончания слова «кристалл».
Стеклокристаллические материалы по своей природе и технологии получения являются своего рода гибридом стекла и керамики. От стекла они отличаются зернистой, кристаллической структурой. На керамику не похожи, потому что их кристаллы намного меньше, а структура монолитнее.
Ситаллы имеют важное преимущество перед керамикой: их можно формовать по обычной технологии стекольного производства, прессовать, прокатывать, вытягивать, выдувать, а также изготовлять порошковым методом, который нашел распространение в керамической промышленности.
 Известные в настоящее время стеклокристаллические материалы подразделяются на две группы: технические ситаллы, синтезируемые на основе чистых оксидов и предназначенные для специальных целей, и шлакоситаллы, получаемые на основе доменных шлаков и предназначенные для массового использования в различных областях промышленности и строительства.
Известные в настоящее время стеклокристаллические материалы подразделяются на две группы: технические ситаллы, синтезируемые на основе чистых оксидов и предназначенные для специальных целей, и шлакоситаллы, получаемые на основе доменных шлаков и предназначенные для массового использования в различных областях промышленности и строительства.
Синтез ситаллов можно осуществлять с заранее заданными свойствами, что обусловливает обширную сферу их применения.
Ситаллы обладают высокой температурой размягчения (свыше 1350 ºС), высокой твердостью и стойкостью к химическим агрессивным средам, а также являются диэлектриками. Ситаллы отличаются хорошим сопротивлением термоударам. Пластинки, нагретые до 900 ºС при погружении в воду с температурой 5 ºС не растрескиваются. Испытания показали, что сопротивление ситаллов истиранию во много раз больше, чем у стекла и керамики.
Характерная особенность закристаллизованных стекол – однородная микрокристалличность. Размеры кристалликов могут колебаться в пределах 0,1-1 мкм. Присутствие этих кристалликов – необходимое условие прочности материала. Сеть мелких кристалликов, сросшихся друг с другом или соединенных тонкой стеклообразной прослойкой, затрудняет развитие трещин в изделии по границам зерен и в каждом зерне в отдельности.
6.1. Теоретические основы синтеза ситаллов
Направленная кристаллизация стекла, используемая для получения стеклокристаллических материалов типа ситаллов и шлакоситаллов, состоит в следующем.
В стекломассу, обладающую оптимальной склонностью к объемной кристаллизации, вводят интенсифицирующие процесс кристаллизации добавки – катализаторы. Введение небольших количеств катализаторов приводит при соответствующей тепловой обработке к образованию в стекле центров кристаллизации, способствующих получению тонкокристаллической структуры в материале при последующей объемной кристаллизации стекла при более высоких температурах.
 Таким образом, превращение стекла в ситалл предусматривает:
Таким образом, превращение стекла в ситалл предусматривает:
1) что стекло должно иметь нужный химический состав (обеспечивать образование таких, например, кристаллических фаз, как кордиерит, сподумен, муллит, волластонит);
2) процесс кристаллизации такого стекла должен осуществляться по особому методу (термическая обработка должна обеспечить образование зародышей кристаллов и их превращение в микрокристаллы с переходом стекла в более или менее закристаллизованное состояние).
Важной стадией превращения стекла в ситалл является процесс образования центров кристаллизации. Они могут возникнуть самопроизвольно (гомогенный механизм) или в результате внесения посторонних частиц извне (гетерогенное зародышеобразование).
Процесс зародышеобразования по гомогенному механизму объясняют на основе теории флуктуаций. Образование зародышей связано с особым состоянием охлаждаемой жидкости, когда возрастает вероятность возникновения микроскопических сгустков молекул. Эти флуктуации плотности могут давать такие сочетания молекул, которые способны стать зародышами новой фазы.
Работа образования зародыша в значительной степени зависит от поверхностного натяжения на границе «зародыш – жидкость». В связи с этим существенное значение могут иметь добавки, влияющие на поверхностное натяжение.
 Вещества, инициирующие процесс зарождения центров кристаллизации, называют катализаторами (инициаторами, нуклеаторами). Катализатор кристаллизации стекла выступает и в роли ускорителя, и в роли участника процесса.
Вещества, инициирующие процесс зарождения центров кристаллизации, называют катализаторами (инициаторами, нуклеаторами). Катализатор кристаллизации стекла выступает и в роли ускорителя, и в роли участника процесса.
Требования к катализаторам следующие:
- катализатор должен иметь неограниченную растворимость в стекле при высоких температурах и ограниченную растворимость при низких температурах;
- катализатор должен обладать низкой энергией активации при образовании центров кристаллизации из расплава в области пониженных температур;
- ионы или атомы катализатора должны иметь повышенную скорость диффузии при низких температурах по сравнению с основными компонентами стекла;
- граница «зародыш кристалла – стекло» должна иметь низкую поверхностную энергию, чтобы обеспечить смачивание кристалла стеклом;
- параметры кристаллической решетки катализатора и выделяющейся кристаллической фазы должны быть близки и не отличаться более чем на 10-15 %.
В качестве катализаторов применяют металлические (Сu, Ag, Au, Si, Pt), оксидные (TiO2, P2O5, Cr2O3, ZrO2, ZnO, SnO2, WO3, MoO3 и др.) и комбинированные (As2O3 + MoO3, TiO2 + MeF2, AgCl + SnO2) вещества.
О механизме действия катализаторов существуют разные гипотезы. Представление о катализаторе, который при известных условиях сам образует зародыши будущих кристаллических зерен главной фазы, справедливо применительно к катализатором металлического типа (золото, серебро и т. д.). Что касается катализаторов оксидного типа (оксида титана, циркония, фосфатов и др.), то вопрос о механизме их действия не может в настоящее время считаться решенным. Имеются основания считать, что оксидные катализаторы способствуют ликвации стекол на две фазы, и это обусловливает появление центров кристаллизации и облегчает рост кристаллических зерен. Причиной резкого увеличения скорости зародышеобразования вследствие ликвации может быть развитие поверхности между стеклообразными фазами и приближение химического состава микрофаз к составу будущих кристаллов, повышающее скорость их кристаллизации.
Ситаллы получают из расплавов, застывающих в стекловидной форме и способных при повторном нагревании выделять определенные кристаллические фазы, или применяют порошки, но не кристаллические, а стекловидные, которые при нагревании кристаллизуются и спекаются в монолитный материал поликристаллического строения.
Отличительная особенность технологии ситаллов состоит в ее генетической связи с технологией стекла. Технологическая схема производства стекла (получение шихты, варка стекла, формование изделий и отжиг изделий) дополняется еще одним этапом – кристаллизацией, которая может идти за формованием, минуя отжиг, или осуществляться после отжига.
Специфическими элементами технологии ситаллов являются следующие:
- Шихта содержит катализатор кристаллизации.
- При использовании летучих катализаторов (фториды, сульфиды) приходится прибегать к специальным мерам по предупреждению потерь этих компонентов, т. к. количество катализатора должно быть определенным. Например, при варке стекол, содержащих сульфидную серу, во избежание ее выгорания недопустимо присутствие кислорода в газовом пространстве. Варку проводят в восстановительных или нейтральных условиях. При использовании диоксида титана важно поддерживать определенные температурные и окислительно– восстановительные условия.
- Многие ситаллы являются «короткими» и имеют узкий температурный интервал формования, к тому же он сдвинут в область повышенных температур. Область формования соответствует вязкости от 1 · 102 до 4 · 107 Па·с, поэтому чаще всего при формовании ситаллов применяют литье (чаще центробежное) и прессование.
При направленной кристаллизации стекла важное значение имеет режим термической обработки. В зависимости от состава стекла, типов кристаллизаторов и назначения ситаллов применяют одно-, двух- и трехступенчатые режимы кристаллизации.
На рис. 6.1 приведен двухступенчатый режим термической обработки, включающий следующие стадии:
а и б – охлаждение или нагревание стекла до заданной температуры первой ступени кристаллизации – I; на этой стадии образуются центры кристаллизации и создается кристаллический каркас будущего тела ситалла; эта стадия протекает при температуре 700-750 ºС и выдержке 0,5-1 ч;
в – медленное нагревание (3-7 град/мин) до температуры второй ступени кристаллизации – II; на этой стадии происходит выделение основной кристаллической фазы на основе образовавшихся ранее центров кристаллизации; вторая ступень кристаллизации протекает при температуре 900-950 ºС и выдержке в течение 1-1,5 ч;
г – медленное охлаждение закристаллизованного стекла до температуры окружающей среды.
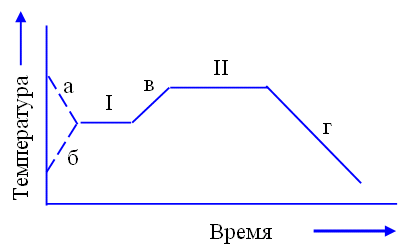
Рис. 6.1. Температурный режим двухступенчатой кристаллизации
6.2. Свойства и применение технических ситаллов
Природа свойств ситаллов имеет много общего с природой тех же свойств исходного стекла и аналогичных керамических материалов, и в то же время превосходит по этим показателям исходное стекло и близкие виды керамики.
- Ситаллы в несколько раз прочнее стекла, большинства керамических материалов и некоторых металлов. Их прочность при изгибе может достигать 2500-3000 кг/см2, а отдельных экспериментальных образцов – 4200 и 5600 кг/см2, т. е превышает прочность кварцевого стекла, нержавеющей стали и титана.
- Плотная микрокристаллическая структура ситаллов обеспечивает им твердость при вдавливании, приближающуюся к твердости закаленных сталей и превышающую твердость плавленого кварца, латуни, чугуна, гранита и стекла. Микротвердость пирокерама 9606 (по методу Виккерса) составляет 640 кг/мм2, в то время как для закаленной стали она равна 550-580 кг/мм2.
- Коэффициент термического расширения у ситаллов может варьироваться в очень широких пределах – от отрицательных значений (–10) до +130·10–7 град–1, что делает их пригодными для спаивания с тяжелыми металлами.
- Кислотоустойчивость большинства ситаллов примерно такая же, как у боросиликатного стекла, а устойчивость к действию щелочей более высокая, ситаллы не окисляются даже при высоких температурах.
- В большинстве ситаллы непрозрачны, однако получен ряд ситаллов, содержащих не менее двух кристаллических фаз, но полностью прозрачных благодаря отсутствию пузырей или пустот, малому размеру кристаллов или отсутствию светорассеяния на границах кристаллов, что требует хорошего совпадения показателей преломления кристаллов и стекловидной фазы.
- Ситаллы обладают нулевым водопоглощением и газонепроницаемы, их можно применять в вакуумных приборах с высоким разряжением.
- Плотность ситаллов колеблется в пределах 2,5-2,72 г/см3.
- Ситаллы имеют плотную микрокристаллическую структуру, подобную структуре керамических материалов на основе чистых оксидов, характеризуемую весьма малыми размерами беспорядочно ориентированных кристаллов и отсутствием пористости. Размеры кристаллов у фосфатсодержащих ситаллов от 0,5 до 6 мкм (вместо 20-50 мкм для обычной керамики).
Технические ситаллы могут быть разбиты на подгруппы либо по составу (литийсодержащие или сподуменовые, свинецсодержащие, высококремнеземистые и др.), либо по ведущему свойству (термостойкие, прозрачные и т. д.), особую подгруппу составляют фотоситаллы.
Ситаллы сподуменового состава относятся к системе Li2O–Al2O3–SiO2. Стекла состава сподумена или эвкриптита могут быть закристаллизованы с образованием сподумена, эвкриптита, кварцеподобных твердых растворов и других фаз. В качестве катализатора обычно применяют 4-6 % TiO2. Термическая обработка при кристаллизации двухступенчатая: первая ступень – при 700-900 ºС в течение 2 ч; вторая – при 1000-1150 ºС с выдержкой 2-4 ч.
В зависимости от соотношения фаз кристаллизации, одни из которых имеют отрицательный КТР (эвкриптит), другие положительный КТР – сподумен, твердые растворы, образуется ситалл с отрицательным, нулевым или положительным КТР.
Благодаря уникальным тепловым свойствам эти ситаллы находят применение во всех областях техники, где требуется высокая стойкость или полная нечувствительность к тепловому удару и пониженная тепловая деформируемость конструкционных элементов (термостойкие трубы, астрооптика, ракетная техника).
Ситаллы кордиеритового состава относятся к системе MgO–Al2O3–SiO2. По сравнению с сподуменовыми эти ситаллы не содержат дефицитных литийсодержащих компонентов. В качестве катализатора обычно применяют 9-11 % TiO2. Термическая обработка при кристаллизации одноступенчатая: при 1250-1300 ºС с выдержкой 1-16 ч.
В зависимости от состава и режима термообработки в составе кристаллических фаз могут быть кордиерит, шпинель, сапфирин, муллит, рутил, алюмотитанаты магния, твердые растворы на основе –кварца.
Кордиеритовые ситаллы не содержат щелочных компонентов, обладают хорошими диэлектрическими свойствами и отличаются хорошей термостойкостью. Они механически более прочные, чем сподуменовые. Применяют в качестве дешевых, термостойких, прочных диэлектриков в разных конструкциях (изоляторах, закрытых схемах, электронной аппаратуре, бытовой посуде).
Высококремнеземистые ситаллы отличаются необычно высоким тепловым расширением. КТР искусственных материалов не превышает 150·10–7 град–1, эти ситаллы могут иметь КТР 177–136·10–7 град–1. Это позволяет получать согласованные спаи с такими металлами, как медь, серебро, алюминий.
В составы стекол для получения этих ситаллов входят (% по массе): SiO2 85-92; Na2O 7,5-14,5; Al2O3 0-2; F 0-3,6. Катализатором, по-видимому, является щелочной компонент, а фтор выступает в роли плавня, поскольку его присутствие в составах необязательно. Термообработка стекол: 1 ступень – 720 ºС, выдержка 2 ч, 2 ступень – 840-900 ºС, выдержка 1-10 ч.
При термообработке образуются тридимит и кристобалит. Эти фазы, по сравнению с кварцем, который входит в состав исходного стекла, имеют более высокий (в 2-2,5 раза) КТР.
Ситаллы применяют для спаев и в других конструкциях, где требуется высокое тепловое расширение.
Свинецсодержащие ситаллы получены в системе PbO–ZnO–B2O3–SiO2. Типичный состав стекла (%): PbO 75-82, ZnO 7-14, B2O3 12-15, SiO2 1,5-3. Применяют разные катализаторы: P2O5, MoO, WO3 и др.
Режимы кристаллизации варьируются в зависимости от состава, например: 1 ступень – при 500 ºС, выдержка 2 ч, 2 ступень – 700 ºС в течение 1 ч.
Стекла и ситаллы этого типа имеют низкую температуру размягчения (450 ºС) и хорошие диэлектрические свойства, в связи с этим они нашли широкое применение в качестве средств для спаивания и герметизации разных электровакуумных приборов (ситаллоцементы), конденсаторов.
Прозрачные ситаллы. Непременным условием прозрачности ситаллов, которые обычно непрозрачны, является весьма малый размер кристаллов и совпадение или близость показателей преломления кристаллов и стекла. По внешнему виду эти ситаллы сходны с оконным стеклом. Различают ситаллы прозрачные в видимой и в инфракрасной частях спектра.
Ситаллы, прозрачные в видимой части спектра, могут иметь разный состав (сподуменовый, кордиеритовый и др.). Их особенность – потеря прозрачности при нагревании до температуры второй ступени. Выступают в роли заменителей кварцевого стекла.
Ситаллы, прозрачные в инфракрасной части спектра получены на основе кальций-алюминатных стекол. Используются в инфракрасной технике (фотографирование в темноте, измерение температуры нагретых тел на расстоянии, земная и космическая связь).
Фотоситаллы. Получают из светочувствительных стекол. Такие стекла содержат добавки, способные в результате облучения и термообработки вызвать в стекле избирательную или сплошную кристаллизацию. Для получения фоточувствительных стекол пригодны многие силикатные составы, в которые введены небольшие добавки светочувствительных металлов и сенсибилизаторы. К таким стеклам относятся, например, литий-алюмосиликатные, % по массе: SiO2 73,5-80, Al2O3 2-10, Li2O 9-18 с добавкой 0,002 % AgCl (фоточувствительный металл), 0,02 % СеО2 (сенсибилизатор).
Фотоситаллы применяют для получения методом травления различных панелей со сквозными отверстиями и других деталей (метод фотоформ): кристаллическая фаза в них может полностью раствориться в HF за время, в течение которого растворение стекловидной фазы только начинается.
Таким образом, ситаллы, по сравнению с большинством других материалов, обладают благоприятным сочетанием многих важных свойств. Регулируя размеры, плотность и химико-минералогический состав кристаллов, можно получать ситаллы с заранее заданными свойствами, удовлетворяющими специальные требования. Благодаря этому ситаллы находят применение в тех же областях техники, что и заменители стекла и керамики, а в ряде случаев и металлов, полимеров, каменного литья и т. д.
6.3. Ситаллы на основе промышленных отходов и горных пород
К ситаллам этого типа относятся шлако-, золо- и петроситаллы.
Шлаковые ситаллы изготавливают из отходов промышленности с добавлением кварцевого песка и небольшого количества других компонентов. Это один из наиболее радикальных и экономических способов утилизации промышленных отходов, позволяющих получать дешевый конструкционный и строительный материал. Принципиально шлакоситалл не отличается от технических ситаллов, поскольку для получения применяют те же методы. Однако в общей проблеме ситаллов шлакоситаллы занимают особое место, определяемое возможными масштабами производства и дешевизной материала.
Доменные металлургические шлаки образуются в процессе производства чугуна. В шлаках присутствуют: СаО до 48 %, SiO2 до 40 %, Al2O3 до 16 %, MgO до 7 %, MnO до 3 %, Fe2O3 до 1,5 %.
Одной из основных характеристик шлака является его модуль основности (Р). Если Р > 1, шлак считается основным, если Р < 1 – кислым;
Р = (СаО + MgO)/(SiO2 + Al2O3).
Шлаки уральских и сибирских заводов содержат больше кремнезема и глинозема и относятся к группе кислых. Шлаки заводов центра и юга России характеризуются повышенным содержанием кальциевых и магниевых оксидов и относятся к основным.
Известно, что доменные шлаки при отливке склонны к кристаллизации. С целью придания шлаковому расплаву технологических свойств стекломассы состав стекла корректируют введением добавок. Одной из основных добавок является песок, также вводят глину и сульфат натрия для модифицирования свойств стекломассы.
В шихту для получения шлакового стекла вводят, % по массе: доменный шлак 50-65, песок 20-40, глину 0-11, сульфат натрия 4-6, уголь 1-3 и катализаторы 0,5-10.
Шлаковые стекла должны иметь хорошую варочную способность, небольшую склонность к кристаллизации в области температур выработки.
Химический состав шлаковых стекол может находиться в пределах, % по массе: SiO2 49-63; Al2O3 5,4-10,7; СаО 22,9-29,6; MgO 1,3-12; Fe2O3 0,1-10; MnO 1-3,5; Na2O 2,6-5 и Cr2O3 0,1-2.
При использовании катализаторов MnS + FeS шлакоситалл получается серовато-черного цвета. Для получения белого цвета в стекло вводят ZnO, который взаимодействует с сульфидами тяжелых металлов, имеющими темный цвет, с образованием сульфида цинка белого цвета. Такому отбеленному шлакоситаллу может быть придан любой цвет при дополнительном введении одного из красителей.
Производство шлакоситаллов включает два основных этапа:
- получение стекла на основе шлаков и изготовление из него изделий;
- термическую обработку изделий, приводящую к кристаллизации стекла и переходу его в стеклокристаллический материал.
При получении шлакоситалла оптимальным является двухступенчатый режим термообработки.
По своей структуре шлакоситаллы представляют собой материал, состоящий на 60-70 % из кристаллической фазы, отдельные зерна которой окружены и скреплены прослойкой остаточного стекла. Размер кристаллов не превышает 0,5-1 мкм. Весьма малый размер кристаллов, сравнительно небольшое различие КТР и плотностей кристаллической и стекловидной фаз, хорошее сцепление кристаллов со стекловидной связкой обеспечивают повышенные прочностные и антикоррозионные свойства шлакоситаллов.
Шлакоситалл по термостойкости значительно превосходит стекло и каменное литье, керамику и может быть использован для изготовления изделий санитарно-технического назначения.
Достаточно высокая стойкость шлакоситаллов против истирания позволяет применять его для футеровки различных камер, путеводов, желобов и других объектов, работающих на истирание.
Высокая химическая стойкость, по сравнению со многими традиционными строительными материалами, позволяет изготавливать из шлакоситаллов футеровку емкостей с кислотами, трубы и изделия для хранения и транспортирования агрессивных, горячих жидкостей.
Шлакоситалл используется для покрытия полов, облицовки стен бытовых и цеховых помещений, сооружения кровель, лестничных маршей, изготовления кухонных раковин.
Благодаря диэлектрическим и эксплуатационным свойствам шлакоситалл используют в электротехнической промышленности для изготовления изоляторов.
Золоситаллы. На тепловых электростанциях, сжигающих твердое топливо в пылевидном состоянии, образуются отходы. При сухом удалении отходов – зола, при удалении расплава отходов – шлак. За многие годы работы ТЭЦ в отвалах накоплено более 100 млн т золошлаков. Золоотвалы являются источником интенсивного пылеобразования и делают непригодными для использования большие земельные площади. Единственным средством избавления от топливных отходов является переработка их в строительные и конструкционные материалы.
Топливные золы и шлаки различаются между собой в зависимости от вида топлива и способа его сжигания.
Большинство топливных шлаков относятся к кислым и отличаются от металлургических тем, что содержат некоторое количество щелочей (до 4 %), большое количество оксидов железа (до 20 %). По химическому составу топливные золы и шлаки близки к составам малощелочных высокоглиноземистых железосодержащих силикатных стекол.
В зависимости от химического состава золы и шлака производится корректировка исходной смеси разными добавками (песок, доломит и др.).
Петроситаллы получают на основе различных горных пород – изверженных (базальт, диабаз, гранит, нефелиновый сиенит и др.), осадочных (пески, глины, мергели, каолины и др.), метаморфических (гнейсы, сланцы, мраморы, серпентиниты).
Химический состав базальта, мас. %: SiO2 – 48,4; Al2O3 – 14,5; СаО – 9,4; MgO – 5,8; Fe2O3 – 6,1; FeO – 10; TiO2 – 2,6; MnO – 0,2; Na2O – 2,5; K2O – 0,5. В качестве катализатора наилучшие результаты получены с добавкой 2-4 % CaF2.
Петроситаллы имеют более высокие свойства, чем заводское каменное литье, обладают меньшей пористостью, более мелкозернистой структурой и повышенной механической прочностью, а также более устойчивы к воздействию кислот и щелочей.
Это связано с более мелкозернистой структурой петроситаллов, поэтому они содержат меньше дефектов, чем крупные кристаллы обычного каменного литья. Кроме того, остаточная стеклофаза в петроситаллах имеет более высокий температурный КТР, чем в базальтовом литье. В результате внутренние напряжения в материале уменьшаются и повышается прочность.
Задание 6
- Выполнить задания для самоконтроля
Вопросы и задания для самоконтроля
- Чем отличаются ситаллы от стекла и керамики?
- Какова роль катализатора в процессе синтеза ситаллов?
- Какие требования предъявляются к катализаторам?
- Назовите основные типы технических ситаллов.
- Дайте названия группам катализаторов:
1) (As2O3 + MoO3), (TiO2 + MeF2), (AgCl + SnO2);
2) Cr2O3, ZrO2, ZnO, SnO2, WO3, MoO3, TiO2, P2O5;
3) Сu, Ag, Au, Si, Pt.
- Пронумеруйте в правильной последовательности основные технологические этапы производства ситаллов: формование;
получение шихты;
варка стекла;
кристаллизация.
- Как зависит структура ситалла от температурно-временного режима кристаллизации? Проанализируйте рис. 6.1.
- Назовите ведущее свойство для следующих ситаллов:
1) сподуменовых;
2) кордиеритовых;
3) высококремнеземистых;
4) свинецсодержащих.
- Чем отличаются технические ситаллы от ситаллов на основе промышленных отходов?
|
|
|
© helpiks.su При использовании или копировании материалов прямая ссылка на сайт обязательна.
|