
- Автоматизация
- Антропология
- Археология
- Архитектура
- Биология
- Ботаника
- Бухгалтерия
- Военная наука
- Генетика
- География
- Геология
- Демография
- Деревообработка
- Журналистика
- Зоология
- Изобретательство
- Информатика
- Искусство
- История
- Кинематография
- Компьютеризация
- Косметика
- Кулинария
- Культура
- Лексикология
- Лингвистика
- Литература
- Логика
- Маркетинг
- Математика
- Материаловедение
- Медицина
- Менеджмент
- Металлургия
- Метрология
- Механика
- Музыка
- Науковедение
- Образование
- Охрана Труда
- Педагогика
- Полиграфия
- Политология
- Право
- Предпринимательство
- Приборостроение
- Программирование
- Производство
- Промышленность
- Психология
- Радиосвязь
- Религия
- Риторика
- Социология
- Спорт
- Стандартизация
- Статистика
- Строительство
- Технологии
- Торговля
- Транспорт
- Фармакология
- Физика
- Физиология
- Философия
- Финансы
- Химия
- Хозяйство
- Черчение
- Экология
- Экономика
- Электроника
- Электротехника
- Энергетика
Массовая доля растворенного вещества.
Массовая доля растворенного вещества.
Существуют различные способы выражения концентрации растворённого вещества в растворе, мы познакомимся с массовой долей растворённого вещества (процентной концентрацией).
I. Массовая доля растворённого вещества wрастворённого вещества- это безразмерная величина, равная отношению массы растворённого вещества mрастворённого вещества к общей массе раствора mраствора :
mраствора = mрастворённого вещества + mрастворителя
Массовую долю растворённого вещества(процентная концентрация) обычно выражают в долях единицы или в процентах. Например, массовая доля растворённого вещества – CaCl2 в воде равна 0,06 или 6%. Это означает, что в растворе хлорида кальция массой 100 г содержится хлорид кальция массой 6 г и вода массой 94 г.
Массовая доля растворённого вещества в растворе – это отношение массы растворённого вещества к массе всего раствора.
Не забывайте, что масса раствора складывается из массы растворителя и растворённого вещества. Сразу разберём пример, чтобы стало понятно.
Пример 1.
У нас есть 200 г воды и 10 г сахара. Смешиваем воду и сахар и получаем раствор. Так вот масса раствора будет равна массе воды (здесь это растворитель) и сахара (растворённое вещество), то есть 200+10=210 г. Это очень важно, не упускайте этот момент из виду.
Теперь возвратимся к массовой доле. Она обозначается латинской буквой w и рассчитывается по простой формуле:
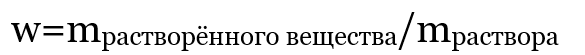
При этом помните, что

Удобнее выражать массовую долю в процентах, поэтому чаще используется такая формула:
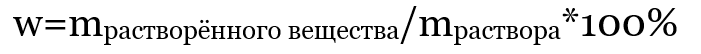
|
|
|
© helpiks.su При использовании или копировании материалов прямая ссылка на сайт обязательна.
|