
- Автоматизация
- Антропология
- Археология
- Архитектура
- Биология
- Ботаника
- Бухгалтерия
- Военная наука
- Генетика
- География
- Геология
- Демография
- Деревообработка
- Журналистика
- Зоология
- Изобретательство
- Информатика
- Искусство
- История
- Кинематография
- Компьютеризация
- Косметика
- Кулинария
- Культура
- Лексикология
- Лингвистика
- Литература
- Логика
- Маркетинг
- Математика
- Материаловедение
- Медицина
- Менеджмент
- Металлургия
- Метрология
- Механика
- Музыка
- Науковедение
- Образование
- Охрана Труда
- Педагогика
- Полиграфия
- Политология
- Право
- Предпринимательство
- Приборостроение
- Программирование
- Производство
- Промышленность
- Психология
- Радиосвязь
- Религия
- Риторика
- Социология
- Спорт
- Стандартизация
- Статистика
- Строительство
- Технологии
- Торговля
- Транспорт
- Фармакология
- Физика
- Физиология
- Философия
- Финансы
- Химия
- Хозяйство
- Черчение
- Экология
- Экономика
- Электроника
- Электротехника
- Энергетика
Практическая работа № 1 по теме: «Первый закон термодинамики»
Практическая работа № 1 по теме: «Первый закон термодинамики»
Цель работы: Научиться находить внутреннюю энергию, теплоту, работу идеального газа в разных процессах
Методические указания к выполнению работы:
1 закон термодинамики: q = Δu + ℓ.
В таблице приведены формулы для расчета процессов.
| Процесс | Связь Параметров | Работа изменения объема | Теплота |
| Изохорный | p2/p1 = T2/T1 | ℓ = 0 | q = cv (T2-T1) |
| Изобарный | v2/v1 = T2/T1 | ℓ = p (v2 -v1) | q = cp (T2-T1) |
| Изотермический | p2/p1 = v1/v2 | ℓ =RT ln (v2/v1) ℓ =RT ln (p1/p2) | q = ℓ |
| Адиабатный | р2/ р1 = (v1/v2)k T2/T1 = (v1/v2)k-1 T2/T1 = (р2/р1)(k-1)/k | 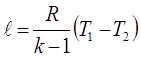
| q = 0 |
| Политропный | р2/ р1 = (v1/v2)n T2/T1 = (v1/v2)n-1 T2/T1 = (р2/р1)(n-1)/n | 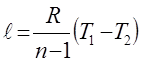
| 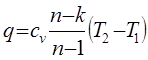
|
Изменение внутренней энергии идеального газа в термодинамическом процессе: Δu = cv∙(T2-Т1).
Изменение энтальпии идеального газа в термодинамическом процессе: Δh = cp∙(T2-Т1).
Ход работы:
Решить задачу 1 своего варианта. Время выполнения: 30 минут.
Задача №1
Газ объемом v1 , находящийся под давлением р1 при температуре t1 в результате осуществления термодинамического процесса расширяется до конечного объема v2.
Найти конечное давление, конечную температуру, работу произведенную газом, тепло и изменение внутренней энергии, если расширение происходит по одному из термодинамических процессов, указанных в таблице.
При решении вариантов задачи, где встречается политропный процесс, следует принять показатель политропы 1,3. Для вариантов, где дан адиабатный процесс, принять показатель адиабаты 1,4.
| Номер варианта | Вид газа | Вид процесса | V1 м³ | Р1 МПа | T1ºC | V2 м³ |
| Азот | Изобарный | 0,15 | 1,5 | 0,5 | ||
| Оксид углерода | Изотермический | 0,2 | 0,6 | |||
| Диоксид серы | Адиабатный | 0,25 | 2,5 | 0,7 | ||
| Диоксид углерода | политропный | 0,3 | 0,8 | |||
| Кислород | изобарный | 0,35 | 3,5 | 0,9 | ||
| Азот | Изобарный | 0,4 | ||||
| Оксид углерода | Изотермический | 0,45 | 4,5 | 1,1 | ||
| Диоксид серы | Адиабатный | 0,5 | 1,2 | |||
| Диоксид углерода | политропный | 0,55 | 5,5 | 1,3 | ||
| Кислород | изобарный | 0,6 | 1,4 | |||
| Азот | изохорный | 0,65 | 6,5 | 1,5 | ||
| Оксид углерода | Изобарный | 0,7 | 1,1 | 1,6 | ||
| Диоксид серы | Изотермический | 0,75 | 1.2 | 1,7 | ||
| Диоксид углерода | Адиабатный | 0,8 | 1,3 | 1,8 | ||
| Кислород | политропный | 0,85 | 1,4 | 1,9 | ||
| Азот | изобарный | 0,9 | 1,5 | |||
| Оксид углерода | Изобарный | 1,6 | 2,1 | |||
| Диоксид серы | Изотермический | 1,1 | 1,7 | 2,2 | ||
| Диоксид углерода | Адиабатный | 1,2 | 1,8 | 2,3 | ||
| Кислород | Политропный | 1,25 | 1,9 | 2,4 |
|
|
|
© helpiks.su При использовании или копировании материалов прямая ссылка на сайт обязательна.
|