
- Автоматизация
- Антропология
- Археология
- Архитектура
- Биология
- Ботаника
- Бухгалтерия
- Военная наука
- Генетика
- География
- Геология
- Демография
- Деревообработка
- Журналистика
- Зоология
- Изобретательство
- Информатика
- Искусство
- История
- Кинематография
- Компьютеризация
- Косметика
- Кулинария
- Культура
- Лексикология
- Лингвистика
- Литература
- Логика
- Маркетинг
- Математика
- Материаловедение
- Медицина
- Менеджмент
- Металлургия
- Метрология
- Механика
- Музыка
- Науковедение
- Образование
- Охрана Труда
- Педагогика
- Полиграфия
- Политология
- Право
- Предпринимательство
- Приборостроение
- Программирование
- Производство
- Промышленность
- Психология
- Радиосвязь
- Религия
- Риторика
- Социология
- Спорт
- Стандартизация
- Статистика
- Строительство
- Технологии
- Торговля
- Транспорт
- Фармакология
- Физика
- Физиология
- Философия
- Финансы
- Химия
- Хозяйство
- Черчение
- Экология
- Экономика
- Электроника
- Электротехника
- Энергетика
Разбор первой задачи. Задача 1. Определите, какое количество молекул содержится в 120 г воды.
Разбор первой задачи
Задача 1. Определите, какое количество молекул содержится в 120 г воды.
Это задача на количество молекул некой порции вещества, и поэтому для её решения существует два пути: решение через количество вещества воды и решение через массу молекулы. Следует отметить, что конечную формулу в обоих случаях мы получим одну и ту же, просто придём к ней по-разному.
Наметим себе план решения задачи.
1 Способ:
Для решения задачи первым действием мы найдём количество вещества данной массы воды. И вторым действием, зная, сколько молекул помещается в 1 моль вещества (число Авогадро - 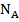 ) и, зная количество молей в нашей порции воды (количество вещества –
) и, зная количество молей в нашей порции воды (количество вещества – 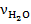 ), мы найдём количество молекул в 120 г воды.
), мы найдём количество молекул в 120 г воды.
2 Способ:
Теперь же первым действием мы найдём массу одной молекулы воды. А вторым действием, зная массу всей порции и массу одной молекулы, найдём опять-таки количество всех молекул.
Независимо от того, каким способом мы решили искать ответ к задаче, нам понадобится молярная масса воды – 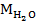 . Она нужна как для нахождения количества вещества:
. Она нужна как для нахождения количества вещества:
 ,
,
так и для нахождения массы одной молекулы
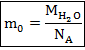
Найдём молярную массу воды. Молярная масса – аддитивная величина, то есть молярная масса сложного вещества – сумма молярных масс химических элементов, входящих в его состав. Не стоит также забывать, что в таблице Менделеева, а именно из нее мы берём значение молярных масс элементов, молярная масса подана в 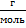 , так что нам нужно ещё перевести ее в СИ, то есть в
, так что нам нужно ещё перевести ее в СИ, то есть в 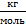 .
.

Теперь, когда мы нашли общую нужную величину для обоих способов решения, получим ответ. И точно также не забудем перевести г в кг, умножая на 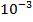 .
.
Способ 1:
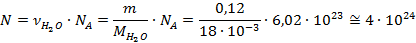
Способ 2:
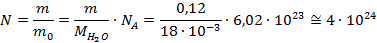
Как и говорилось выше, оба способа решения отличаются лишь тем, как они начинаются. Стоит ещё заметить, что количество молекул, как и любое другое количество, – безразмерная величина.
Разбор второй задачи
Перейдём к следующей задаче.
Задача 2:
Определить скорость движения частиц воздуха при нормальных условиях.
Прежде чем начинать записывать какие-либо формулы, нам нужно уяснить два момента, фигурирующие в условии задачи. Первое – это то, что мы считаем воздух, который является смесью газов, неким псевдогазом с собственными молекулами. И второе – это то, что условие здесь нам подаётся в виде словосочетания «нормальные условия». Значения величин, которые будут нужны нам для подсчётов, мы возьмём из табличных данных: давление при нормальных условиях равно атмосферному давлению и обозначается 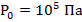 , плотность воздуха при нормальных условиях
, плотность воздуха при нормальных условиях 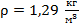 .
.
Эту задачу следует решать, используя основное уравнение МКТ:
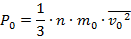
Или же, воспользовавшись одной из формул прошлого урока:
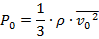
Отсюда:
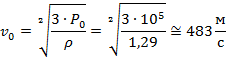
Разбор третьей задачи
Перейдём к третьей задаче.
Задача 3
В ёмкости объёмом 1 л находится газ массой 5 г, частицы которого двигаются со скоростью 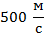 .
.
Определить давление этого газа.
Эта задача также является задачей на основное уравнение МКТ, поэтому её решение начинается точно так же, как и решение предыдущей задачи:
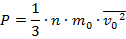
Или же, воспользовавшись одной из формул прошлого урока:
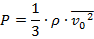
Однако теперь мы столкнулись с дополнительной сложностью, ведь мы не знаем, что за газ находится в сосуде, поэтому не можем воспользоваться табличными данными. Зато мы можем вспомнить определение плотности (масса единицы объёма) и в связи с этим записать
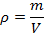
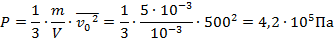
При подстановке данных мы не забыли перевести г в кг, а также л в 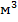 , учитывая, что
, учитывая, что 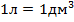 .
.
На следующем занятии мы подробнее остановимся на таком макропараметре идеального газа, как температура.
|
|
|
© helpiks.su При использовании или копировании материалов прямая ссылка на сайт обязательна.
|