
- Автоматизация
- Антропология
- Археология
- Архитектура
- Биология
- Ботаника
- Бухгалтерия
- Военная наука
- Генетика
- География
- Геология
- Демография
- Деревообработка
- Журналистика
- Зоология
- Изобретательство
- Информатика
- Искусство
- История
- Кинематография
- Компьютеризация
- Косметика
- Кулинария
- Культура
- Лексикология
- Лингвистика
- Литература
- Логика
- Маркетинг
- Математика
- Материаловедение
- Медицина
- Менеджмент
- Металлургия
- Метрология
- Механика
- Музыка
- Науковедение
- Образование
- Охрана Труда
- Педагогика
- Полиграфия
- Политология
- Право
- Предпринимательство
- Приборостроение
- Программирование
- Производство
- Промышленность
- Психология
- Радиосвязь
- Религия
- Риторика
- Социология
- Спорт
- Стандартизация
- Статистика
- Строительство
- Технологии
- Торговля
- Транспорт
- Фармакология
- Физика
- Физиология
- Философия
- Финансы
- Химия
- Хозяйство
- Черчение
- Экология
- Экономика
- Электроника
- Электротехника
- Энергетика
Уравнение состояния идеального газа. Уравнений Клайперона-Менделеева
1. Уравнение состояния идеального газа. Уравнений Клайперона-Менделеева
pV = 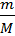 RT
RT
R = 8,31 Дж/(моль*К) – универсальная постоянная
2. Газовые законы
1) Закон Гей-Люссака
m = const
p=const
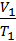 =
= 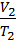 =const
=const

 V
V
изобара

Т
 Р
Р
 изобара
изобара
 |
Т


 Р
Р
изобара
Т
2) Объединенный газовый закон
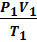 =
= 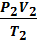 =const
=const
3) Закон Бойля-Мариотта
m = const
T = const
P1V1 = P2V2 = const
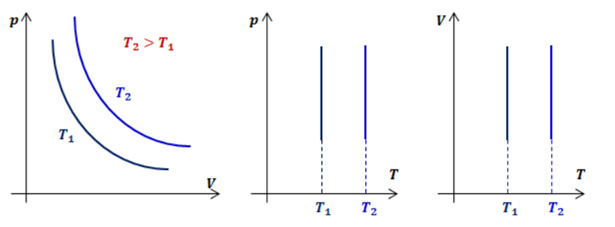
изотерма и и
з з
о о
т т
е е
р р
м м
а а
4) Закон Шарля
m = const
V = const
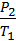 =
= 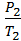 = const
= const

 P
P
изохора
 T
T

 P
P
И
З
О
Х
О
Р
А
 V
V
 V
V
 |
И
З
О
Х
О
Р
A
 T
T
5) Закон Дальтона
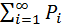 = P1+P2 + P3 …
= P1+P2 + P3 …
Задания:
1) Уравнение Клапейрона: pV/T = const. Уравнение Клапейрона-Менделеева: pV/T = m/u*R. Вторая форма уточняет струкутуру константы, следовательно, содержит больше информации.
2) R – универсальная газовая постоянная – объем одного моля любого газа при нормальных условиях. В этом состоит физический смысл универсальной газовой постоянной
3) Изотермический процесс - сжатие или расширение газа при неизменной температуре.
Изобарный процесс - нагрев газа в сосуде при фиксированном давлении поршня.
Изохорный процесс - эксперименты с газом в любом закрытом сосуде.
4) Равновесное состояние газа - это состояние, при котором температура и давление во всех точках объема одинаковы.
|
|
|
© helpiks.su При использовании или копировании материалов прямая ссылка на сайт обязательна.
|