| № 15 Методы микроскопии (люминесцентная, темнопольная, фазово-контрастная, электронная).
Люминесцентная (или флюоресцентная) микроскопия.Основана на явлении фотолюминесценции.
Люминесценция — свечение веществ, возникающее после воздействия на них каких-либо источников энергии: световых, электронных лучей, ионизирующего излучения. Фотолюминесценция — люминесценция объекта под влиянием света. Если освещать люминесцирующий объект синим светом, то он испускает лучи красного, оранжевого, желтого или зеленого цвета. В результате возникает цветное изображение объекта.
Темнопольная микроскопия.Микроскопия в темном поле зрения основана на явлении дифракции света при сильном боковом освещении взвешенных в жидкости мельчайших частиц (эффект Тиндаля). Эффект достигается с помощью параболоид- или кардиоидконденсора, которые заменяют обычный конденсор в биологическом микроскопе .
Фазово-контрастная микроскопия. Фазово-контрастное приспособление дает возможность увидеть в микроскоп прозрачные объекты. Они приобретают высокую контрастность изображения, которая может быть позитивной или негативной. Позитивным фазовым контрастом называют темное изображение объекта в светлом поле зрения, негативным — светлое изображение объекта на темном фоне.
Для фазово-контрастной микроскопии используют обычный микроскоп и дополнительное фазово-контрастное устройство, а также специальные осветители.
Электронная микроскопия.Позволяет наблюдать объекты, размеры которых лежат за пределами разрешающей способности светового микроскопа (0,2 мкм). Электронный микроскоп применяется для изучения вирусов, тонкого строения различных микроорганизмов, макромолекулярных структур и других субмикроскопических объектов.
|
№ 16 Рост и размножение бактерий. Фазы размножения.
Жизнедеятельность бактерий характеризуется ростом — формированием структурно-функциональных компонентов клетки и увеличением самой бактериальной клетки, а также размножением — самовоспроизведением, приводящим к увеличению количества бактериальных клеток в популяции.
Бактерии размножаются путем бинарного деления пополам, реже путем почкования. Актиномицеты, как и грибы, могут размножаться спорами. Актиномицеты, являясь ветвящимися бактериями, размножаются путем фрагментации нитевидных клеток. Грамположительные бактерии делятся путем врастания синтезирующихся перегородок деления внутрь клетки, а грамотрицательные — путем перетяжки, в результате образования гантелевид-ных фигур, из которых образуются две одинаковые клетки.
Делению клеток предшествует репликация бактериальной хромосомы по полуконсервативному типу (двуспиральная цепь ДНК раскрывается и каждая нить достраивается комплементарной нитью), приводящая к удвоению молекул ДНК бактериального ядра — нуклеоида.
Репликация ДНК происходит в три этапа: инициация, элонгация, или рост цепи, и терминация.
Размножение бактерий в жидкой питательной среде.Бактерии, засеянные в определенный, не изменяющийся объем питательной среды, размножаясь, потребляют питательные элементы, что приводит в дальнейшем к истощению питательной среды и прекращению роста бактерий. Культивирование бактерий в такой системе называют периодическим культивированием, а культуру — периодической. Если же условия культивирования поддерживаются путем непрерывной подачи свежей питательной среды и оттока такого же объема культуральной жидкости, то такое культивирование называется непрерывным, а культура — непрерывной.
При выращивании бактерий на жидкой питательной среде наблюдается придонный, диффузный или поверхностный (в виде пленки) рост культуры. Рост периодической культуры бактерий, выращиваемых на жидкой питательной среде, подразделяют на несколько фаз, или периодов:
1.лаг-фаза;
2.фаза логарифмического роста;
3.фаза стационарного роста, или максимальной концентрации
бактерий;
4.фаза гибели бактерий.
Эти фазы можно изобразить графически в виде отрезков кривой размножения бактерий, отражающей зависимость логарифма числа живых клеток от времени их культивирования.
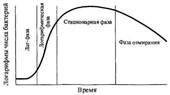
Лаг-фаза — период между посевом бактерий и началом размножения. Продолжительность лаг-фазы в среднем 4—5 ч. Бактерии при этом увеличиваются в размерах и готовятся к делению; нарастает количество нуклеиновых кислот, белка и других компонентов.
Фаза логарифмического (экспоненциального) роста является периодом интенсивного деления бактерий. Продолжительность ее около 5— 6 ч. При оптимальных условиях роста бактерии могут делиться каждые 20—40 мин. Во время этой фазы бактерии наиболее ранимы, что объясняется высокой чувствительностью компонентов метаболизма интенсивно растущей клетки к ингибиторам синтеза белка, нуклеиновых кислот и др.
Затем наступает фаза стационарного роста, при которой количество жизнеспособных клеток остается без изменений, составляя максимальный уровень (М-концентрация). Ее продолжительность выражается в часах и колеблется в зависимости от вида бактерий, их особенностей и культивирования.
Завершает процесс роста бактерий фаза гибели, характеризующаяся отмиранием бактерий в условиях истощения источников питательной среды и накопления в ней продуктов метаболизма бактерий. Продолжительность ее колеблется от 10 ч до нескольких недель. Интенсивность роста и размножения бактерий зависит от многих факторов, в том числе оптимального состава питательной среды, окислительно-восстановительного потенциала, рН, температуры и др.
Размножение бактерий на плотной питательной среде.Бактерии, растущие на плотных питательных средах, образуют изолированные колонии округлой формы с ровными или неровными краями (S- и R-формы), различной консистенции и цвета, зависящего от пигмента бактерий.
Пигменты, растворимые в воде, диффундируют в питательную среду и окрашивают её. Другая группа пигментов нерастворима в воде, но растворима в органических растворителях. И, наконец, существуют пигменты, не растворимые ни в воде, ни в органических соединениях.
Наиболее распространены среди микроорганизмов такие пигменты, как каротины, ксантофиллы и меланины. Меланины являются нерастворимыми пигментами черного, коричневого или красного цвета, синтезирующимися из фенольных соединений. Меланины наряду с каталазой, супероксидцисмутазой и пероксидазами защищают микроорганизмы от воздействия токсичных перекисных радикалов кислорода. Многие пигменты обладают антимикробным, антибиотикоподобным действием.
|
№ 17 Способы получения энергии бактериями (дыхание, брожение). Методы культивирования анаэробов.
Дыхание, или биологическое окисление, основано на окислительно-восстановительных реакциях, идущих с образованием АТФ-универсального аккумулятора химической энергии. Энергия необходима микробной клетке для ее жизнедеятельности. При дыхании происходят процессы окисления и восстановления: окисление — отдача донорами (молекулами или атомами) водорода или электронов; восстановление — присоединение водорода или электронов к акцептору. Акцептором водорода или электронов может быть молекулярный кислород (такое дыхание называется аэробным) или нитрат, сульфат, фумарат (такое дыхание называется анаэробным — нитратным, сульфатным, фумаратным).
Анаэробиоз (от греч. аег — воздух + bios — жизнь) — жизнедеятельность, протекающая при отсутствии свободного кислорода. Если донорами и акцепторами водорода являются органические соединения, то такой процесс называется брожением. При брожении происходит ферментативное расщепление органических соединений, преимущественно углеводов, в анаэробных условиях. С учетом конечного продукта расщепления углеводов различают спиртовое, молочнокислое, уксуснокислое и другие виды брожения.
По отношению к молекулярному кислороду бактерии можно разделить на три основные группы: облигатные, т.е. обязательные, аэробы, облигатные анаэробы и факультативные анаэробы.
Методы культивирования анаэробов.
Для культивирования анаэробов необходимо понизить окислительно-восстановительный потенциал среды, создать условия анаэробиоза, т. е. пониженного содержания кислорода в среде и окружающем ее пространстве. Это достигается применением физических, химических и биологических методов.
Физические методы.Основаны на выращивании микроорганизмов в безвоздушной среде, что достигается:
1) посевом в среды, содержащие редуцирующие и легко окисляемые вещества;
2) посевом микроорганизмов в глубину плотных питательных сред;
3) механическим удалением воздуха из сосудов, в которых выращиваются анаэробные микроорганизмы;
4) заменой воздуха в сосудах каким-либо индифферентным газом.
В качестве редуцирующих веществ обычно используют кусочки (около 0,5 г) животных или растительных тканей (печень, мозг, почки, селезенка, кровь, картофель, вата). Эти ткани связывают растворенный в среде кислород и адсорбируют бактерии. Чтобы уменьшить содержание кислорода в питательной среде, ее перед посевом кипятят 10—15 мин, а затем быстро охлаждают и заливают сверху небольшим количеством стерильного вазелинового масла. Высота слоя масла в пробирке около 1 см.
В качестве легко окисляемых веществ используют глюкозу, лактозу и муравьинокислый натрий.
Лучшей жидкой питательной средой с редуцирующими веществами является среда Китта — Тароцци, которая используется с успехом для накопления анаэробов при первичном посеве из исследуемого материала и для поддержания роста выделенной чистой культуры анаэробов.
Посев микроорганизмов в глубину плотных сред производят по способу Виньяль — Вейона, который состоит в механической защите посевов анаэробов от кислорода воздуха. Берут стеклянную трубку длиной 30 см и диаметром 3—6 мм. Один конец трубки вытягивают в капилляр в виде пастеровской пипетки, а у другого конца делают перетяжку. В оставшийся широкий конец трубки вставляют ватную пробку. В пробирки с расплавленным и охлажденным до 50°С питательным агаром засевают исследуемый материал. Затем насасывают засеянный агар в стерильные трубки Виньяль — Вейона. Капиллярный конец трубки запаивают в пламени горелки и трубки помещают в термостат. Так создаются благоприятные условия для роста самых строгих анаэробов. Для выделения отдельной колонии трубку надрезают напильником, соблюдая правила асептики, на уровне колонии, ломают, а колонию захватывают стерильной петлей и переносят в пробирку с питательной средой для дальнейшего выращивания и изучения в чистом виде.
Удаление воздуха производят путем его механического откачивания из специальных приборов — анаэроста-тов, в которые помещают чашки с посевом анаэробов. Переносный анаэростат представляет собой толстостенный металлический цилиндр с хорошо притертой крышкой (с резиновой прокладкой), снабженный отводящим краном и вакуумметром. После размещения засеянных чашек или пробирок воздух из анаэростата удаляют с помощью вакуумного насоса.
Замену воздуха индифферентным газом (азотом, водородом, аргоном, углекислым газом) можно производить в тех же анаэростатах путем вытеснения его газом из баллона.
Химические методы.Основаны на поглощении кислорода воздуха в герметически закрытом сосуде (анаэро-стате, эксикаторе) такими веществами, как пирогаллол или гидросульфит натрия Na2S204.
Биологические методы.Основаны на совместном выращивании анаэробов со строгими аэробами. Для этого из застывшей агаровой пластинки по диаметру чашки вырезают стерильным скальпелем полоску агара шириной около 1 см. Получается два агаровых полудиска в одной чашке. На одну сторону агаровой пластинки засевают аэроб, например часто используют S. aureus или Serratia marcescens. На другую сторону засевают анаэроб. Края чашки заклеивают пластилином или заливают расплавленным парафином и помещают в термостат. При наличии подходящих условий в чашке начнут размножаться аэробы. После того, как весь кислород в пространстве чашки будет ими использован, начнется рост анаэробов (через 3—4 сут). В целях сокращения воздушного пространства в чашке питательную среду наливают возможно более толстым слоем.
Комбинированные методы.Основаны на сочетании физических, химических и биологических методов создания анаэробиоза.
| |
|
№ 18 Типы и механизмы питания бактерий.
Типы питания.Микроорганизмы нуждаются в углеводе, азоте, сере, фосфоре, калии и других элементах. В зависимости от источников углерода для питания бактерии делятся на аутотрофы, использующие для построения своих клеток диоксид углерода С02 и другие неорганические соединения, и гетеротрофы, питающиеся за счет готовых органических соединений. Аутотрофными бактериями являются нитрифицирующие бактерии, находящиеся в почве; серобактерии, обитающие в воде с сероводородом; железобактерии, живущие в воде с закисным железом, и др.
Гетеротрофы, утилизирующие органические остатки отмерших организмов в окружающей среде, называются сапрофитами. Гетеротрофы, вызывающие заболевания у человека или животных, относят к патогенным и условно-патогенным. Среди патогенных микроорганизмов встречаются облигатные и факультативные паразиты (от греч. parasitos — нахлебник). Облигатные паразиты способны существовать только внутри клетки, например риккетсии, вирусы и некоторые простейшие.
В зависимости от окисляемого субстрата, называемого донором электронов или водорода, микроорганизмы делят на две группы. Микроорганизмы, использующие в качестве доноров водорода неорганические соединения, называют литотрофны-ми (от греч. lithos — камень), а микроорганизмы, использующие в качестве доноров водорода органические соединения, — органотрофами.
Учитывая источник энергии, среди бактерий различают фототрофы, т.е. фотосинтезирующие (например, сине-зеленые водоросли, использующие энергию света), и хемотрофы, нуждающиеся в химических источниках энергии.
Механизмы питания.Поступление различных веществ в бактериальную клетку зависит от величины и растворимости их молекул в липидах или воде, рН среды, концентрации веществ, различных факторов проницаемости мембран и др. Клеточная стенка пропускает небольшие молекулы и ионы, задерживая макромолекулы массой более 600 Д. Основным регулятором поступления веществ в клетку является цитоплазматическая мембрана. Условно можно выделить четыре механизма проникновения питательных веществ в бактериальную клетку: это простая диффузия, облегченная диффузия, активный транспорт, транслокация групп.
Наиболее простой механизм поступления веществ в клетку — простая диффузия, при которой перемещение веществ происходит вследствие разницы их концентрации по обе стороны цитоплазматической мембраны. Вещества проходят через липид-ную часть цитоплазматической мембраны (органические молекулы, лекарственные препараты) и реже по заполненным водой каналам в цитоплазматической мембране. Пассивная диффузия осуществляется без затраты энергии.
Облегченная диффузия происходит также в результате разницы концентрации веществ по обе стороны цитоплазматической мембраны. Однако этот процесс осуществляется с помощью молекул-переносчиков, локализующихся в цитоплазматической мембране и обладающих специфичностью. Каждый переносчик транспортирует через мембрану соответствующее вещество или передает другому компоненту цитоплазматической мембраны — собственно переносчику. Белками-переносчиками могут быть пермеазы, место синтеза которых — цитоплазматическая мембрана. Облегченная диффузия протекает без затраты энергии, вещества перемещаются от более высокой концентрации к более низкой.
Активный транспорт происходит с помощью пермеаз и направлен на перенос веществ от меньшей концентрации в сторону большей, т.е. как бы против течения, поэтому данный про цесс сопровождается затратой метаболической энергии (АТФ), образующейся в результате окислительно-восстановительных реакций в клетке.
Перенос (транслокация) групп сходен с активным транспортом, отличаясь тем, что переносимая молекула видоизменяется в процессе переноса, например фосфорилируется.
Выход веществ из клетки осуществляется за счет диффузии и при участии транспортных систем.
| |

