
- Автоматизация
- Антропология
- Археология
- Архитектура
- Биология
- Ботаника
- Бухгалтерия
- Военная наука
- Генетика
- География
- Геология
- Демография
- Деревообработка
- Журналистика
- Зоология
- Изобретательство
- Информатика
- Искусство
- История
- Кинематография
- Компьютеризация
- Косметика
- Кулинария
- Культура
- Лексикология
- Лингвистика
- Литература
- Логика
- Маркетинг
- Математика
- Материаловедение
- Медицина
- Менеджмент
- Металлургия
- Метрология
- Механика
- Музыка
- Науковедение
- Образование
- Охрана Труда
- Педагогика
- Полиграфия
- Политология
- Право
- Предпринимательство
- Приборостроение
- Программирование
- Производство
- Промышленность
- Психология
- Радиосвязь
- Религия
- Риторика
- Социология
- Спорт
- Стандартизация
- Статистика
- Строительство
- Технологии
- Торговля
- Транспорт
- Фармакология
- Физика
- Физиология
- Философия
- Финансы
- Химия
- Хозяйство
- Черчение
- Экология
- Экономика
- Электроника
- Электротехника
- Энергетика
ОК – 8 Газовые законы.
ОК – 8 Газовые законы.
Идеальный газ – это модель реального газа, описывающая процессы, происходящие в нём, движение и взаимодействие частиц.
- молекулы, абсолютно упругие тела, имеющие форму шара.
- молекулы принимаются за материальные точки.
- силы притяжения между молекулами – отсутствуют, а силы отталкивания возникают только в момент соударения.
- газ сжимаем до плотной упаковки.
- молекулы в пространстве распределены равномерно
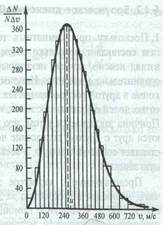
- большинство молекул, имеют какую- то среднюю скорость.(Отто Штерн 1920 ).
 [p] = [Па]
газ оказывает суммарное воздействие на стенки сосуда,
. т.е. оказывает давление.
давление зависит:
- от концентрации частиц; n =
[p] = [Па]
газ оказывает суммарное воздействие на стенки сосуда,
. т.е. оказывает давление.
давление зависит:
- от концентрации частиц; n =  [n] = [м -3]
-от температуры;
- от скорости движения;
- от массы атомов.
основное уравнение МКТ (уравнение Клаузиуса)
p =
[n] = [м -3]
-от температуры;
- от скорости движения;
- от массы атомов.
основное уравнение МКТ (уравнение Клаузиуса)
p = 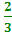 n Ek
P =
n Ek
P =  n moυ2ср.кв следствия p =
n moυ2ср.кв следствия p =  ρ υ2ср.кв
при смеси газов в сосуде выполняется закон Дальтона: давление смеси газов в сосуде равно сумме парциальных давлений входящих в него газов.
pоб = ∑ pi
ρ υ2ср.кв
при смеси газов в сосуде выполняется закон Дальтона: давление смеси газов в сосуде равно сумме парциальных давлений входящих в него газов.
pоб = ∑ pi




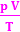 =
=  R
для данной массы газа отношение произведения давления на объём к температуре есть величина постоянная.
R
для данной массы газа отношение произведения давления на объём к температуре есть величина постоянная.