
- Автоматизация
- Антропология
- Археология
- Архитектура
- Биология
- Ботаника
- Бухгалтерия
- Военная наука
- Генетика
- География
- Геология
- Демография
- Деревообработка
- Журналистика
- Зоология
- Изобретательство
- Информатика
- Искусство
- История
- Кинематография
- Компьютеризация
- Косметика
- Кулинария
- Культура
- Лексикология
- Лингвистика
- Литература
- Логика
- Маркетинг
- Математика
- Материаловедение
- Медицина
- Менеджмент
- Металлургия
- Метрология
- Механика
- Музыка
- Науковедение
- Образование
- Охрана Труда
- Педагогика
- Полиграфия
- Политология
- Право
- Предпринимательство
- Приборостроение
- Программирование
- Производство
- Промышленность
- Психология
- Радиосвязь
- Религия
- Риторика
- Социология
- Спорт
- Стандартизация
- Статистика
- Строительство
- Технологии
- Торговля
- Транспорт
- Фармакология
- Физика
- Физиология
- Философия
- Финансы
- Химия
- Хозяйство
- Черчение
- Экология
- Экономика
- Электроника
- Электротехника
- Энергетика
Лабораторная работа № 11. Определение трехвалентного железа в растворе соли железа методом построения градуировочного графика
Лабораторная работа № 11
Определение трехвалентного железа в растворе соли железа методом построения градуировочного графика
Цель: : фотоколориметрически определить содержание железа (III) в растворе в виде тиоцианатного комплекса, используя в расчетах метод градуировочного графика
Посуда и реактивы: аналитические весы, фотоэлектроколориметр, стеклянные мерные цилиндры на 100 мл; колбы, железоаммонийные квасцы NH4Fe(SO4)2*12H2O; дистиллированная вода; азотная кислота.
Задание: выполните опыты, оформите отчёт.
Правила техники безопасности:
1. Правила работы с реактивами.
2. Правила работы с химической посудой.
3. Правила работы с нагревательными приборами.
Методические указания к выполнению лабораторной работы:
Спектр поглощения продукта взаимодействия ионов Fe3+ с SCN- имеет следующий вид: 360 420 480 540 600 l, нм. А = 0,0 0,2 0,4
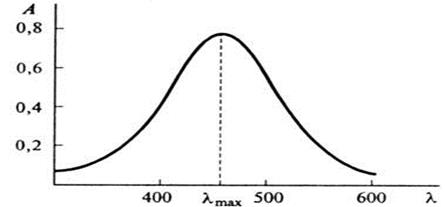
Максимальное поглощение наблюдается в интервале 470-485 нм, величина полуширины полосы поглощения составляет примерно 140 нм (410 - 550 нм). Оптимальным светофильтром для измерения оптической плотности для данного случая является светофильтр с максимумом пропускания при 490 нм (490±10 нм).
| Ход работы: ПРИГОТОВЛЕНИЕ СЕРИИ СТАНДАРТНЫХ РАСТВОРОВ 1. Приготовить стандартный раствор железоаммонийных квасцов. 1 мл. NH4Fe(SO4)2*12H2O содержит 0,1 мг железа (0,1мг/1мл)
МNH4Fe(SO4)2*12H2O= АFe= МNH4Fe(SO4)2*12H2O – АFe г/л Х - 0,1 х = г/л Взвесить на аналитических весах х г. железоаммонийных квасцов, растворить в мерной колбе дистиллированной воды. Подкислить 30 мл. концентрированной серной кислотой и довести раствор до метки в колбе 1 л. 0.1 мг железа в 1 мл. 2. В пронумерованные мерные колбы (1 – 7) вместимостью 50,00 мл мерной (градуированной) пипеткой, предназначенной строго для соединений железа, последовательно вносим по 0,50; 1,00; 1,50; 2,00; 2,50; 3,00 и 3,50 мл стандартного раствора с концентрацией железа (III) 100,0 мкг/мл. (0,1 мг/мл) 3. В каждую колбу добавляем по 5 мл 10% раствора KSCN (градуированной пробиркой). Аккуратно доливаем водой, дистиллированной на 1 см ниже метки и по каплям капельной пипеткой, доводим до метки; закрываем пробкой и тщательно перемешиваем.
ПРИГОТОВЛЕНИЕ РАСТВОРА НЕИЗВЕСТНОЙ КОНЦЕНТРАЦИИ
1. Полученную пробу количественно (полностью, многократно промывая водой, через воронку, аккуратно) переносим в мерную колбу (Х) вместимостью 50,00 мл; добавляем 5 мл 10% раствора KSCN, доводим дистиллированной водой до метки, закрываем пробкой и перемешиваем.
ИЗМЕРЕНИЕ ОПТИЧЕСКОЙ ПЛОТНОСТИ
1. Проводим измерения оптической плотности (А) каждого раствора (1–7, Х) на фотоэлектроколориметре (КФК-2, КФК-2МП) при светофильтре с максимумом пропускания 490 нм в кювете с толщиной поглощающего слоя 1,00 см относительно воды дистиллированной. 2. Полученные результаты представляем в виде таблицы:
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
| Лист | ||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| изм | Лист | № докум | Подп. | Дата | ||||||||||||||||||||||||||||||||||||||||||||||||||
|
Расчет массы железа (III) в приготовленных растворах | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
© helpiks.su При использовании или копировании материалов прямая ссылка на сайт обязательна.
|