
- Автоматизация
- Антропология
- Археология
- Архитектура
- Биология
- Ботаника
- Бухгалтерия
- Военная наука
- Генетика
- География
- Геология
- Демография
- Деревообработка
- Журналистика
- Зоология
- Изобретательство
- Информатика
- Искусство
- История
- Кинематография
- Компьютеризация
- Косметика
- Кулинария
- Культура
- Лексикология
- Лингвистика
- Литература
- Логика
- Маркетинг
- Математика
- Материаловедение
- Медицина
- Менеджмент
- Металлургия
- Метрология
- Механика
- Музыка
- Науковедение
- Образование
- Охрана Труда
- Педагогика
- Полиграфия
- Политология
- Право
- Предпринимательство
- Приборостроение
- Программирование
- Производство
- Промышленность
- Психология
- Радиосвязь
- Религия
- Риторика
- Социология
- Спорт
- Стандартизация
- Статистика
- Строительство
- Технологии
- Торговля
- Транспорт
- Фармакология
- Физика
- Физиология
- Философия
- Финансы
- Химия
- Хозяйство
- Черчение
- Экология
- Экономика
- Электроника
- Электротехника
- Энергетика
ХИМИЧЕСКОЕ РАВНОВЕСИЕ
ХИМИЧЕСКОЕ РАВНОВЕСИЕ
1.В системеSO2 (г) + Cl2 (г)  SO2Cl2 (г) + Q смещению химического равновесия вправо способствует 1)увеличение температуры 2)уменьшение давления 3)увеличение концентрации хлора 4)уменьшение концентрации оксида серы (IV)
SO2Cl2 (г) + Q смещению химического равновесия вправо способствует 1)увеличение температуры 2)уменьшение давления 3)увеличение концентрации хлора 4)уменьшение концентрации оксида серы (IV)
2. Равновесие в системе N2 + O2  2NO – Q будет смещаться в сторону продукта реакции при 1)увеличении концентрации кислорода 2)увеличении давления 3)уменьшении давления 4)понижении температуры
2NO – Q будет смещаться в сторону продукта реакции при 1)увеличении концентрации кислорода 2)увеличении давления 3)уменьшении давления 4)понижении температуры
3. Изменение давления смещает равновесие в системе 1) H2(г) + S(тв)  H2S(г
H2S(г
2) 3H2(г) + N2(г)  2NH3(г) 3)N2(г) + O2(г)
2NH3(г) 3)N2(г) + O2(г)  2NO(г) 4)H2(г) + Cl2(г)
2NO(г) 4)H2(г) + Cl2(г)  2HCl(г
2HCl(г
4. На смещение равновесия системы N2 (г) + O2 (г)  2NO (г) – Q не оказывает влияния 1)повышение температуры 2)повышение давления 3)повышение концентрации NO 4)уменьшение концентрации N2
2NO (г) – Q не оказывает влияния 1)повышение температуры 2)повышение давления 3)повышение концентрации NO 4)уменьшение концентрации N2
5. Химическое равновесие в системе 2HBr (г) ⇄ H2 (г) + Br2 (г) – Q сместится в сторону продуктов реакции при 1)повышении давления 2)повышении температуры 3)понижении давления 4)использовании катализатора
6. Химическое равновесие в системе С4Н10(г) ⇄ С4Н6(г) + 2Н2(г) – Q сместится в сторону обратной реакции, если 1)повысить давление2)добавить катализатор3)уменьшить концентрацию Н24)повысить температуру
7. Химическое равновесие в системе H2(г) + Cl2(г)  2HCl(г) + Q сместится влево при 1)уменьшении концентрации хлора 2)уменьшении концентрации хлороводорода 3)увеличении давления 4)уменьшении температуры
2HCl(г) + Q сместится влево при 1)уменьшении концентрации хлора 2)уменьшении концентрации хлороводорода 3)увеличении давления 4)уменьшении температуры
8. В системеCO2(г)+ C(тв)⇄2CO(г)−Q смещение химического равновесия вправо произойдёт при 1)повышении температуры 2)использовании катализатора 3)увеличении давления 4)уменьшении концентрации исходных веществ
9. Химическое равновесие в системе SO2(г) + 2H2S(г) ⇄ 3S(тв) + 2H2O(г) смещается в сторону продуктов реакции при 1)понижении давления 2)увеличении концентрации водяного пара 3)увеличении концентрации оксида серы(IV) 4)введении катализатора
10. В какой системе изменение давления не приведёт к смещению химического равновесия?
1)H2(г) + I2(г) ⇄ 2HI(г) 2)CO(г) + Cl2(г) ⇄ COCl2(г) 3)2CO(г) + O2(г) ⇄ 2CO2(г) 4)N2(г) + 3H2(г) ⇄ 2NH3(г)
11. Равновесие реакции СаСО3  СаО + СО2 – Q смещается вправо при 1)уменьшении температуры и увеличении давления 2)увеличении температуры и уменьшении давления 3)увеличении температуры и увеличении давления 4)уменьшении температуры и уменьшении давления
СаО + СО2 – Q смещается вправо при 1)уменьшении температуры и увеличении давления 2)увеличении температуры и уменьшении давления 3)увеличении температуры и увеличении давления 4)уменьшении температуры и уменьшении давления
12. Химическое равновесие в системе СаСО3(тв) ⇄ СаО(тв) + СО2(г) – Q смещается вправо при 1)повышении давления 2)повышении концентрации CO2 3)понижении температуры 4)повышении температуры
13. Химическое равновесие в системе C4H8(г) + H2(г) ⇄ C4H10(г) + Q смещается в сторону исходных веществ в результате 1)увеличения концентрации водорода 2)повышения температуры 3)повышения давления 4)использования катализатора
14. Смещению химического равновесия вправо в системе СO2(г) + С(тв)  2СО(г) – Q будет способствовать 1)уменьшение температуры 2)уменьшение давления 3)увеличение концентрации СО 4)уменьшение концентрации СO2
2СО(г) – Q будет способствовать 1)уменьшение температуры 2)уменьшение давления 3)увеличение концентрации СО 4)уменьшение концентрации СO2
15.Химическое равновесие в системе C4H10 (г)  C4H8 (г) + H2 (г) – Q можно сместить в сторону продуктов реакции 1)повышением температуры и повышением давления 2)повышением температуры и понижением давления 3)понижением температуры и повышением давления 4)понижением температуры и понижением давления
C4H8 (г) + H2 (г) – Q можно сместить в сторону продуктов реакции 1)повышением температуры и повышением давления 2)повышением температуры и понижением давления 3)понижением температуры и повышением давления 4)понижением температуры и понижением давления
16. На состояние химического равновесия в системе 2SO2 + O2  2SO3 + Q не влияет 1)катализатор 2)изменение концентрации исходных веществ 3)изменение температуры 4)изменение давления
2SO3 + Q не влияет 1)катализатор 2)изменение концентрации исходных веществ 3)изменение температуры 4)изменение давления
17. Верны ли следующие суждения о смещении химического равновесия в системе С2Н4(г) + Н2(г) ⇄ С2Н6(г) + Q?
| А. | При увеличении температуры в данной системе смещения химического равновесия не происходит. |
| Б. | При увеличении концентрации водорода равновесие в системе смещается в сторону исходных веществ. |
1)верно только А 2)верно только Б 3)верны оба суждения 4)оба суждения неверны
18. В какой системе состояние химического равновесия не изменится при увеличении давления? 1)CO(г) + H2O(г) ⇄ CO2(г) + H2(г) 2)CH4(г) + H2O(г) ⇄ CO(г) + 3H2(г)
3)C(тв) + H2O(г) ⇄ CO(г) + H2(г ) 4)2NO(г) + O2(г) ⇄ 2NO2(г)
19. Химическое равновесие в системе CH4(г)+ 2H2O(г)⇄ CO2(г)+ 4H2(г)− Q смещается в сторону образования оксида углерода(IV) при 1)повышении давления 2)повышении температуры 3)понижении температуры 4)добавлении катализатора
20. На смещение химического равновесия обратимой реакции не влияет 1)увеличение температуры 2)уменьшение температуры 3)добавление катализатора 4)изменение концентраций веществ
21. В системе N2(г)+ O2(г)⇄2NO(г)−Q химическое равновесие не смещается при 1)увеличении концентрации NO 2)повышении давления 3)повышении температуры 4)увеличении концентрации O2
22. Химическое равновесие в системе I2(г) + Cl2(г) ⇄ 2ICl(г) + Q смещается в сторону продукта реакции при 1)повышении температуры 2)понижении температуры 3)увеличении давления 4)введении катализатора
23. В системе SO2(г) + 2H2S(г) ⇄ 3S(тв) + 2H2O(г) на смещение химического равновесия не оказывает влияния 1)уменьшение количества серы 2)понижение давления 3)увеличение концентрации сероводорода 4)повышение давления
24. Равновесие в системе 3O2(г)  2O3(г) – Q сместится вправо при уменьшении 1)температуры 2)давления 3)концентрации О2 4)концентрации О3
2O3(г) – Q сместится вправо при уменьшении 1)температуры 2)давления 3)концентрации О2 4)концентрации О3
25. Равновесие в системе H2(г) + I2(г)  2HI(г) + Q сместится в сторону продуктов реакции 1)при повышении температуры 2)при повышении давления3)в присутствии катализатора4)при понижении температуры
2HI(г) + Q сместится в сторону продуктов реакции 1)при повышении температуры 2)при повышении давления3)в присутствии катализатора4)при понижении температуры
26. Химическое равновесие в системе 2CO(г) ⇄ CO2(г) + C(тв) + 173 кДж
смещается в сторону продуктов реакции при 1)повышении давления 2)повышении температуры 3)понижении давления 4)использовании катализатора
27. В какой системе изменение давления не влияет на смещение химического равновесия?
1)N2(г) + 3H2(г) 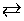 2NH3(г ) 2)2Н2(г) + О2(г)
2NH3(г ) 2)2Н2(г) + О2(г) 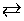 2Н2О(г)
2Н2О(г)
3)H2(г) + Cl2(г) 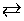 2НCl(г) 4)SO2(г) + Cl2(г)
2НCl(г) 4)SO2(г) + Cl2(г) 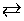 SO2Cl2(г)
SO2Cl2(г)
28. В системе 2SO2(г) + O2(г)  2SO3(г) + Q смещению химического равновесия в сторону исходных веществ будет способствовать 1)уменьшение давления 2)уменьшение температуры 3)увеличение концентрации SО2 4)уменьшение концентрации SO3
2SO3(г) + Q смещению химического равновесия в сторону исходных веществ будет способствовать 1)уменьшение давления 2)уменьшение температуры 3)увеличение концентрации SО2 4)уменьшение концентрации SO3
29. В системе Fe2O3 (тв.) + 3CO (г)  2Fe (тв.) + 3CO2 (г) + Q на смещение химического равновесия не влияет 1)увеличение концентрации CO 2)уменьшение температуры 3)увеличение давления 4)уменьшение концентрации CO2
2Fe (тв.) + 3CO2 (г) + Q на смещение химического равновесия не влияет 1)увеличение концентрации CO 2)уменьшение температуры 3)увеличение давления 4)уменьшение концентрации CO2
30.Химическое равновесие в системе С2Н5ОН + СН3СООН ⇄ СН3СООС2Н5 + Н2О – Q смещается в сторону продуктов реакции при 1)добавлении воды 2)уменьшении концентрации уксусной кислоты 3)увеличении концентрации эфира 4)удалении воды
31. Изменение давления оказывает влияние на смещение равновесия в системе 1)2SO2 + O2  2SO3 (г) 2)2HI (г)
2SO3 (г) 2)2HI (г)  H2 + I2 (г) 3)СO + Н2О (г)
H2 + I2 (г) 3)СO + Н2О (г)  СO2 + Н2 4)N2 + О2
СO2 + Н2 4)N2 + О2  2NО
2NО
32. Химическое равновесие в системе 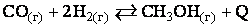 сместится в сторону продукта реакции при 1)понижении температуры 2)понижении концентрации CO 3)повышении концентрации СН3ОН 4)повышении температуры
сместится в сторону продукта реакции при 1)понижении температуры 2)понижении концентрации CO 3)повышении концентрации СН3ОН 4)повышении температуры
33. Верны ли следующие суждения о смещении химического равновесия в системе O2(г) + 2CO(г) ⇄ 2CO2(г) + Q?
| А. | При уменьшении температуры химическое равновесие в данной системе сместится в сторону продуктов реакции. |
| Б. | При уменьшении концентрации угарного газа равновесие системы сместится в сторону продуктов реакции. |
1)верно только А 2)верно только Б 3)верны оба суждения 4)оба суждения неверны
34.Изменение давления не повлияет на состояние химического равновесия в системе 1)2NO(г)+ O2(г)⇄ 2NO2(г) 2)N2(г)+ 3H2(г)⇄ 2NH3(г) 3)2CO(г)+ O2(г)⇄ 2CO2(г) 4)N2(г)+ O2(г)⇄ 2NO(г)
35. В системеSO2 (г) + Cl2 (г)  SO2Cl2 (г) + Q смещению химического равновесия вправо способствует 1)увеличение температуры 2)уменьшение давления 3)увеличение концентрации хлора 4)уменьшение концентрации оксида серы (IV)
SO2Cl2 (г) + Q смещению химического равновесия вправо способствует 1)увеличение температуры 2)уменьшение давления 3)увеличение концентрации хлора 4)уменьшение концентрации оксида серы (IV)
36. Химическое равновесие с системе N2(r) + O2(r)  2NO(г) – Q не смещается при 1)увеличении концентрации NO 2)понижении давления 3)понижении температуры 4)добавлении кислорода
2NO(г) – Q не смещается при 1)увеличении концентрации NO 2)понижении давления 3)понижении температуры 4)добавлении кислорода
37. В системеSO2 (г) + Cl2 (г)  SO2Cl2 (г) + Q смещению химического равновесия вправо способствует 1)увеличение температуры 2)уменьшение давления 3)увеличение концентрации хлора 4)уменьшение концентрации оксида серы (IV)
SO2Cl2 (г) + Q смещению химического равновесия вправо способствует 1)увеличение температуры 2)уменьшение давления 3)увеличение концентрации хлора 4)уменьшение концентрации оксида серы (IV)
38. Химическое равновесие с системеN2(r) + O2(r)  2NO(г) – Q не смещается при 1)увеличении концентрации NO 2)понижении давления 3)понижении температуры 4)добавлении кислорода
2NO(г) – Q не смещается при 1)увеличении концентрации NO 2)понижении давления 3)понижении температуры 4)добавлении кислорода
39. Химическое равновесие в системе СО2(г) + Н2О(ж)  Н2СО3(ж) + Q сместится вправо при 1)понижении температуры 2)введении катализатора 3)понижении давления 4)уменьшении концентрации СО2
Н2СО3(ж) + Q сместится вправо при 1)понижении температуры 2)введении катализатора 3)понижении давления 4)уменьшении концентрации СО2
40. Химическое равновесие в системе C4H10(г) ⇄ C4H6(г) + 2H2(г) − Q сместится в сторону продуктов реакции при 1)повышении температуры 2)понижении температуры 3)использовании катализатора 4)уменьшении концентрации C4H10
41. Химическое равновесие с системе N2(r) + O2(r)  2NO(г) – Q не смещается при 1)увеличении концентрации NO 2)понижении давления 3)понижении температуры 4)добавлении кислорода
2NO(г) – Q не смещается при 1)увеличении концентрации NO 2)понижении давления 3)понижении температуры 4)добавлении кислорода
42. Химическое равновесие в системе СО2(г) + Н2О(ж)  Н2СО3(ж) + Q сместится вправо при 1)понижении температуры 2)введении катализатора 3)понижении давления 4)уменьшении концентрации СО2
Н2СО3(ж) + Q сместится вправо при 1)понижении температуры 2)введении катализатора 3)понижении давления 4)уменьшении концентрации СО2
43. В какой системе увеличение давления и понижение температуры смещает химическое равновесие в сторону продуктов реакции? 1)2SO2(г) + O2(г)  2SО3(г) + Q
2SО3(г) + Q
2)N2(г) + О2(г)  2NO(г) – Q 3)CO2(г) + 2C(тв.)
2NO(г) – Q 3)CO2(г) + 2C(тв.)  2CO(г) – Q4) 2NH3(г)
2CO(г) – Q4) 2NH3(г)  N2(г) + 3H2(г) – Q
N2(г) + 3H2(г) – Q
44. Изменение давления не смещает равновесие в системе
1)Н2(г) + Sе(г)  H2Sе(г) 2)Н2(г) +Br2(ж)
H2Sе(г) 2)Н2(г) +Br2(ж)  2HBr(г)
2HBr(г)
3)Н2(г) + Сl2(г)  2HCl(г) 4)2NO(г) + O2(г)
2HCl(г) 4)2NO(г) + O2(г)  2NO2(г)
2NO2(г)
45. В системе COСl2(г)  CO(г) + Cl2(г) – Q смещению химического равновесия вправо будет способствовать 1)уменьшение температуры 2)увеличение концентрации оксида углерода (II) 3)увеличение давления 4)уменьшение концентрации хлора
CO(г) + Cl2(г) – Q смещению химического равновесия вправо будет способствовать 1)уменьшение температуры 2)увеличение концентрации оксида углерода (II) 3)увеличение давления 4)уменьшение концентрации хлора
46. Верны ли следующие суждения о смещении химического равновесия в системе 2CO(г) + O2(г) ⇄ 2CO2(г) + Q?
| А. | При понижении давления химическое равновесие в данной системе сместится в сторону продукта реакции. |
| Б. | При увеличении концентрации углекислого газа химическое равновесие системы сместится в сторону продукта реакции. |
1)верно только А 2)верно только Б 3)верны оба суждения 4)оба суждения неверны
47. В какой системе при повышении давления химическое равновесие сместится в сторону исходных веществ? 1)N2(г) + 3H2(г)  2NH3(г) + Q 2)N2O4(г)
2NH3(г) + Q 2)N2O4(г)  2NO2(г) – Q
2NO2(г) – Q
3)CO2(г) + H2(г)  CO(г) + H2O(г) – Q 4)4HCl(г) + O2
CO(г) + H2O(г) – Q 4)4HCl(г) + O2  2H2O(г) + 2Cl2(г) + Q
2H2O(г) + 2Cl2(г) + Q
48. При повышении давления равновесие смещается вправо в системе
1)2CO2(г)  2CO(г) + O2(г) 2)С2Н4(г)
2CO(г) + O2(г) 2)С2Н4(г)  С2Н2(г) + Н2(г)
С2Н2(г) + Н2(г)
3)PCl3(г) + Cl2(г)  PCl5(г) 4)H2(г) + Сl2(г)
PCl5(г) 4)H2(г) + Сl2(г)  2 HCl(г)
2 HCl(г)
49. Верны ли следующие суждения о смещении химического равновесия в системе СO(г) + Cl2(г) ⇄ СOCl2(г) + Q?
| А. | При использовании катализатора смещения химического равновесия в данной системе не происходит. |
| Б. | При увеличении температуры химическое равновесие в данной системе сместится в сторону исходных веществ. |
1)верно только А 2)верно только Б 3)верны оба суждения 4)оба суждения неверны
50. На смещение химического равновесия в системе Fe3O4(тв) + CO(г)  3FeO(тв) + CO2(г) + Q не оказывает влияния 1)уменьшение концентрации СО 2)увеличение температуры 3)увеличение давления 4)уменьшение концентрации СО2
3FeO(тв) + CO2(г) + Q не оказывает влияния 1)уменьшение концентрации СО 2)увеличение температуры 3)увеличение давления 4)уменьшение концентрации СО2
51. Химическое равновесие в системе 2NO(г) + O2 (г)  2NO2 (г) + Q смещается в сторону образования продукта реакции при 1)повышении давления 2)повышении температуры 3)понижении давления 4)применении катализатора
2NO2 (г) + Q смещается в сторону образования продукта реакции при 1)повышении давления 2)повышении температуры 3)понижении давления 4)применении катализатора
52. На смещение химического равновесия в системе N2 + 3H2  2NH3 + Q не оказывает влияния 1)понижение температуры 2)повышение давления 3)удаление аммиака из зоны реакции 4)применение катализатора
2NH3 + Q не оказывает влияния 1)понижение температуры 2)повышение давления 3)удаление аммиака из зоны реакции 4)применение катализатора
53. Химическое равновесие в системе Fe3О4(тв) + 4СО(г) ⇄ 3Fe(тв) + 4СО2(г) – Q смещается в сторону продуктов реакции при 1)понижении температуры 2)использовании катализатора 3)повышении температуры 4)понижении давления
54. При одновременном повышении температуры и понижении давления химическое равновесие сместится вправо в реакции 1)Н2 + S(г)  Н2S + Q 2)2SO2 + O2
Н2S + Q 2)2SO2 + O2  2SO3 + Q
2SO3 + Q
3)2NH3  N2 + 3H2 – Q 4)2НСl
N2 + 3H2 – Q 4)2НСl  Н2 + Сl2 – Q
Н2 + Сl2 – Q
55. В системе 2CO (г) + O2 (г)  2CO2 (г) + Q смещению химического равновесия в сторону исходных веществ будет способствовать 1)увеличение давления 2)увеличение концентрации оксида углерода (IV) 3)уменьшение температуры 4)увеличение концентрации кислорода
2CO2 (г) + Q смещению химического равновесия в сторону исходных веществ будет способствовать 1)увеличение давления 2)увеличение концентрации оксида углерода (IV) 3)уменьшение температуры 4)увеличение концентрации кислорода
56. На состояние химического равновесия в системе H2(г) + I2(г) 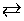 2HI(г) – Q не влияет 1)увеличение давления 2)увеличение концентрации I2 3)увеличение температуры 4)уменьшение температуры
2HI(г) – Q не влияет 1)увеличение давления 2)увеличение концентрации I2 3)увеличение температуры 4)уменьшение температуры
57. В какой системе при повышении давления химическое равновесие сместится вправо?
1)2HI (г) 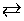 H2 (г) + I2 (г) 2)C (тв) + S2 (г)
H2 (г) + I2 (г) 2)C (тв) + S2 (г) 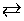 CS2 (г) 3)C3H6 (г) + H2 (г)
CS2 (г) 3)C3H6 (г) + H2 (г) 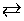 C3H8 (г) 4)H2 (г) + F2 (г)
C3H8 (г) 4)H2 (г) + F2 (г) 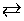 2HF (г)
2HF (г)
58. Химическое равновесие в системе CO2 (г) + C (тв)  2CO (г) – Q сместится вправо при 1)повышении давления 2)понижении температуры 3)повышении концентрации СO 4)повышении температуры
2CO (г) – Q сместится вправо при 1)повышении давления 2)понижении температуры 3)повышении концентрации СO 4)повышении температуры
59. Химическое равновесие в системе NH3 · H2O  NH4+ + OH– сместится в сторону образования NH3 · H2O при добавлении к водному раствору аммиака 1)NaCl 2)NaOH 3)HCl 4)AlCl3
NH4+ + OH– сместится в сторону образования NH3 · H2O при добавлении к водному раствору аммиака 1)NaCl 2)NaOH 3)HCl 4)AlCl3
60. В системе CH3COOH(ж) + CH3OH(ж) ⇄ CH3COOCH3(ж) + H2O(ж) смещению химического равновесия в сторону образования сложного эфира будет способствовать 1)добавление метанола 2)повышение давления 3)повышение концентрации эфира 4)добавление гидроксида натрия
61.В системе СО(г) + Н2О(г) ⇄ СО2(г) + Н2(г) + Q смещению химического равновесия вправо будет способствовать 1)уменьшение давления 2)увеличение температуры 3)увеличение концентрации СО 4)увеличение концентрации Н2
62. В системе 2SO2(г) + O2(г) ⇄ 2SO3(г) + Q смещение химического равновесия вправо произойдет при 1)добавлении катализатора 2)повышении температуры 3)увеличении концентрации оксида серы (VI ) 4)повышении давления
63. Верны ли следующие суждения о смещении химического равновесия в системе CO(г) + 2Н2(г) ⇄ СH3OH(г) + Q?
| А. | При понижении температуры химическое равновесие в данной системе смещается в сторону продуктов реакции. |
| Б. | При уменьшении концентрации метанола равновесие в системе смещается в сторону продуктов реакции. |
1)верно только А 2)верно только Б 3)верны оба суждения 4)оба суждения неверны
ОТВЕТЫ
|
|
|
© helpiks.su При использовании или копировании материалов прямая ссылка на сайт обязательна.
|