
- Автоматизация
- Антропология
- Археология
- Архитектура
- Биология
- Ботаника
- Бухгалтерия
- Военная наука
- Генетика
- География
- Геология
- Демография
- Деревообработка
- Журналистика
- Зоология
- Изобретательство
- Информатика
- Искусство
- История
- Кинематография
- Компьютеризация
- Косметика
- Кулинария
- Культура
- Лексикология
- Лингвистика
- Литература
- Логика
- Маркетинг
- Математика
- Материаловедение
- Медицина
- Менеджмент
- Металлургия
- Метрология
- Механика
- Музыка
- Науковедение
- Образование
- Охрана Труда
- Педагогика
- Полиграфия
- Политология
- Право
- Предпринимательство
- Приборостроение
- Программирование
- Производство
- Промышленность
- Психология
- Радиосвязь
- Религия
- Риторика
- Социология
- Спорт
- Стандартизация
- Статистика
- Строительство
- Технологии
- Торговля
- Транспорт
- Фармакология
- Физика
- Физиология
- Философия
- Финансы
- Химия
- Хозяйство
- Черчение
- Экология
- Экономика
- Электроника
- Электротехника
- Энергетика
Многие лекарства являются конкурентными ингибиторами ферментов. В основе действия некоторых токсичных веществ лежит ингибирование активности ферментов.
Билет 11
Вопрос 1
Многие лекарства являются конкурентными ингибиторами ферментов. В основе действия некоторых токсичных веществ лежит ингибирование активности ферментов.
Пример 2.Органические фторфосфаты типа ди-изопропилфторфосфата (ДФФ) являются ядами, потому что ковалентно связываются с остатком се-рина в активном центре некоторых ферментов.
Диизопропилфторфосфати подобные соединения связываются в активном центре ферментов, которые используют остаток серина для гидролитического расщепления.
Симптомы отравления органическими фтор-фосфатами связаны в основном с необратимым ингибированием фермента — ацетилхолинэсте-разы (АХЭ).
Ацетилхолинэстеразаускоряет гидролиз ацетил-холина, функционирующего в качестве нейроме-диатора (рис. 2.19). Продукты распада ацетилхолина — ацетат и холин — не способны действовать как нейромедиаторы. Гидролиз ацетилхолина — важный этап в проведении нервного импульса.
Увеличение количества ацетилхолина в синапти-ческой щели при ингибировании АХЭ приводит к стойкой деполяризации постсинаптической мембраны и может вызвать паралич.
ДФФ и подобные фторфосфаты образуют кова-лентную связь с остатком серина в активном центре АХЭ. Ингибирование является необратимым, и активность АХЭ восстанавливается только после синтеза новых молекул фермента.
Вопрос 2
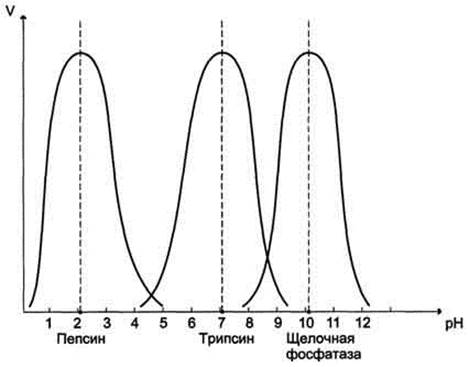
Зависимость существует потому, что различные ферменты «работают» при разных условиях – от кислотной до щелочной.
Вопрос 3
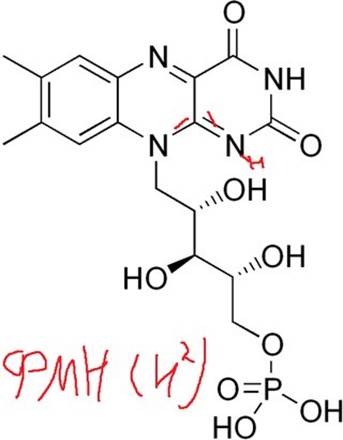
Кофермент ФАДа-витамин В2
Вопрос 4
Сахара́зы — обширная группа гликозил-гидролаз,(Гликозил-гидролазы (или гликозидазы) катализируют гидролиз гликозидных связей в молекулах углеводов, приводя к появлению двух более мелких молекул углеводов. Эти ферменты встречаются в клетках почти всех живых организмов.) способных расщеплять молекулы сахарозы на глюкозу и фруктозу
Она катализирует реакцию расщипления сахарозы на глюкозу и фруктозу
Доказательство-практикум, 5.1.2
Вопрос 5
Электронтранспортные цепи митохондрий эукариот
§ Комплекс I (НАДН дегидрогеназа) окисляет НАД-Н, отбирая у него два электрона и перенося их на растворимый в липидах убихинон, который внутри мембраны диффундирует к комплексу III. Вместе с этим, комплекс I перекачивает 4 протона из матрикса в межмембранное пространство митохондрии.
§ Комплекс II (Сукцинат дегидрогеназа) не перекачивает протоны, но обеспечивает вход в цепь дополнительных электронов за счёт окисления сукцината.
§ Комплекс III (Цитохром bc1 комплекс) переносит электроны с убихинола на два водорастворимых цитохрома с, расположенных на внутренней мембране митохондрии. Убихинол передаёт 2 электрона, а цитохромы за один цикл переносят по одному электрону. При этом туда также переходят 2 протона убихинола и перекачиваются комплексом.
§ Комплекс IV (Цитохром c оксидаза) катализирует перенос 4 электронов с 4 молекул цитохрома на O2 и перекачивает при этом 4 протона в межмембранное пространство. Комплекс состоит из цитохромов a и a3, которые, помимо гема, содержат ионы меди.
Кислород, поступающий в митохондрии из крови, связывается с атомом железа в геме цитохрома a3 в форме молекулы O2. Каждый из атомов кислорода присоединяет по два электрона и два протона и превращается в молекулу воды.
|
|
|
© helpiks.su При использовании или копировании материалов прямая ссылка на сайт обязательна.
|