
- Автоматизация
- Антропология
- Археология
- Архитектура
- Биология
- Ботаника
- Бухгалтерия
- Военная наука
- Генетика
- География
- Геология
- Демография
- Деревообработка
- Журналистика
- Зоология
- Изобретательство
- Информатика
- Искусство
- История
- Кинематография
- Компьютеризация
- Косметика
- Кулинария
- Культура
- Лексикология
- Лингвистика
- Литература
- Логика
- Маркетинг
- Математика
- Материаловедение
- Медицина
- Менеджмент
- Металлургия
- Метрология
- Механика
- Музыка
- Науковедение
- Образование
- Охрана Труда
- Педагогика
- Полиграфия
- Политология
- Право
- Предпринимательство
- Приборостроение
- Программирование
- Производство
- Промышленность
- Психология
- Радиосвязь
- Религия
- Риторика
- Социология
- Спорт
- Стандартизация
- Статистика
- Строительство
- Технологии
- Торговля
- Транспорт
- Фармакология
- Физика
- Физиология
- Философия
- Финансы
- Химия
- Хозяйство
- Черчение
- Экология
- Экономика
- Электроника
- Электротехника
- Энергетика
Тема урок: Щелочные металлы. Строение атомов химических элементов. I группы главной подгруппы. Задание 2:Составьте электронные формулы атомов лития, натрия, калия. Физические свойства щелочных металлов
Тема урок: Щелочные металлы
Металлы главной подгруппы I группы называются щелочными металлами. Свое название они получили от названия соответствующих им гидроксидов, хорошо растворимых в воде, — щелочей.
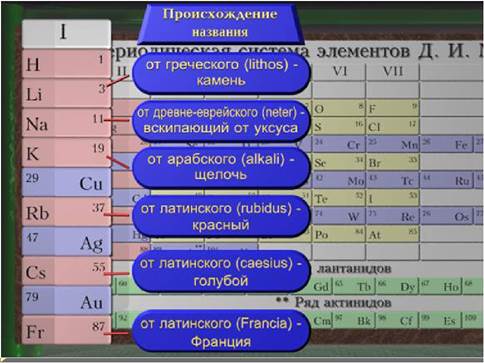

Строение атомов химических элементов
I группы главной подгруппы
Задание1: заполните таблицу: «Общая характеристика химических элементов I группы главной подгруппы»
| Название и символ элемента | Состав атомного ядра:p = ?, n = ? | Число валентных электронов | Число энергетических уровней | Характерные степени окисления |
| Li – литий | ||||
| Na – натрий | ||||
| Rb – рубидий | ||||
| Cs – цезий | ||||
| Fr – франций |
Задание 2:Составьте электронные формулы атомов лития, натрия, калия
Задание 3: Сделайте выводы: в чём сходство и в чём различие в строении атомов щелочных металлов
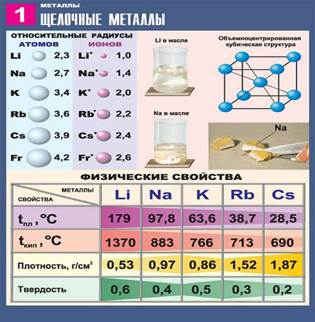
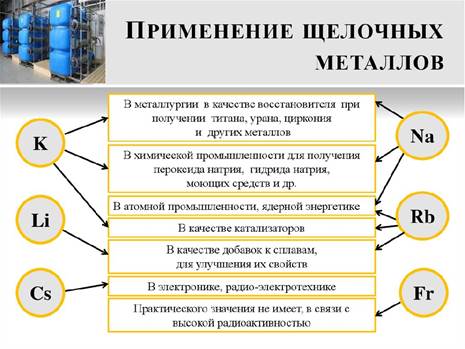
Физические свойства щелочных металлов
Щелочные металлы – это простые вещества, для которых также, как и для всех металлов, характерна металлическая связь и металлическая кристаллическая решетка. Металлическая связь возникает за счет отдачи одного электрона атомом металла и образованием иона металла с положительным зарядом: М0 – 1е → М+1. Наличие металлической связи и металлической кристаллической решетки обуславливает следующие физические свойства щелочных металлов: серебристо – белые, мягкие, обладают блеском, легкие, их плотность меньше 5 г/см3 и возрастает от лития к цезию, легкоплавкие, их температура, наоборот, от лития к цезию уменьшается.

|
|
|
© helpiks.su При использовании или копировании материалов прямая ссылка на сайт обязательна.
|