
- Автоматизация
- Антропология
- Археология
- Архитектура
- Биология
- Ботаника
- Бухгалтерия
- Военная наука
- Генетика
- География
- Геология
- Демография
- Деревообработка
- Журналистика
- Зоология
- Изобретательство
- Информатика
- Искусство
- История
- Кинематография
- Компьютеризация
- Косметика
- Кулинария
- Культура
- Лексикология
- Лингвистика
- Литература
- Логика
- Маркетинг
- Математика
- Материаловедение
- Медицина
- Менеджмент
- Металлургия
- Метрология
- Механика
- Музыка
- Науковедение
- Образование
- Охрана Труда
- Педагогика
- Полиграфия
- Политология
- Право
- Предпринимательство
- Приборостроение
- Программирование
- Производство
- Промышленность
- Психология
- Радиосвязь
- Религия
- Риторика
- Социология
- Спорт
- Стандартизация
- Статистика
- Строительство
- Технологии
- Торговля
- Транспорт
- Фармакология
- Физика
- Физиология
- Философия
- Финансы
- Химия
- Хозяйство
- Черчение
- Экология
- Экономика
- Электроника
- Электротехника
- Энергетика
Реферат по дисциплине. Основы токсикологии и токсикология биоматериалов. Отравление фосфорорганическими соединениями». Проверил . Москва, 2020
Министерство науки и высшего образования Российской Федерации
ФГБОУ ВО «Российский химико-технологический университет
имени Д. И. Менделеева»
Институт проблем химии и устойчивого развития
Кафедра биоматериалов
Реферат по дисциплине
Основы токсикологии и токсикология биоматериалов
«Отравление фосфорорганическими соединениями»
Проверил
д.х.н., профессор А. Н. Кусков
Обучающийся О.Л. Астаркина
Москва, 2020
Содержание
Введение…………………………………………………………….……………3
1. Токсикологическая характеристика фосфорорганических веществ………4
2. Физико-химические свойства и токсические свойства ФОС………………6
3. Механизм токсического действия ФОС……………………………………..8
3.1. Теория антихолистэразного действия………………………………….…8
3.2. Теория неантихолинэстеразного действия………………………………10
4. Пути поступления, распределения, биотрансформации и выведения вещества………………………………………………………………………….12
5. Особенности клинических проявлений при отравлении…………………..14
6. Основные принципы терапии отравления………………………….……….16
Заключение……………………………………………………………………….19
Список используемой литературы……………………………………...………20
Введение
Впервые токсические свойства фосфорорганических соединений (ФОС) были обнаружены в начале ХХ века. Во времена Второй мировой войны ФОС применялись в качестве боевых отравляющих веществ (газ зарин), а в конце войны были созданы промышленные установки по синтезу первых пестицидов. Вскоре они заменили собой низкоэкологичные ДДТ, гексохлоран и прочие хлорорганические соединения в сельском хозяйстве, оказавшись простыми в синтезе и высокоэффективными против насекомых. В настоящее время ФОС не утратили своих преимуществ и широко используются для обработки садов, овощебахчевых, зерновых и других культур в качестве инсектицидов. Однако существует и обратная сторона медали, заключающаяся в значительной токсичности используемых ФОС. Большинство из них при попадании на кожу, вдыхании или проглатывании легко всасываются, вызывая отравления различной степени как среди работников сельского хозяйства, так и среди населения, использующего инсектициды в быту. Таким образом, в настоящее время есть необходимость в проведении исследований с целью анализа токсикологических характеристик ФОС и оценки степени их опасности для безопасности жизнедеятельности.
1. Токсикологическая характеристика фосфорорганических веществ
ФОС (зарин, зоман, VX, фосфакол, армин, карбофос, дихлофос и др.) – токсичные химические вещества, относящиеся к нейротоксикантам нервно-паралитического действия.
Нейротоксичность – это способность химических веществ, действуя на организм, вызывать нарушение структуры и (или) функции нервной системы.
Нейротоксичность присуща большинству известных веществ. Она может быть следствием прямого, или опосредованного повреждением других органов, действия токсикантов на нервную систему. Практически любая острая интоксикация в той или иной степени сопровождается нарушениями функций нервной системы.
К числу нейротоксикантов относят вещества, для которых порог чувствительности нервной системы (отдельных её гистологических и анатомических образований) существенно ниже, чем других органов и систем, и в основе интоксикации которыми лежит поражение именно нервной системы. Токсический процесс, развивающийся в результате действия нейротоксикантов, проявляется нарушением механизмов нервной регуляции жизненно важных органов и систем, а также памяти, мышления, эмоций, поведения и т.д.
В основе токсического действия нейротоксикантов может лежать повреждение любого структурного элемента нервной системы путем изменения пластического и энергетического обмена, нарушения генерации, проведения нервного импульса по возбудимым мембранам, передачи сигнала в синапсах.
ФОС абсорбируются через кожу, слизистую бронхов и кишечника. Высокотоксичные ФОС не обладают раздражающим действием на месте аппликации (слизистые оболочки верхних дыхательных путей и желудочно-кишечного тракта, конъюнктива глаз, кожа) и проникают в организм практически незаметно.
ФОС оказывают местное и резорбтивное действие. Большинство развивающихся эффектов является следствием перевозбуждения мускарин- и никотинчувствительных холинэргических синапсов центральной нервной системы и периферии.
Ингибируя холинэстеразу плазмы и эритроцитов, предотвращая распад ацетилхолина, который, в связи с этим, накапливается в нервных окончаниях и нервно-мышечных соединениях, ФОС вызывают развитие судорожного синдрома, комы и гибели пострадавшего от остановки дыхания и сердечной деятельности на фоне истощения энергетических ресурсов организма.
Судороги возникают либо в результате гиперактивации процессов возбуждения, либо угнетения процессов торможения. Основными возбуждающими нейромедиаторами мозга являются ацетилхолин и возбуждающие аминокислоты (глутамат, аспартат). Тормозные процессы осуществляются с помощью пресинаптических и постсинаптических механизмов. В различных отделах центральной нервной системы механизмы пре- и постсинаптического торможения осуществляются посредством высвобождения в синаптическую щель гамма-аминомасляной кислоты (ГАМК).
По классификации Л.И. Медведя выделяют следующие ФОС: сильноядовитые (DL50 – <50мг/кг): тиофос, октаметил; высокотоксичные (DL50 – 200мг/кг): метилмеркаптофос, дихлорфос (ДДВФ); средней степени токсичности (DL50 – 200-1000 мг/кг): хлорофос, карбофос, цианофос; малотоксичные (DL50 > 1000 мг/кг).
2. Физико-химические свойства и токсические свойства ФОС
Фосфорорганические инсектициды обычно представляют собой сложные эфиры, амиды или тиоловые производные фосфорной, алкилфосфорной (табун, зарин, зоман, и V-средства – БОВ), тиофосфорной и тиофосфоновой кислот. Это бесцветные жидкости, различные по консистенции, не имеющие запаха. Наиболее плотным является вещество VX, напоминающее липкое смазочное масло.
Табл. 1. Сравнительная характеристика некоторых ФОС
| Свойства | Зарин | Зоман | VX |
| Название | Изопропил метилфосфонамид | Пинаколиловый эфир метилфторфосфоновой кислоты | О-этил-S-2- диизопропиламин этилметилфосфонат |
| ММ | 182,2 | 267,4 | |
| Агрегатное состояние | Жидкость без цвета и запаха, хорошо растворим в воде и орг. растворителях | Прозрачная жидкость с легким запахом камфоры. Плохо растворим в воде. | Жидкость янтарного цвета, напоминающая машинное масло. |
| T кип, ◦С | |||
| LCt50 г*мин/м3 | 0,035-0,1 | 0,025-0,05 | 0,005-0,035 |
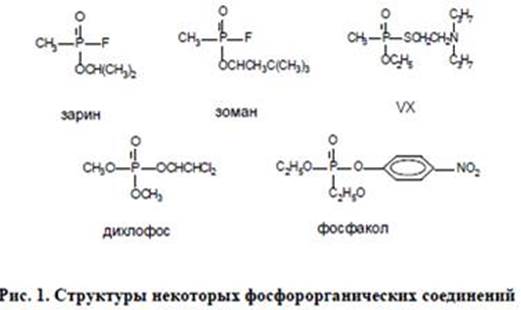
Фосфорорганические соединения, кроме некоторых (хлорофос), плохо растворимы в воде и хорошо — в органических растворителях и липидах. Концентраты эмульсий переходят в воде в стойкую эмульсию. Такие эмульсии наиболее опасны для рыбоводства. ФОС относительно малостойки в окружающей среде. Большая часть их разлагается в почве, воде, растениях в течение нескольких месяцев. Только некоторые инсектоакарициды внутрирастительного действия (метилмеркаптофос, антио, фосфамид, сайфос и др.) сохраняются до года. Скорость гидролиза таких соединений возрастает в несколько раз с увеличением pH воды и её температуры.
Все органофосфаты обладают высокой реакционной способностью, в частности, способностью к неспецифической сорбции белками крови и ферментативному гидролизу. В крови животных и других тканях, главным образом в печени, обнаружены ферменты типа фосфатаз (условно называемые зариназами, зоманазами), под действием которых происходит гидролиз фосфорорганических веществ (ФОВ) с образованием нетоксических веществ. Гидролиз ФОВ у различных животных происходит с различной скоростью, и от этого в определенной степени зависит различная токсичность вещества.
С другой стороны, токсичность некоторых ФОС (инсектицидов) в организме усиливается в результате ферментативного окисления или перегруппировки атомов под действием микросомальных оксидаз печени и цитохрома Р-450 (летальный синтез).
В результате процессов метаболизма в органах рыб ФОС преобразуются в более токсичные метаболиты: например, хлорофос превращается в более токсичный диметилдихлорвинилфосфат (ДДВФ), карбофос — молооксон, метилмеркаптофос — сульфаксид и сульфон. Метаболизм осуществляется путем окисления, гидролиза эстеразами и переноса частей молекулы к глутатиону.
ФОС обладают функциональной кумуляцией, вследствие чего они могут вызывать хронические отравления, однако способность к материальной кумуляции у них выражена значительно слабее, чем у хлорорганических соединений.
3. Механизм токсического действия ФОС
3.1. Теория антихолинэстеразного действия
Благодаря выяснению химической природы передачи нервного возбуждения стало возможным открытие механизма действия органофосфатов.
Установление роли ацетилхолина в процессе передачи нервного возбуждения привлекало внимание исследователей в изучению строения и функции ферментов, названных холинэстеразами (ХЭ), обеспечивающих быстрый гидролиз ацетилхолина (АХ).
Ацетилхолин – медиатор в ЦНС при передаче импульсов с двигательных нервов на мышцы, во всех ганглиях, при переходе возбуждения с постганглионарных парасимпатических волокон на эффекторные клетки, а также с постганглионарных симпатических волокон, иннервирующих потовые железы.
Результат токсического действия ФОС определяется сходством строения органофосфатов со строением естественного субстрата ХЭ – АХ. При взаимодействии ХЭ с АХ образуется ацетилированный фермент, представляющий собой непрочное соединение, которое быстро гидролизуется. В результате активные центры ХЭ освобождаются для новых реакций с АХ. Вступая во взаимодействие с ФОС, ХЭ образует с ним устойчивый фосфорилированный фермент, устойчивый к гидролизу и неспособный реагировать с АХ. Такой фермент утрачивает свою основную каталитическую функцию, а потому гидролиз АХ замедляется или полностью прекращается, накапливаясь в синапсах. Накопление АХ вызывает возбуждение холинорецепторов, что приводит к перевозбуждению нервной системы, судорогам, а впоследствии к угнетению и параличу нервной системы.
Взаимодействие ФОС и АХЭ проходит в две фазы и может быть представлено следующим образом:
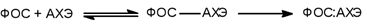
Процесс превращения образовавшейся в первой фазе обратимо фосфорилированной холинэстеразы в необратимо связанную форму называется «старение» фосфорилхолинэстеразы. Скорость «старения» зависит от строения алкильных радикалов при атоме фосфора: чем «тяжелее» радикалы, тем ниже скорость «спонтанной реактивации» и выше скорость «старения». Так АХЭ, ингибированная VX (R -OC2H5), стареет чрезвычайно медленно, зарином (R -OCН(СH3)2) – в течение нескольких часов, зоманом (R -OCНСН3С(СH3)3) – в считанные минуты. В основе лежит процесс отщепления алкильных радикалов от атома фосфора, связанного с активным центром, энзима. При этом одновременно изменяется конформация белковой части энзима.
Накопление ацетилхолина вследствие угнетения ацетилхолинэтероза (АХЭ) приводит к перевозбуждению М-Н-холинреактивных систем на периферии и в центральной нервной системе.
Перевозбуждение м-холинорецепторов – мускариноподобное действие, которое клинически выражается перевозбуждением парасимпатической нервной системы (миоз, спазм аккомодации, бронхо-спазм, одышка, удушье, бронхорея, брадикардия, гиперсаливация, спазмы кишечника, тенезмы, повышенная потливость, сокращение матки и мочевого пузыря).
Перевозбуждение Н-холинорецепторов – никотиноподобный эффект, проявляется как перевозбуждение симпатических ганглиев и мионевральных синапсов поперечнополосатой мускулатуры (фибрилляция мышц, общая слабость мышц и дыхательной мускулатуры, ишемия миокарда и головного мозга). Кроме этого, выделяют центральное действие ФОС, которое зависит как от накопления ацетилхолина, так и от других причин (кислородного голодания и др.) (головная боль, страх, возбуждение, потеря сознания, тонико-клонические судороги, кома, паралич дыхательного центра).
При высоких концентрациях ФОС развивается стойкий синаптический блок (курареподобное действие), вызывающий паралич диафрагмы и обуславливающий молниеносную форму клиники интоксикации.
3.2. Теория неантихолинэстеразного действия
Наряду с широко рассматриваемой антихолинэстеразной теорией действия ФОВ, многочисленными исследованиями указывается на то, что она не исчерпывает всех вариантов первичных фармакологических реакций, ответственных как за лечебные, так и за токсические эффекты этих химических соединений.
Действие на холинорецепторы
Из возможных неантихолинэстеразных механизмов наиболее важным является действие ФОС на холинорецепторы. Поскольку и холинорецепторы, и холинэстераза адаптированы к одному и тому же нейромедиатору, ингибиторы холинэстеразы могут проявить активность и по отношению к холинорецепторам.
По-видимому, блокада проведения нервно-мышечного сигнала, развивающаяся при смертельной интоксикации ФОС, связана не только со стойким деполяризующим действием избыточного количества ацетилхолина, но и с прямым действием ФОС на нервно-мышечные синапсы (по типу действия деполяризующих миорелаксантов). Так, в эксперименте на изолированном нервно-мышечном препарате млекопитающего, при внесении в инкубационную среду достаточной дозы ФОС, наблюдается полное прекращение передачи нервного импульса с нервного волокна на мышцу. Однако через некоторое время на фоне практически “тотального” угнетения активности холинэстеразы отмечается восстановление нервно-мышечной проводимости в синапсах. Восстановление нормального проведения нервного импульса у лиц, перенесших интоксикацию ФОС, осуществляется за счет медленно протекающих процессов дэфосфорилирования АХЭ (“спонтанная реактивация”), синтеза АХЭ в перикарионе нервных клеток de novo и транспорта ее в нервные окончания, снижения содержания ацетилхолина в синаптической щели, десенситизации холинорецепторов (понижение чувствительности к ацетилхолину).
Нехолинэргические механизмы токсического действия
Помимо действия на холинореактивные структуры, ФОС, в высоких дозах, обладают прямым повреждающим действием на клетки различных органов и тканей (нервной системы, печени, почек, системы крови и т.д.), в основе которого лежат общие механизмы цитотоксичности: нарушение энергетического обмена клетки; нарушение гомеостаза внутриклеточного кальция; активация свободнорадикальных процессов в клетке; повреждение клеточных мембран. Чем менее токсично ФОС, тем значимее роль указанных механизмов в развитии проявлений тяжелого поражения данным токсикантом. Существуют ФОС, полностью лишенные антихолинэстеразной активности, токсичность которых обусловлена исключительно их цитотоксическим действием (три-о-крезилфосфат).
4. Пути поступления, распределения, биотрансформации и выведения вещества
ФОС хорошо всасываются через органы дыхания, слизистые, кожные покровы благодаря своей способности хорошо растворяться в жирах. Не обладая раздражающим действием в месте проникновения, органофосфаты всасываются практически незаметно. Ускорению всасывания ФОС способствуют любые повреждения кожи и слизистых, что обуславливает необходимость защиты не только органов дыхания, но и кожных покровов при работе с фосфорорганическими веществами, а также определения их содержания в воде и продовольствии.
В момент всасывания ФОС определенное время накапливается в тканях входных ворот, создавая своеобразное депо. Особенно это характерно для VХ при проникновении через кожные покровы. Затем ФОС постепенно поступают в кровоток, создавая необходимую токсическую концентрацию в крови. Благодаря хорошей растворимости в липидах, органофосфаты быстро проникают через различные мембраны, достигая центральной нервной системы и нервно-мышечных синапсов. Большее токсическое действие при этом оказывается на первый оказавшийся на пути движения яда орган. На его долю приходится большая концентрация токсического вещества. Однако в дальнейшем ФОС распределяются в организме более-менее равномерно. Более высокие концентрации могут при этом определяться в органах выделения (почки, печень, легкие, плазма крови). Худшим проникновением через гемато-энцефалический барьер обладают ФОС, содержащие в своей структуре заряженные атомы серы или азота. Также они не обладают центральным действием.
Обезвреживание ФОС в организме может происходить следующими способами:
- окисление с участием микросомальных ферментов – оксидаз и коферментов – НАДФ.Н2, цитохрома Р-450.;
- ферментативный гидролиз как основной путь обезвреживания ФОС за счёт ферментных систем гидролаз (фосфотазы, карбоксиэстеразы, карбооксиамидазы). Гидролиз обеспечивает превращение жирорастворимых органофосфатов в водорастворимые соединения, которые удаляются из организма почками;
- конъюгация: соединение ФОС с эндогенными молекулами также улучшает растворимость фосфорорганических веществ в воде и ускоряет процесс выведения их из организма. Обычно реакции конъюгации осуществляются после реакций ферментативного гидролиза и разрыва эфирных связей в молекуле токсиканта;
- восстановление – реакция обуславливает обезвреживание отдельных органофосфатов: снижая положительный заряд фосфора, исключается его взаимодействие с активным центром АХЭ, что ведёт к уменьшению токсических свойств ФОС.
В основном фосфорорганические соединения выводятся почками, печенью, а также слизистой кишечника.
5. Особенности клинических проявлений при отравлении
Развитие симптомов отравления ФОВ зависит от многих факторов, в значительной мере от:
- величины поражающей дозы;
- особенностей действия различных ФОВ: их химической стойкости в биологических средах, скорости преодоления гистогематического и гематоэнцефалического барьеров;
- пути поступления токсиканта в организм: ингаляционная, перкутанная, желудочно-кишечная формы.
Степень отравления влияет в первую очередь на показатели активности холистеразы. Выделяют три степени тяжести:
· лёгкая степень (миотическая, диспноэтическая, кардиальная, желудочно-кишечная, невротическая формы);
· средняя степень (бронхоспастическая форма);
· тяжёлая степень (генерализованная форма).
По течению:
- острая форма (молниеносное течение и замедленное);
- хроническая форма.
Лёгкая степень поражения возникает через несколько минут после воздействия вещества и характеризуется эмоциальной лабильностью. Снижение активности ХЭ составляет 30-50% от исходного значения. Преобладают симптомы, связанные с расстройством зрения — понижение остроты зрения, миоз, слезотечение, понижение внутриглазного давления. Иногда наблюдаются боли за грудиной, незначительное учащение пульса, в ряде случаев – повышение артериального давления. Кроме того, затруднение дыхания, бронхоспазм и снижение жизненной ёмкости лёгких. Желудочно-кишечная форма проявляется в виде тошноты, слюнотечения, спазма кишечника. Иногда наблюдается кратковременный лейкоцитоз, но существенные изменения крови при лёгком отравлении отсутствуют.
При отравлениях средней степени тяжести появляется бронхоспастический криз, схожий с приступами удушья при бронхиальной астме, приступы которого повторяются каждые 10-15 минут. В перерыве между приступами дыхание затруднено. Возникает чувство страха, раздражительность, нарушается восприятие окружающей обстановки. К другим симптомам относятся обильное слюнотечение, повышенное артериальное давление, рвота, понос, усиленная секреция бронхиальных и потовых желез. Наблюдаются фибриллярные подёргивания мышц. Зрачки резко сужены. Нейтрофильный лейкоцитоз. Снижение активности ХЭ на 50-70%.
При отравлении тяжёлой степени – молниеносное и острое развитие патологического состояния. Миоз наступает в течение одной минуты (в терминальном периоде зрачки могут расширяться). Кожа белая, влажная. В течение 2-4 минут после отравления начинают периодически возникать приступы удушья, приводящие к нарушению дыхания. Отмечается артериальная гипотензия и брадикардия. В течение 5-7 минут появляются клонико-тонические судороги и мышечные подергивания отдельных мышечных групп. Изо рта и носа выделяется пенистая жидкость, наблюдаются непроизвольное мочеиспускание и дефекация. В крови – значительный лейкоцитоз. В течение десяти минут — кома с арефлексией и адинамией. Смерть наступает в результате асфиксии — следствия паралича дыхательной мускулатуры — или паралича сосудодвигательного центра и остановки сердца в течение 10-15 минут. Угнетение активности холинэстеразы на 70-80 %.
6. Основные принципы терапии отравления
- при попадании яда на кожу поражённые участки необходимо промыть щелочным раствором натрия гидрокарбоната;
- при ингаляции на пострадавшего надевают противогаз и выводят из заражённой зоны;
- при пероральном отравлении производится зондовое промывание желудка 10–15 л воды 12–15 ◦С до чистых промывных вод, введение через зонд вазелинового масла 300–500 мл. Промывание проводят до полной ликвидации мускарино- и никотиноподобного действия токсиканта;
- для удаления яда из кишечника применяются адсорбирующие средства – уголь активированный, слабительные средства – магния сульфат, высокие сифонные клизмы, кишечный лаваж – макрогол (форлакс);
- форсированный диурез – фуросемид (лазикс), гемосорбция, гемодиализ, перитонеальный диализ, гемофильтрация;
- специфическая (антидотная) терапия – атропин (атропина сульфат) внутривенно;
- в течение первых суток с момента отравления введение реактиватора ацетилхолинэстеразы – дипироксим;
- интубация трахеи, ИВЛ;
- симптоматическая терапия – диазепам (сибазон).
Для снижения мускариноподобного действия вводят атропина сульфат. Экстракорпоральные методы детоксикации (эффективны только на ранних сроках отравления) – гемосорбция, гемодиализ, гемофильтрация.
Табл. 6.1. Основные направления терапии при отравлении ФОС
| Основные направления | Группы препаратов |
| Нормализация гомеостаза внутриклеточного кальция | Блокаторы Ca каналов (верапамил, нифедипин и др.) |
| Нормализация электролитного обмена | Электролиты (препараты калия) |
| Устранение гипоксии | Кислородотерапия. Антигипоксанты (олифен, цитохром «С»). Препараты янтарной кислоты |
| Угнетение перекисного окисления липидов | Антиоксиданты (токоферол, аскорбат) |
| Защита клеток мозга от повреждения возбуждающими аминокислотами | Антагонисты глутаматных рецепторов (кеталар и др.) |
| Устранение психических нарушений | Нейролептики. Антидепрессанты. Психостимуляторы |
| Устранение судорожного синдрома | Противосудорожные (производные бензодиазепина; производные барбитуровой кислоты; антагонисты ВАК и т.д.) |
| Стимуляция дыхания | Этимизол |
| Поддержание сердечно-сосудистой | Сердечные гликозиды |
Антидотная терапия основана с одной стороны на блокировании холинорецепторов и препятствовании действию эндогенного АХ, а с другой – на нормализации обмена ацетилхолина путём восстановления активности ХЭ. То есть антидоты условно можно разделить на две группы: холинолитики и реактиваторы ХЭ.
Табл. 6.2 Антидоты
| Направление | Препараты |
| Защита холинорецепторов | Холинолитические (антихолинэргические) средства |
| Реактивация холинэстеразы* | Оксимы |
| Защита холинэстеразы от необратимого угнетения ФОС | Обратимые ингибиторы холинэстеразы |
| Нейтрализация ФОС | Оксимы; специфические антитела |
| Ускорение метаболизма ФОС | Индукторы микросомальных ферментов |
| Возмещение холинэстеразы | Препараты очищенной холинэстеразы |
| Подавление синтеза и высвобождения ацетилхолина | Производные дифенилгликолятов, гемихолиний |
* Реактиваторы холинэстеразы относят к специфическим антидотам, их применяют в первые сутки с момента отравления, когда органофосфаты ещё не связаны с АХЭ прочно и необратимо.
В настоящее время используют аллоксим и диэтиксим.
Аллоксим в 1-й стадии отравления вводят в/м по 0,075 г через 3 ч.
во 2-й – по 0,15 г через 3 ч первые 12 ч, затем по 0,075 г через 3 ч.
в 3-й стадии – по 0,15 г через 2 ч первые 12 ч, затем по 0,075 г через 2 ч.
Диэтиксим в 1-й стадии отравления вводят внутримышечно по 0,5 г через 4 ч;
во 2-й – по 0,5 г через 2 – 3 ч;
в 3-й стадии – по 0,5 г через 1 – 2 ч.
Заключение
Несмотря на запрет химического оружия от 1993 года, существует угроза применения ядов нейротоксического действия (зарин, зоман, V-газы) террористами и в локальных конфликтах. Кроме того, с ростом населения требуются большие объёмы урожая, что приводит к невозможности отказа или снижения используемых количеств пестицидов, в частности инсектицидов. Поэтому отравления фосфорорганическими соединениями в сфере сельского хозяйства и, в частности, в быту по-прежнему распространены. Таким образом, в настоящее время особое значение имеет проблема поиска антидотных и симптоматических средств, а также специальная подготовка медицинских специалистов, компетентных в вопросах оказания помощи при отравлении органофосфатами.
Список использованной литературы
1. Темченко А.В., Фосфорорганические соединения: токсикологическая характеристика и степень опасности// Международный студенческий научный вестник. – 2017. - № 4. – с. 289-291.
2. Калинина Т.С., Бородин В.А., Отравления фосфорорганическими веществами, признаки отравления ФОВ, лечение// Проблемы обеспечения безопасности при ликвидации последствий черезвычайных ситуаций, - 2018. – Том 1. – с. 249-250.
3. Кундиев Ю.И., Всасывание пестицидов через кожу и профилактика отравлений. – Киев, 1975. – 200 с.
4. Справочники MSD.
5. Дж. Робертс, М. Касерио, Основы органической химии. – Издание 2-ое. – М., 1978. – 1730 с.
6. Минакина Л.Н., Зобнин Ю.В., Клёц О.П., Одинец А.Д., Куклина Л.Б., Основные принципы лечения острых отравлений. Учебное пособие для студентов. – Иркутск, 2019. – 64 с.
7. Фосфорорганические отравляющие вещества// Газета «Коммерсантъ». – 2004. - №99. – с.5.
8. Studbooks.net
|
|
|
© helpiks.su При использовании или копировании материалов прямая ссылка на сайт обязательна.
|