
- Автоматизация
- Антропология
- Археология
- Архитектура
- Биология
- Ботаника
- Бухгалтерия
- Военная наука
- Генетика
- География
- Геология
- Демография
- Деревообработка
- Журналистика
- Зоология
- Изобретательство
- Информатика
- Искусство
- История
- Кинематография
- Компьютеризация
- Косметика
- Кулинария
- Культура
- Лексикология
- Лингвистика
- Литература
- Логика
- Маркетинг
- Математика
- Материаловедение
- Медицина
- Менеджмент
- Металлургия
- Метрология
- Механика
- Музыка
- Науковедение
- Образование
- Охрана Труда
- Педагогика
- Полиграфия
- Политология
- Право
- Предпринимательство
- Приборостроение
- Программирование
- Производство
- Промышленность
- Психология
- Радиосвязь
- Религия
- Риторика
- Социология
- Спорт
- Стандартизация
- Статистика
- Строительство
- Технологии
- Торговля
- Транспорт
- Фармакология
- Физика
- Физиология
- Философия
- Финансы
- Химия
- Хозяйство
- Черчение
- Экология
- Экономика
- Электроника
- Электротехника
- Энергетика
Задание по физике 21 гр. 15.12.20.
Задание по физике 21 гр. 15.12.20.
Тема урока: Решение задач по теме «Атомное ядро. Естественная радиоактивность»
Цель занятия: повторить материал, связанный со строением атома, атомного ядра, научиться определять энергию связи между частицами в ядрах атомов, записывать ядерные реакции, находить продукты радиоактивных превращений.
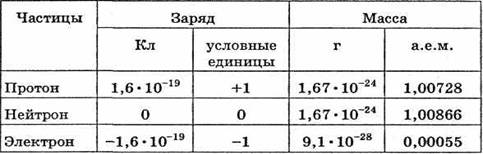
Для этого нам нужна таблица Менделеева, табличные значения масс частиц, входящих в состав атома.
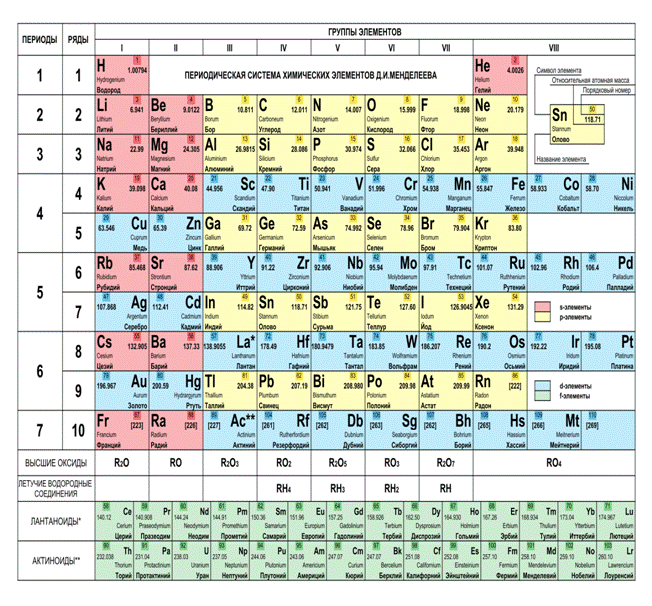
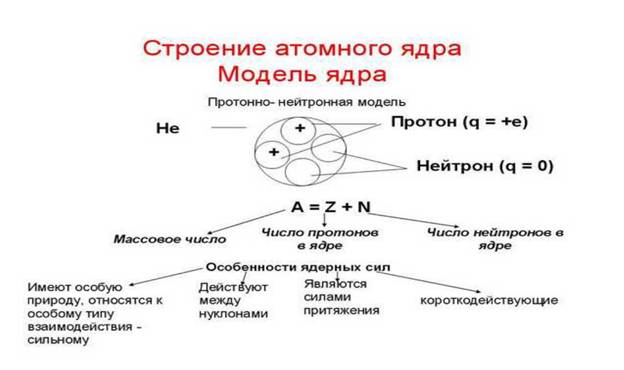
1).Известно, что атом - наименьшая частица химического элемента, обладающая всеми его свойствами. Атом состоит из ядра, в котором находятся нейтроны и протоны и электронов - отрицательно заряженных частиц, которые движутся вокруг ядра по орбитам. При этом нужно помнить, что число электронов в атоме всегда определяется порядковым номером элемента в таблице Менделеева. Например, если кислород находится на 8 месте, то у него восемь электронов. Так как атом в целом электрически нейтрален и заряд электронов равен заряду протонов, то число протонов в ядре всегда равно числу электронов: Ze=Zp, поэтому в ядре атома кислорода восемь протонов: Zp=8. Чтобы найти число нейтронов в ядре нужно вспомнить, что протоны и нейтроны вместе определяют атомную массу ядра атома и А= Zp + N, .где N. - число нейтронов. Так как атомная масса кислорода составляет 16, то число нейтронов в атоме кислорода N= 16-8=8. Таким образом в атоме кислорода 8 протонов, 8 нейтронов и 8 электронов.
Задание1. Определим число частиц в атомах урана 92U238 Решение: У атома урона порядковый номер 92, а атомная масса 238. Тогда: Ze = 92 - число электронов
Zр = 92 – число протонов т.к.Ze=Zp
N = А- Zp =238 - 92= 146 нейтронов.
Задание 2. Определим энергию связи между протонами и нейтронами в ядре атома урана.
Для этого воспользуемся формулой : Есв= Δm·c2, где
с= 3·108 м/с – скорость света; Δm - дефект массы, который рассчитывается по формуле: Δm =( Zp·mР + N·mN) – mЯ 1а.е.м. = 931,5 МэВ/с2 - одна атомная единица массы Так как mР = 1,00728 а.е.м., а нейтрона mN =1,00866 а.е.м., масса ядра атома урана mЯ = 238.12376а.е.м. –из таблицы Менделеева, то Δm = ( 92·1,00728+ 146·1,00866) – 238,12376 = (92,66976+147,26436) -238,12376 = 5,81 а.е.м.= 5,81· 931,5 МэВ/с2 =5407,8 МэВ/с2
Есв= Δm·c2 =5407,8 МэВ/с2·с2=5407,8 МэВ - энергия связи между протонами и нейтронами в ядре урана. Результат можно получить в Дж.
1 МэВ = 1,6·10-13 Дж
2).Рассмотрим естественную радиоактивность - самопроизвольное превращение ядер атомов радиоактивного вещества, сопровождающееся 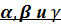 – излучением.
– излучением.
Вспомним, что 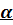 –излучение - поток положительно заряженных частиц- ядер атомо гелия 2He4
–излучение - поток положительно заряженных частиц- ядер атомо гелия 2He4 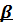 - излучение - поток быстрых электронов - -1е0
- излучение - поток быстрых электронов - -1е0
Посмотрим, во что превратятся ядра уран 92U238 при 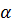 – распаде. Для этого составим уравнение ядерной реакции:
– распаде. Для этого составим уравнение ядерной реакции:
 92U238 2He4 + Z ХA,где Z ХA – ядро неизвестного химического элемента.
92U238 2He4 + Z ХA,где Z ХA – ядро неизвестного химического элемента.
Для того, чтобы определить, какое новое ядро появилось , воспользуемся законом сохранения зарядовых и массовых чисел.
По закону сохранения заряда (нижние индексы в обозначении ядер):
92= 2+ Z, откуда Z=90
По закону сохранения массы (верхние индексы) : 238=4+ А, откуда А=234
Таким образом, в результате 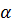 – распад получилось новое ядро с порядковым номером на2 клеточки ближе у к началу таблицы Менделева на 2 клеточки - ядро атома тория 90Th234
– распад получилось новое ядро с порядковым номером на2 клеточки ближе у к началу таблицы Менделева на 2 клеточки - ядро атома тория 90Th234
При 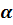 – распаде обрвазуются ядра нового химического элемента, расположенного на 1 клеточку ближе к началу таблицы Менделева. (правило смещения при
– распаде обрвазуются ядра нового химического элемента, расположенного на 1 клеточку ближе к началу таблицы Менделева. (правило смещения при 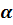 - распаде)
- распаде)
 92U238 2He4 +90Th234
92U238 2He4 +90Th234
 Аналогично при
Аналогично при 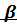 - распаде : 92U238 -1е0 + Z ХA
- распаде : 92U238 -1е0 + Z ХA
По закону сохранения заряда (нижние индексы в обозначении ядер):
92= -1 + Z, откуда Z+ 92+1= 93 – порядковый номер нового ядра - это нептуний Np
По закону сохранения массы (верхние индексы) : 238=0+ 238
 Таким образом : 92U238 -1е0 + 93Np238
Таким образом : 92U238 -1е0 + 93Np238
|
|
|
© helpiks.su При использовании или копировании материалов прямая ссылка на сайт обязательна.
|