
- Автоматизация
- Антропология
- Археология
- Архитектура
- Биология
- Ботаника
- Бухгалтерия
- Военная наука
- Генетика
- География
- Геология
- Демография
- Деревообработка
- Журналистика
- Зоология
- Изобретательство
- Информатика
- Искусство
- История
- Кинематография
- Компьютеризация
- Косметика
- Кулинария
- Культура
- Лексикология
- Лингвистика
- Литература
- Логика
- Маркетинг
- Математика
- Материаловедение
- Медицина
- Менеджмент
- Металлургия
- Метрология
- Механика
- Музыка
- Науковедение
- Образование
- Охрана Труда
- Педагогика
- Полиграфия
- Политология
- Право
- Предпринимательство
- Приборостроение
- Программирование
- Производство
- Промышленность
- Психология
- Радиосвязь
- Религия
- Риторика
- Социология
- Спорт
- Стандартизация
- Статистика
- Строительство
- Технологии
- Торговля
- Транспорт
- Фармакология
- Физика
- Физиология
- Философия
- Финансы
- Химия
- Хозяйство
- Черчение
- Экология
- Экономика
- Электроника
- Электротехника
- Энергетика
Изотопы. Открытие нейтрона
Изотопы
Изотопы – ядра одного и того же химического элемента которые отличаться числом нейтронов (одинаковый заряд, разные массы).
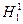 водород (стабилен), с кислородом образует обычную воду, которая кипит при температуре tk=1000C ,а замерзает при температуре tпл=00C
водород (стабилен), с кислородом образует обычную воду, которая кипит при температуре tk=1000C ,а замерзает при температуре tпл=00C
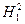 дейтерий (стабилен), с кислородом образует тяжелую воду которая кипит при температуре tk=101,20C, а замерзает при температуре tпл=3,80C
дейтерий (стабилен), с кислородом образует тяжелую воду которая кипит при температуре tk=101,20C, а замерзает при температуре tпл=3,80C
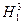 тритий - радиоактивный элемент с периодом полураспада T=12 лет
тритий - радиоактивный элемент с периодом полураспада T=12 лет
Открытие нейтрона
В 1932 г. Дж. Чедвиг доказал, что поток α – частиц выбивает из бериллия нейтральные частицы имеющие массу, а 1836 большую чем у электрона и чуть больше массы протона.

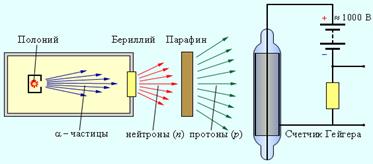
Нейтрон – нестабильная частица: свободный нейтрон за 15 минут распадается на протон, электрон и нейтрино – частицу лишенную массы покоя
В 1931 году В. Паули высказал предположение, что при распаде нейтрона выделяется еще одна частица с нулевыми значениями массы и заряда, которая уносит с собой часть энергии. Новая частица получила название нейтрино

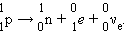
Строение атомного ядра
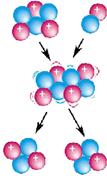
Атомные ядра различных элементов состоят из двух частиц (нуклонов) – протонов и нейтронов.
Число протонов, входящих в состав атомного ядра, обозначают символом Z и называют зарядовым числом или атомным номером. Число нейтронов обозначают символом N.
Заряд ядра равен Z·e.
Общее число нуклонов называют массовым числом A: A = Z + N.
|
|
|
© helpiks.su При использовании или копировании материалов прямая ссылка на сайт обязательна.
|