- Автоматизация
- Антропология
- Археология
- Архитектура
- Биология
- Ботаника
- Бухгалтерия
- Военная наука
- Генетика
- География
- Геология
- Демография
- Деревообработка
- Журналистика
- Зоология
- Изобретательство
- Информатика
- Искусство
- История
- Кинематография
- Компьютеризация
- Косметика
- Кулинария
- Культура
- Лексикология
- Лингвистика
- Литература
- Логика
- Маркетинг
- Математика
- Материаловедение
- Медицина
- Менеджмент
- Металлургия
- Метрология
- Механика
- Музыка
- Науковедение
- Образование
- Охрана Труда
- Педагогика
- Полиграфия
- Политология
- Право
- Предпринимательство
- Приборостроение
- Программирование
- Производство
- Промышленность
- Психология
- Радиосвязь
- Религия
- Риторика
- Социология
- Спорт
- Стандартизация
- Статистика
- Строительство
- Технологии
- Торговля
- Транспорт
- Фармакология
- Физика
- Физиология
- Философия
- Финансы
- Химия
- Хозяйство
- Черчение
- Экология
- Экономика
- Электроника
- Электротехника
- Энергетика
Вывод молекулярных формул органических веществ
Вывод молекулярных формул органических веществ
по продуктам сгорания
Задача 1.Какова молекулярная формула углеводорода, имеющего плотность 1,97 г/л, если при сгорании 4,4 г. его в кислороде образовалось 6,72 л. СО2 и 7,2 г. Н2О.
Общепринятое решение
| Дано: M (CхHу) = 4,4 г. ρ (н.у.) = 1,97 г/л V (СО2) = 6,72 л. m (Н2О) = 7,2 г. | Решение: Составляем пропорции: |
| Вывести формулу CхHу - ? |
Задача 2 Общепринятое решение.
1) При сгорании 3г. углеводорода было получено 8,8 г.углекислого газа,5,4 г. воды. Относительная плотность углеводорода по воздуху равна 1,03. Определите молекулярную формулу углеводорода.
3г. 8,8г. 5,4г.
CxHу + О2 = СО2 + Н2О
 44г 18г
44г 18г
Т.к. -.это углеводород = кроме углерода и водорода в нём больше ничего не содержится. Весь углерод из углеводорода перешёл в 8,8г СО2, а водород в 5,4г Н2О.
1. Рассчитаем Мr (CxHу)
Мr (CxHу) = 1,03 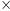 29 = 30
29 = 30
2.Рассчитаем массу углерода в 8,8г СО2
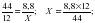 Х = 2,4г
Х = 2,4г
3. Рассчитаем массу водорода в 5,4г Н2О.
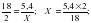 Х = 0,6
Х = 0,6
4. Рассчитаем количество атомов углерода и водорода
γ = т/Аr; х : у = 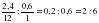 ;= С2Н6
;= С2Н6
5. Устанавливаем простейшая формула или истинная
Мr (С2Н6) = 12  2 + 6 = 30; Это истинная формула
2 + 6 = 30; Это истинная формула
Задача 1
| анализ | v=m/M v=V/Vm |
| Найдем М углеводорода | М (CхHу) = Vm · ρ М (CхHу) = 22,4л/моль ·1,97г/л = 44г/моль |
| По условию | 4.4г 6.72л 7.2г |
| Уравнение | CxHу + О2 = СО2 + Н2О |
| М (г/моль) | 44 18 |
| М v (л/моль) | 22.4 |
| Количество (моль) | 0.1 0.3 0.4 |
| Отношение количеств | 1 3 4 |
| Количество элемента | 3 8 |
| Молекулярная формула | C3H8 |
Задача 2
| М углеводорода | Мr (CxHу) = 1,03  29 = 30
М=30г/моль 29 = 30
М=30г/моль
|
| Массы по условию | 3г. 8,8г. 5,4г. |
| уравнение | CxHу + О2 = СО2 + Н2О |
| Молярная масса г/моль | 30  44 18 44 18
|
| Количество вещества(моль) | 0.1 0.2 0.3 |
| Отношение количеств веществ | 1 2 3 |
| Количество элементов Углерода водорода | 2 6 |
| Формула | С2 Н6 |
|
|
|
© helpiks.su При использовании или копировании материалов прямая ссылка на сайт обязательна.
|